Mit der weitreichenden Anwendung von mRNA-COVID-19-Impfstoffen in großen Bevölkerungsgruppen wurde die Sicherheit von mRNA-Impfstoffen bestätigt. mRNA verfügt über die Fähigkeit, jedes beliebige Protein auszudrücken und bietet potenzielle Lösungen für verschiedene unerfüllte klinische Bedarfe.
Yaohai Bio-Pharma bietet eine umfassende Lösung für die Forschung und Entwicklung sowie die GMP-Produktion von mRNA an, gestützt auf ein starkes Forschungsplattform und ein konformes GMP-System. Unsere Dienstleistungen sind darauf abgestimmt, die spezifischen Anforderungen unserer Kunden zu erfüllen und ihnen hochwertige mRNA-Wirkstoffe und LNP-mRNA-Endprodukte in Mengen von Milligramm bis Gramm bereitzustellen, sowie detaillierte Entwicklungs- und Produktionsberichte und Testberichte.
Wir haben von unserem Partner NanoStar Pharmaceuticals eine Lizenz für die LNP-Patentechnologie erhalten, um zukünftige potenzielle Patentstreitigkeiten zu vermeiden.
mRNA/LNP Gesamtlösung von Yaohai Bio-Pharma
Liefergegenstände
| Qualitätsstufe |
Liefergegenstände |
Spezifikation |
ANWENDUNGEN |
| nicht-GMP |
Wirkstoff, mRNA |
0,1~10 mg (mRNA) |
Präklinische Forschung wie Zelltransfektion, Entwicklung analytischer Methoden, Vorstabilitätstudien, Formulierungsentwicklung |
| Arzneimittelprodukt, LNP-mRNA |
| GMP, Sterilität |
Wirkstoff, mRNA |
10 mg~70 g |
Investigational new drug (IND), Klinische Versuchserlaubnis (CTA), Klinisches Versorgungsmaterial, Biologische Lizenzantrag (BLA), Kommerzielle Versorgung |
| Arzneimittelprodukt, LNP-mRNA |
5000 Ampullen oder Fertigspritzen/Karaffen |
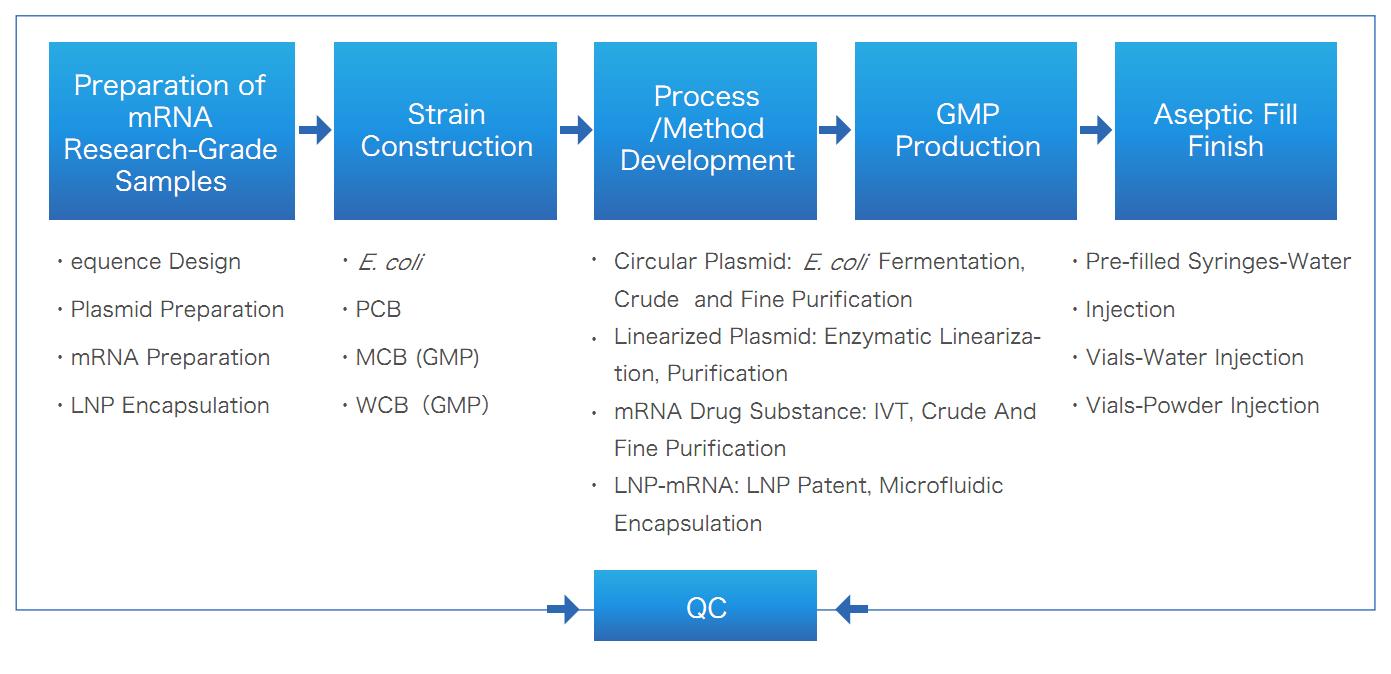
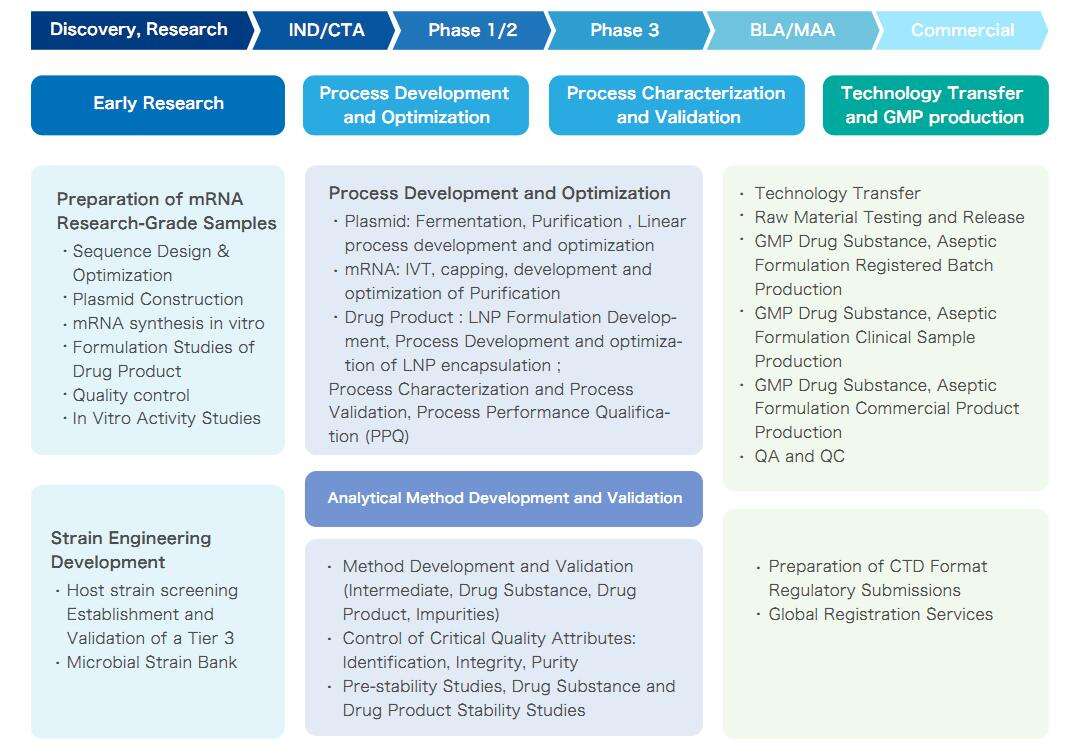
Yaohais mRNA CRDMO Dienstleistung, die den gesamten Lebenszyklus von mRNA abdeckt
Plattformmerkmale
Plasmid-DNA-Plattform
- Mehrere 7L Fermentiersysteme, tierfrei im gesamten Prozess
- Klare Nachverfolgbarkeit von Plasmiden und Wirtsbakterien, ohne deklaratorische Hindernisse
- Der Ausbeute von Plasmid mit Poly-A über 500 mg/L
- Poly-A-Verlustrate weniger als 5 bp
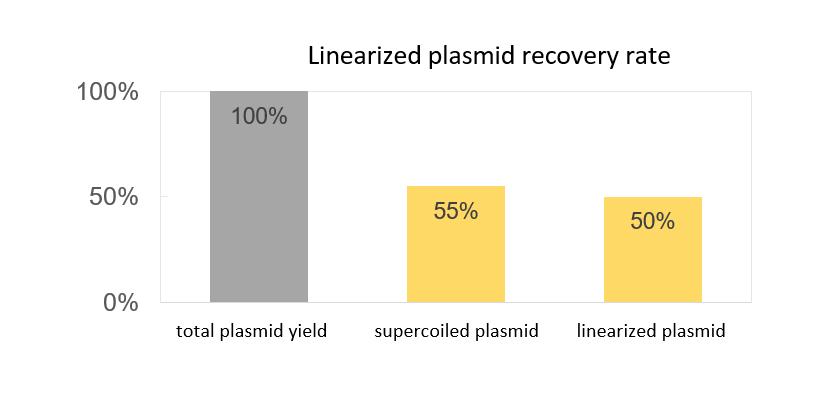
- Anteil supercoiler Plasmide über 90%; Rückgewinnungsrate über 55%
- Linearisierungseffizienz über 99%; Rückgewinnungsrate linearisierter Plasmide von 90%
Wirkstoff-Plattform für mRNA
- Mehrere 1L Reaktoren (GMP)
- Ein hohes Transkriptionsverhältnis von 1:120 ermöglicht einen skalierbaren IVT-Prozess
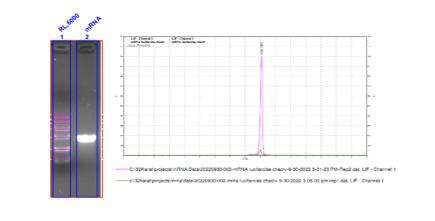
- mRNA-Integrität über 98 %
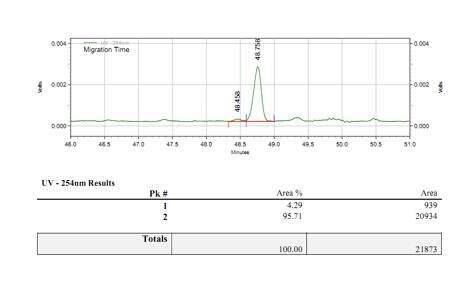
- Stabiler Capping-Prozess mit einer Capping-Rate von über 95 %
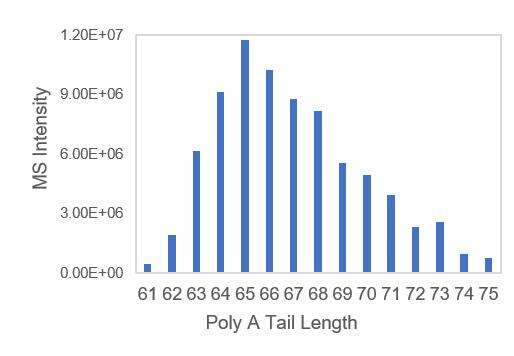
- Transkriptionstemplates mit A-Tails, die eine gleichmäßige Verteilung der Poly-A-Tails sicherstellen.
LNP-Einkapselungsplattform
- LNP-Patentechnologie autorisiert durch unsere Partner, um Patentstreitigkeiten für unsere Kunden zu vermeiden.



(Unsere Partner)
- Durchführung eines hochgradig flexiblen Mikrofluidik-Einkapselungsprozesses, wodurch eine Einkapslungseffizienz von über 95 % erreicht wird.
- Die LNP-Partikelgröße liegt zwischen 80-100 nm, mit einem niedrigen polydisperen Index (PDI) von 0,05, was auf eine gleichmäßige Verteilung der Partikelgrößen hinweist.
- LNP-Partikel weisen eine schwache Ladung auf, mit einem Zeta-Potential von etwa -2,18 mV.
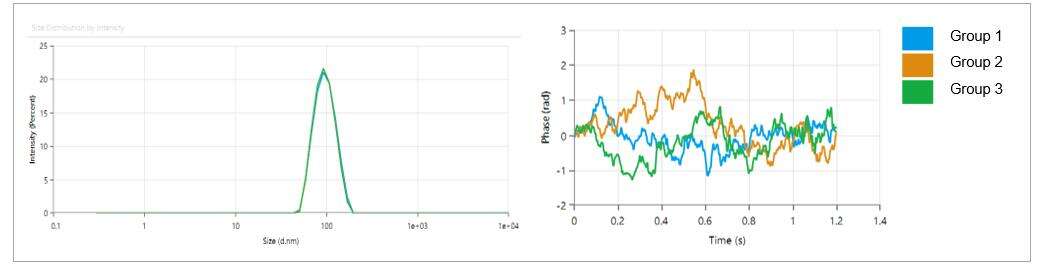
| Prüfposten |
Testverfahren |
Testergebnis |
| Einkapselungseffizienz |
Ribogreen |
92.7% |
| Partikelgröße |
Malvern |
92,07 nm |
| PDI |
Malvern |
0.05 |
| Zeta |
Malvern |
-2,18 mV |
Methodenentwicklungsplattform
Wir bieten eine umfassende Methodenentwicklungsplattform zur Analyse von kreisförmigen und linearisierten Plasmiden, mRNA-Rohstoffen und fertigen LNP-mRNA-Produkten an. Unsere Analysen umfassen eine Vielzahl von Parametern, wie Integrität, Reinheit, Capping-Effizienz, Poly-A-Verteilung, Einkapselungseffizienz, Partikelgröße, LNP-Komponenten und verschiedene Prozessrückstände (HCP, HCD, HCR, dsRNA, Antibiotika, DNase I, T7 RNA-Polymerase, Pockenvirus-Capping-Enzym, 2-O-Methyltransferase etc.).
Partielle Methoden werden wie folgt demonstriert:
Nachweis der Integrität von mRNA (Kapillarelektrophorese)
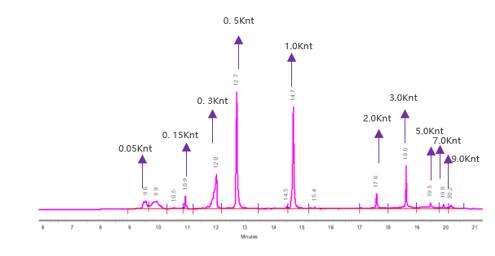
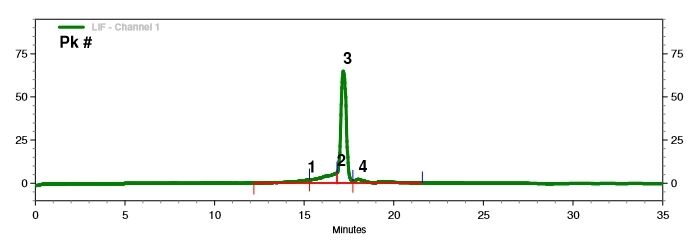
Wir haben optimale Trennbedingungen entwickelt, um mRNA-Moleküle unterschiedlicher Längen präzise zu trennen.
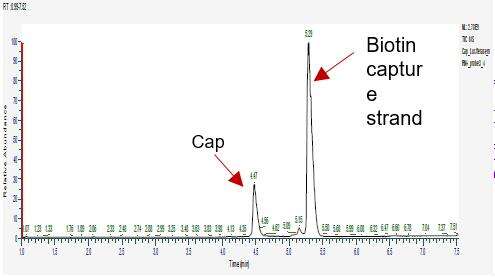
Nachweis der Effizienz der mRNA-Capping (LC-MS)
Wir haben geeignete Bedingungen für die Kлеivuѕg deѕ 5' Endes und die Trennung von 5'-End-Oligonukleotiden entwickelt, wodurch eine genaue Trennung von cappierten und uncappierten Fragmenten ermöglicht wird.
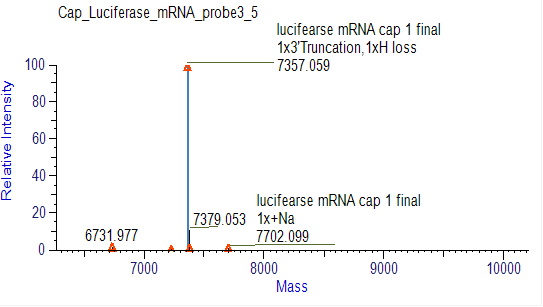
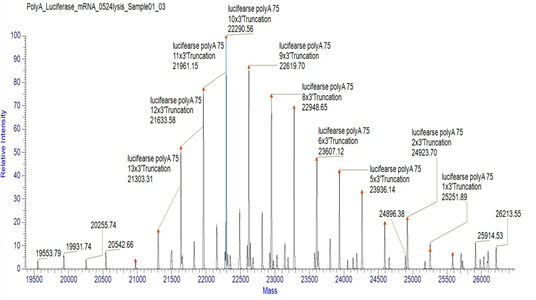
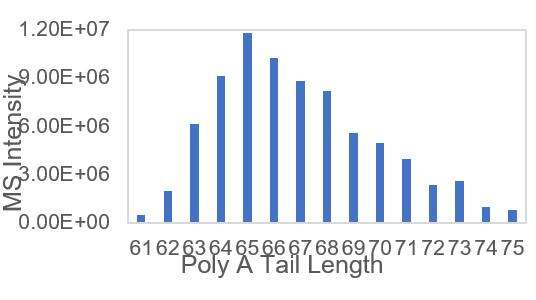
Nachweis der passenden mRNA PolyA-Endverteilung (LC-MS)
Wir haben geeignete Bedingungen für das Abschneiden der 3'-Enden und die Trennung von 3'-End-Oligonukleotiden entwickelt, die eine präzise Bestimmung der Verteilung der PolyA-Schwänze ermöglichen.
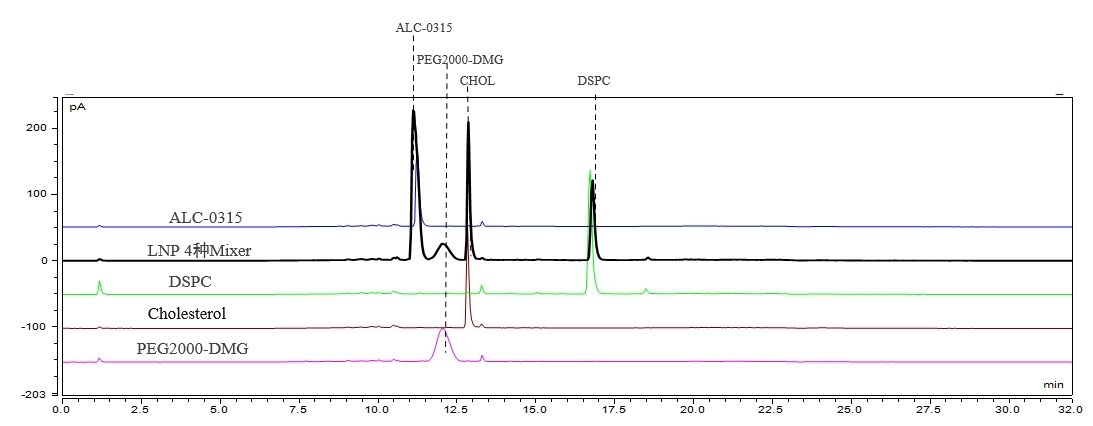
Nachweis der LNP-Komponenten und -Inhaltsstoffe (HPLC-CAD)
Wir haben eine geeignete chromatographische Methode etabliert, die eine Basistrennung der vier LNP-Komponenten erreicht. Diese Methode zeigt eine hervorragende Reproduzierbarkeit.
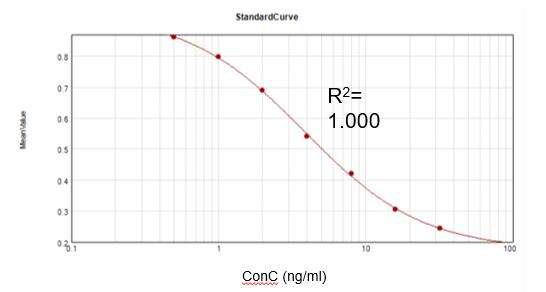
Bestimmung des Restkanamycin-Gehalts (ELISA)
Basierend auf einem kommerziellen Assay-Kit erhielten wir eine geeignete Kalibrierkurve (R2 = 1,000) und erreichten einen Rückgewinnungsgrad von 104,8 %.
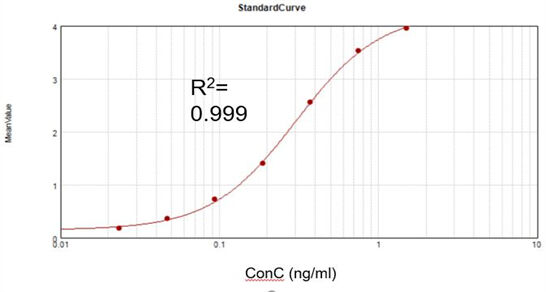
Restkonzentration an dsRNA
Basierend auf einem kommerziellen Assay-Kit erhielten wir eine geeignete Kalibrierkurve (R2 = 0,999) und erreichten einen Rückgewinnungsgrad von 105,5 %.
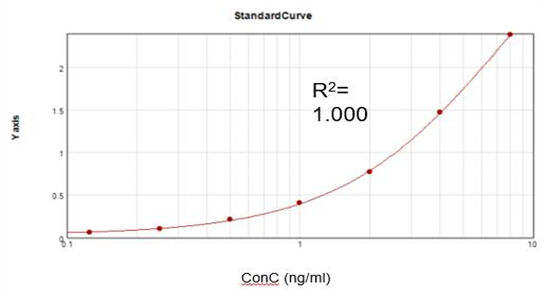
Residueller T7 RNA-Polymerase (Elisa)
Basierend auf einem kommerziellen Assay-Kit erhielten wir eine geeignete Kalibrierkurve (R2 = 1,000) und erreichten einen Rückgewinnungsgrad von 107,9 %.
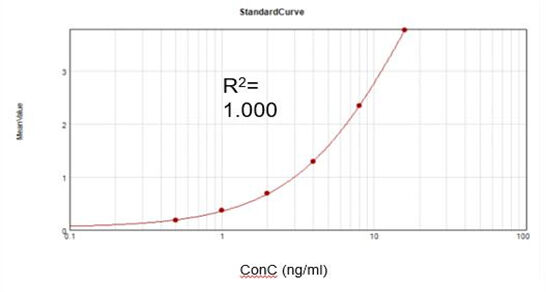
Residuelles Vaccinia-Virus-Capping-Enzym (ELISA)
Basierend auf einem kommerziellen Assay-Kit erhielten wir eine geeignete Kalibrierkurve (R2 = 1,000) und erreichten einen Rückgewinnungsgrad von 92 %.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN






















