Con l'applicazione diffusa dei vaccini mRNA contro il COVID-19 su grandi popolazioni, la sicurezza dei vaccini mRNA è stata validata. L'mRNA ha la capacità di esprimere qualsiasi proteina, offrendo soluzioni potenziali per vari bisogni clinici non soddisfatti.
Yaohai Bio-Pharma offre una soluzione completa per la Ricerca e Sviluppo (R&D) dell'mRNA e la produzione GMP, supportata da una solida piattaforma di ricerca e da un sistema GMP conforme. I nostri servizi sono progettati per soddisfare i requisiti unici dei nostri clienti, fornendo loro sostanze farmaceutiche mRNA di alta qualità e prodotti finiti LNP-mRNA in quantità da milligrammi a grammi, nonché rapporti dettagliati di sviluppo e produzione e rapporti di test.
Abbiamo ottenuto l'autorizzazione per la tecnologia brevettata LNP dal nostro partner, NanoStar Pharmaceuticals, garantendo di evitare possibili contese brevettuali in futuro.
soluzione Integrata mRNA/LNP di Yaohai Bio-Pharma
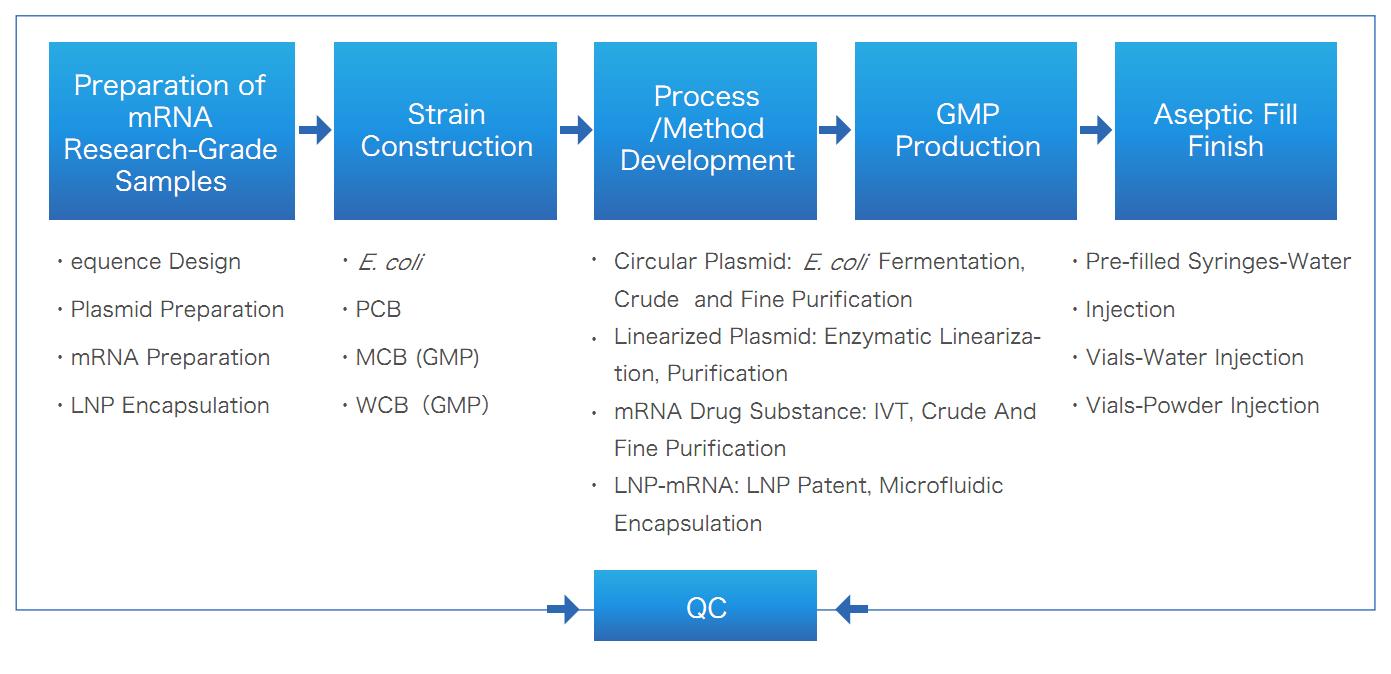
Consegne
| Grado |
Consegne |
Specifiche |
Applicazioni |
| non-GMP |
Sostanza Farmaceutica, mRNA |
0,1~10 mg (mRNA) |
Ricerca preclinica come trasfazione cellulare, Sviluppo di metodi analitici, Studi di prestabilità, Sviluppo di formulazioni |
| Drug Product, LNP-mRNA |
| GMP, Sterilità |
Sostanza Farmaceutica, mRNA |
10 mg~70 g |
Investigational new drug (IND), Autorizzazione del trial clinico (CTA), Fornitura per trial clinici, Richiesta di licenza biologica (BLA), Fornitura commerciale |
| Drug Product, LNP-mRNA |
5000 flaconi o siringhe/cartridge prefissati |
Servizio CRDMO mRNA di Yaohai, che copre l'intero ciclo di vita del mRNA
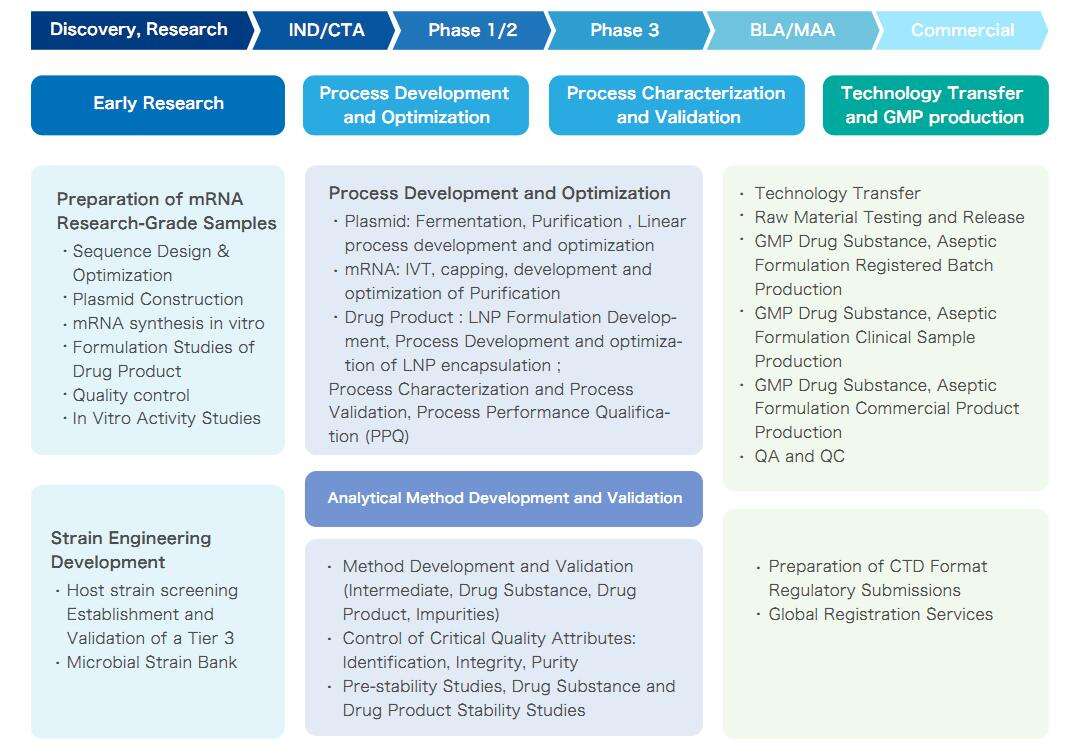
Caratteristiche della Piattaforma
Piattaforma DNA Plasmidico
- Sistemi di fermentazione multipli da 7L, senza materiali di origine animale durante tutto il processo
- Tracciabilità chiara dei plasmidi e delle batterie ospiti, senza ostacoli alla dichiarazione
- Resa del plasmide contenente poli A superiore a 500 mg/L
- Tasso di perdita di poli A inferiore a 5 bp
- Proporzione di plasmidi sovraspirale superiore al 90%; tasso di recupero superiore al 55%
- Efficienza di linearizzazione superiore al 99%; tasso di recupero del plasmide linearizzato del 90%
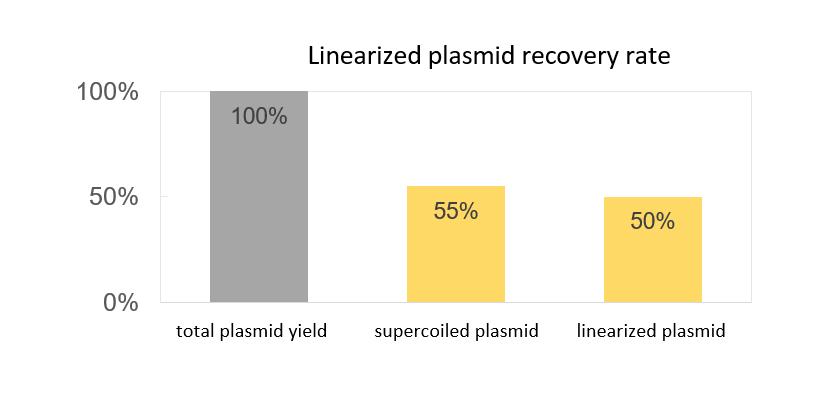
Piattaforma di sostanza farmaceutica mRNA
- Reattori multipli da 1L (GMP)
- Un alto rapporto di trascrizione di 1:120 consente un processo IVT scalabile
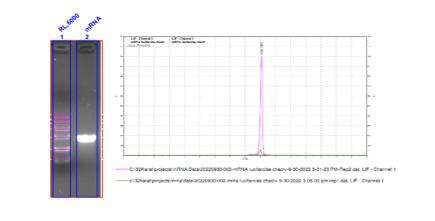
- integrità dell'mRNA superiore al 98%
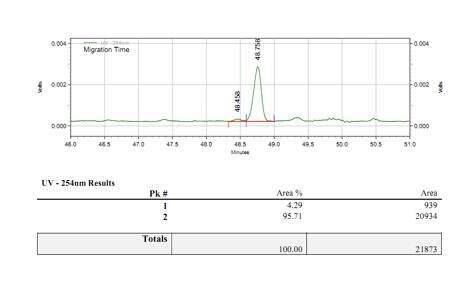
- Processo di cappatura stabile con una frequenza di cappatura superiore al 95%
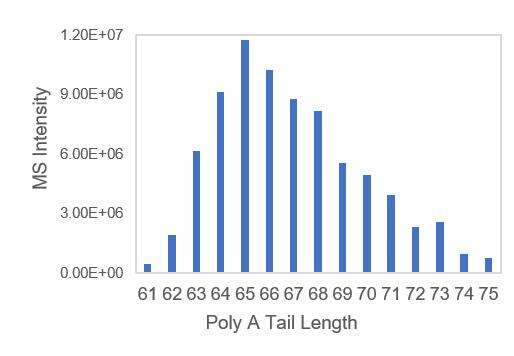
- Modelli di trascrizione con code A, che garantisco una distribuzione uniforme delle code poly A.
Piattaforma di Incapsulamento LNP
- Tecnologia brevettata LNP autorizzata dai nostri partner per garantire l'evitamento di dispute brevettuali per i nostri clienti.



(I nostri partner)
- Impiegando un processo di incapsulazione microfluidica altamente versatile, si raggiunge un'efficienza di incapsulazione superiore al 95%.
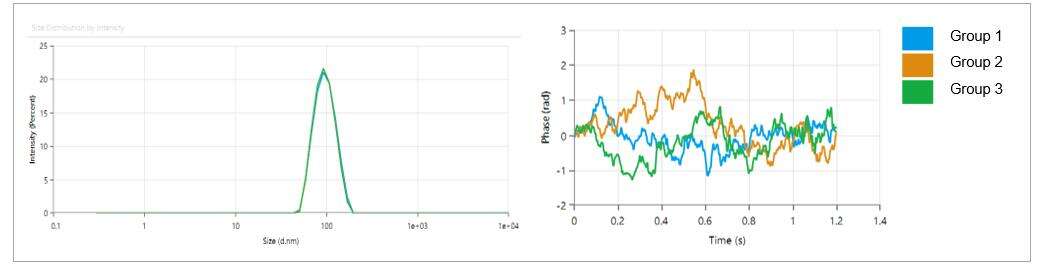
- La dimensione delle particelle LNP è compresa tra 80-100 nm, con un indice di polidispersità (PDI) basso di 0,05, indicativo di una distribuzione uniforme delle dimensioni delle particelle.
- Le particelle LNP presentano una carica debole, con un potenziale Zeta di circa -2,18 mV.
| Voce di prova |
Metodo di prova |
Risultato del test |
| Efficienza di incapsulamento |
Ribogreen |
92.7% |
| Dimensione delle Particelle |
Malvern |
92,07 nm |
| PDI |
Malvern |
0.05 |
| Zeta |
Malvern |
-2,18 mV |
Piattaforma per lo sviluppo dei metodi
Offriamo una piattaforma completa per lo sviluppo dei metodi per l'analisi di plasmidi circolari e linearizzati, materie prime mRNA e prodotti finali LNP-mRNA. La nostra analisi copre una varietà di parametri, come l'integrità, la purezza, l'efficienza di cappatura, la distribuzione di poli A, l'efficienza di incapsulamento, le dimensioni delle particelle, i componenti LNP e vari residui di processo (HCP, HCD, HCR, dsRNA, antibiotici, DNase I, T7 RNA polimerasi, enzima di cappatura della vaccinia, 2-O metiltransferasi, ecc.).
I metodi parziali vengono dimostrati come segue:
Rilevazione dell'integrità dell'mRNA (Elettroforesi Capillare)
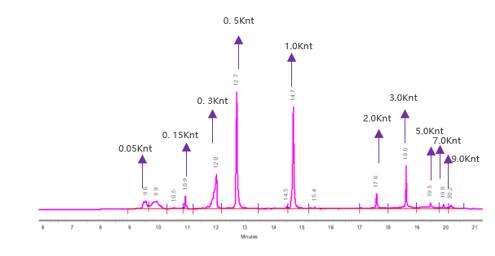
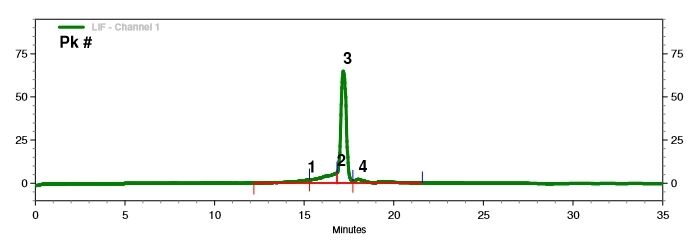
Abbiamo sviluppato condizioni di separazione ottimali per separare con precisione molecole di mRNA di lunghezze variabili.
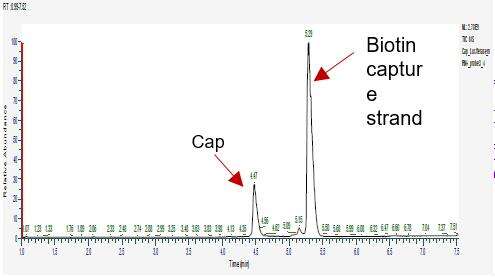
Rilevazione dell'efficienza del cappuccio dell'mRNA (LC-MS)
Abbiamo sviluppato condizioni adatte per il taglio e la separazione degli oligonucleotidi della fine 5', consentendo una separazione precisa dei frammenti cappucciati e non cappucciati.
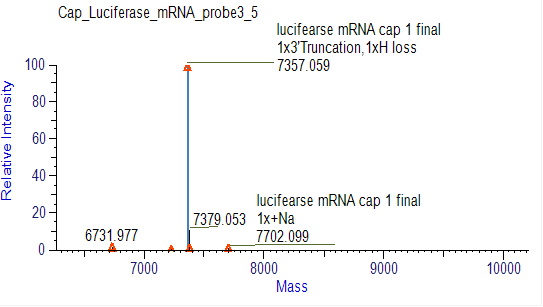
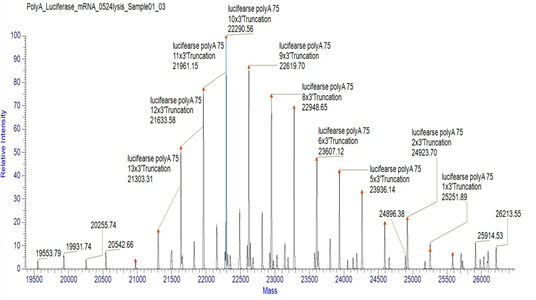
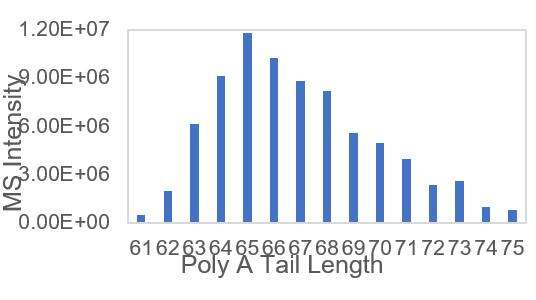
Rilevazione della distribuzione della coda PolyA dell'mRNA adatta (LC-MS)
Abbiamo sviluppato condizioni adatte per il taglio delle estremità 3' e la separazione degli oligonucleotidi terminali 3', che permettono un rilevamento preciso della distribuzione delle code polyA.
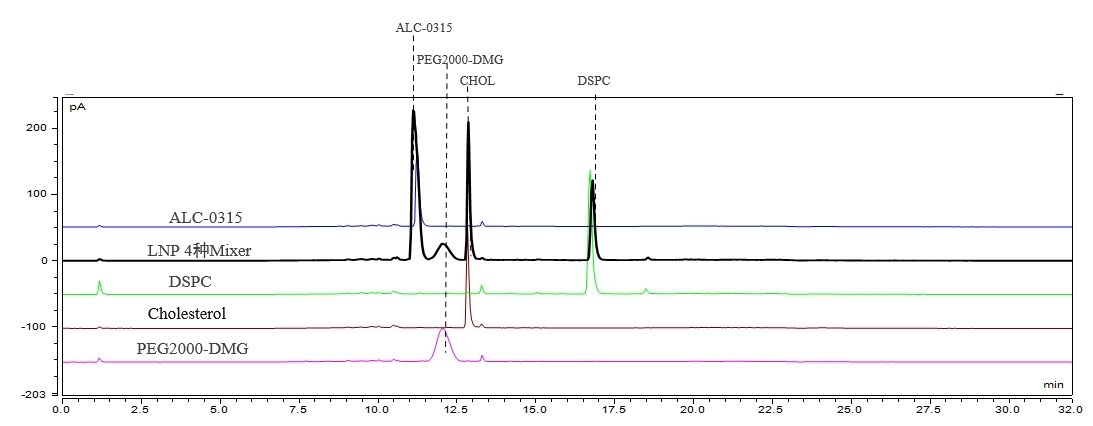
Rilevazione dei componenti e del contenuto dei LNP (HPLC-CAD)
Abbiamo stabilito un metodo cromatografico adeguato che consente una separazione a livello di base di quattro componenti dei LNP. Questo metodo dimostra una riproducibilità eccellente.
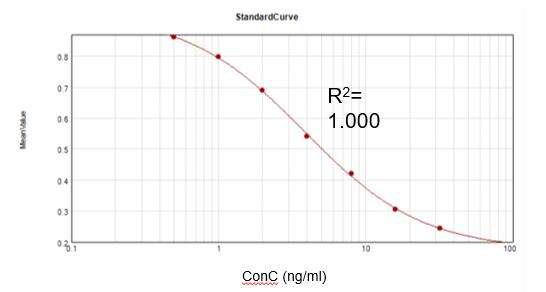
Concentrazione residua di Kanamicina (ELISA)
Basandoci su un kit diagnostico commerciale, abbiamo ottenuto una curva di calibrazione adeguata (R2 = 1,000) e raggiunto un tasso di recupero del 104,8%.
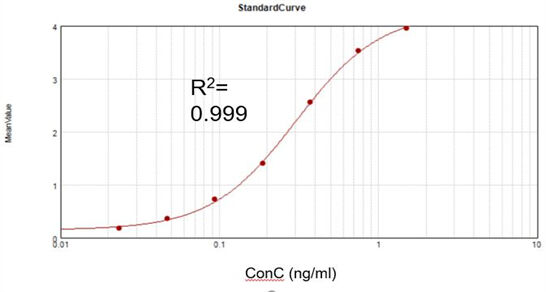
Concentrazione residua di dsRNA
Basandoci su un kit diagnostico commerciale, abbiamo ottenuto una curva di calibrazione adeguata (R2 = 0,999) e raggiunto un tasso di recupero del 105,5%.
Polimerasi RNA T7 Residua (Elisa)
Basandoci su un kit diagnostico commerciale, abbiamo ottenuto una curva di calibrazione adeguata (R2 = 1,000) e raggiunto un tasso di recupero del 107,9%.
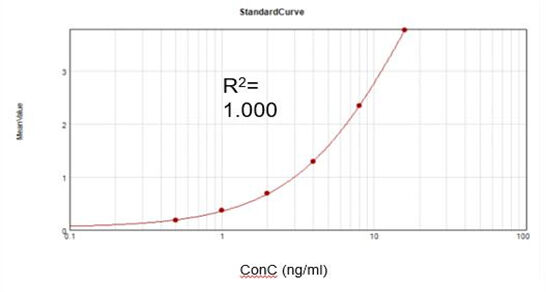
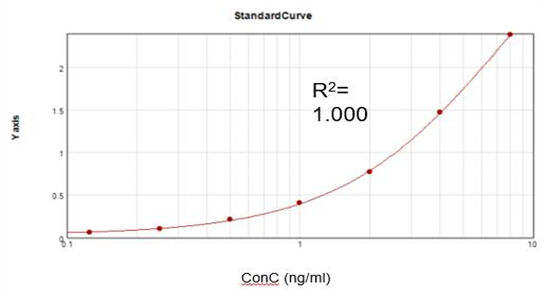
Enzima di Cappatura del Vaiolo Residuo (ELISA)
Basandoci su un kit diagnostico commerciale, abbiamo ottenuto una curva di calibrazione adeguata (R2 = 1,000) e raggiunto un tasso di recupero del 92%.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN






















