เนื่องจากมีการนำวัคซีน mRNA สำหรับป้องกันโควิด-19 ไปใช้อย่างแพร่หลายในประชากรจำนวนมาก ความปลอดภัยของวัคซีน mRNA จึงได้รับการตรวจสอบแล้ว mRNA มีความสามารถในการแสดงโปรตีนใดๆ ก็ได้ โดยนำเสนอวิธีแก้ปัญหาที่เป็นไปได้สำหรับความต้องการทางคลินิกต่างๆ ที่ยังไม่ได้รับการตอบสนอง
Yaohai Bio-Pharma นำเสนอโซลูชันที่ครอบคลุมสำหรับการผลิต mRNA R&D และ GMP ซึ่งได้รับการสนับสนุนโดยแพลตฟอร์มการวิจัยที่แข็งแกร่งและระบบ GMP ที่เป็นไปตามข้อกำหนด บริการของเราได้รับการออกแบบมาเพื่อตอบสนองความต้องการเฉพาะของลูกค้าของเรา โดยนำเสนอสารตัวยา mRNA คุณภาพสูงและผลิตภัณฑ์สำเร็จรูป LNP-mRNA ในปริมาณตั้งแต่มิลลิกรัมถึงกรัม ตลอดจนรายงานการพัฒนาและการผลิตโดยละเอียด และรายงานการทดสอบ
เราได้รับอนุญาตสำหรับเทคโนโลยีสิทธิบัตร LNP จากพันธมิตรของเรา NanoStar Pharmaceuticals เพื่อให้มั่นใจว่าจะหลีกเลี่ยงข้อพิพาทด้านสิทธิบัตรที่อาจเกิดขึ้นได้ในอนาคต
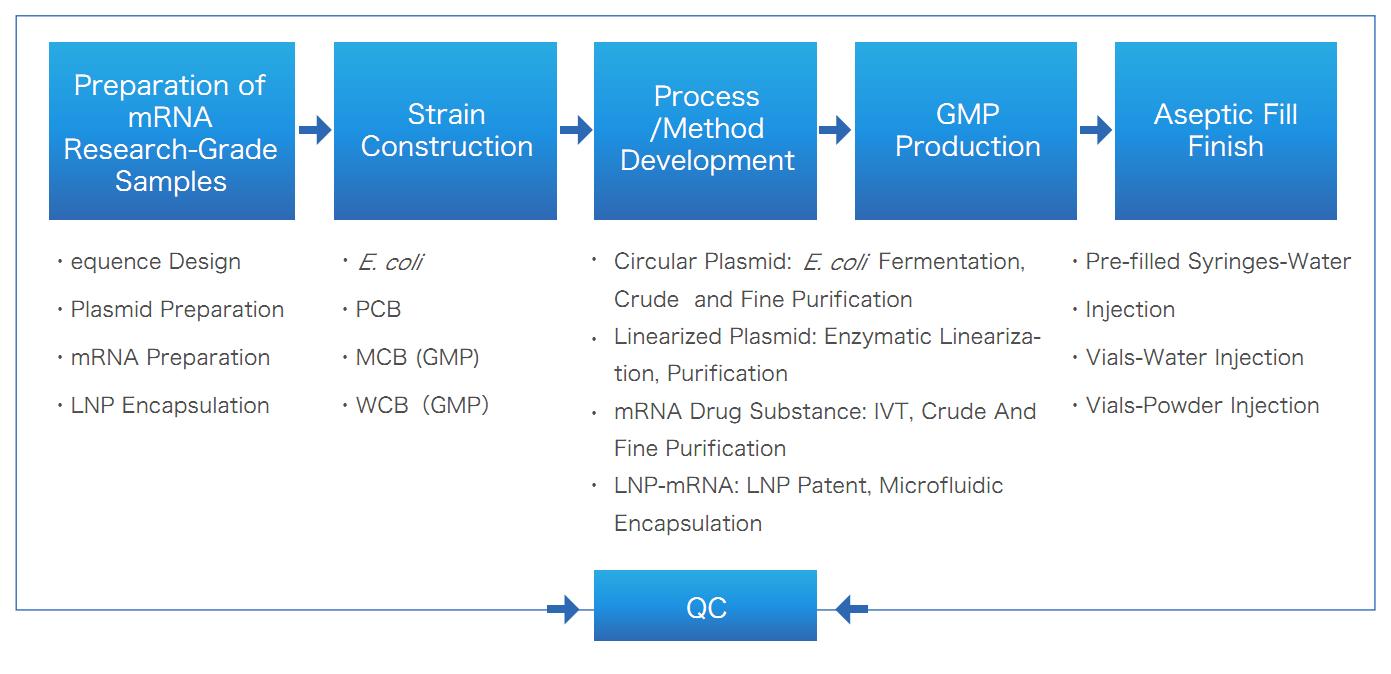
mRNA/LNP โซลูชั่นครบวงจรของ Yaohai Bio-Pharma
การส่งมอบ
| เกรด |
การส่งมอบ |
Specification |
การใช้งาน |
| ไม่ใช่ GMP |
สารยา mRNA |
0.1~10 มก. (mRNA) |
การวิจัยพรีคลินิก เช่น การถ่ายเซลล์ การพัฒนาวิธีการวิเคราะห์ การศึกษาความคงตัวเบื้องต้น การพัฒนาสูตรผสม |
| ผลิตภัณฑ์ยา LNP-mRNA |
| GMP, ความเป็นหมัน |
สารยา mRNA |
10 มก.~70 ก |
ยาใหม่ที่ใช้ในการวิจัย (IND), การอนุมัติการทดลองทางคลินิก (CTA), การจัดหาการทดลองทางคลินิก, การขอใบอนุญาตทางชีวภาพ (BLA), การจัดหาเชิงพาณิชย์ |
| ผลิตภัณฑ์ยา LNP-mRNA |
5000 ขวดหรือหลอดฉีดยา/ตลับบรรจุยาที่บรรจุไว้ล่วงหน้า |
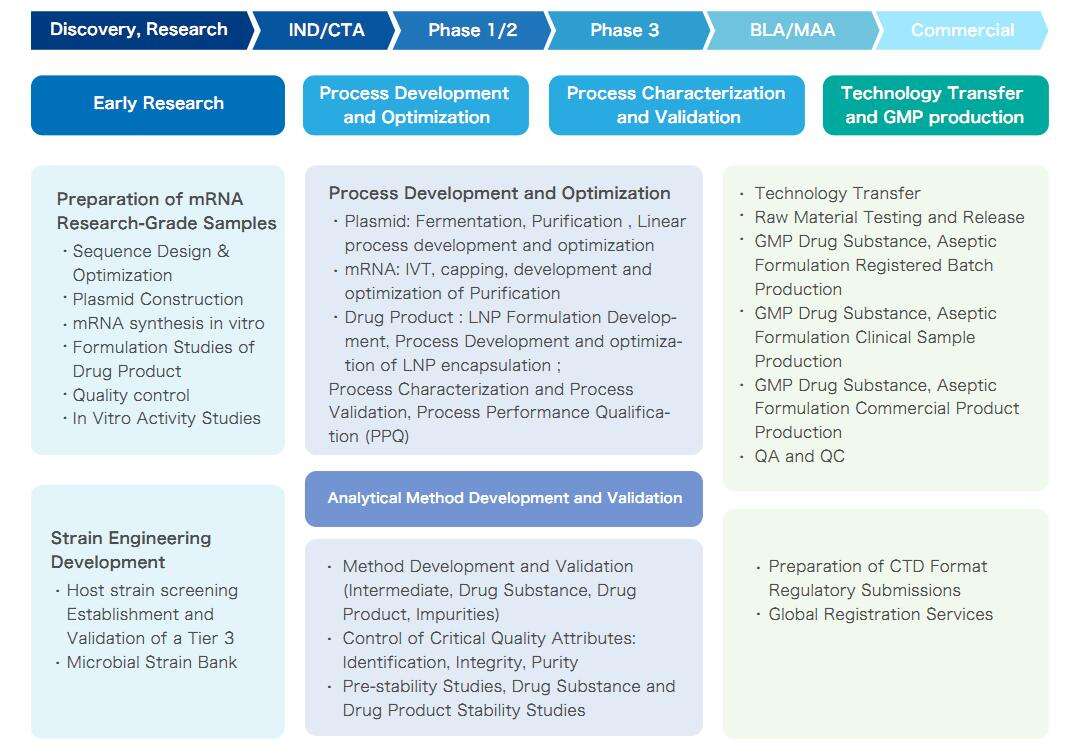
บริการ mRNA CRDMO ของ Yaohai ครอบคลุมวงจรชีวิตของ mRNA ทั้งหมด
คุณสมบัติของแพลตฟอร์ม
แพลตฟอร์มดีเอ็นเอพลาสมิด
- ระบบหมัก 7 ลิตรหลายระบบ ไร้สัตว์ตลอดกระบวนการ
- ตรวจสอบย้อนกลับของพลาสมิดและแบคทีเรียโฮสต์ได้อย่างชัดเจน โดยไม่มีอุปสรรคในการประกาศ
- ผลผลิตของพลาสมิดที่มีโพลีเอเกิน 500 มก./ลิตร
- อัตราการสูญเสียโพลีเอน้อยกว่า 5 bp
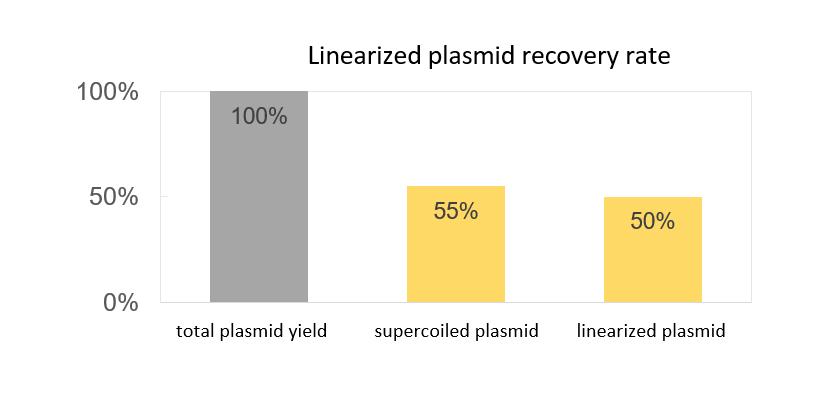
- สัดส่วนพลาสมิด Supercoiled มากกว่า 90%; อัตราการฟื้นตัวมากกว่า 55%
- ประสิทธิภาพเชิงเส้นเกิน 99%; อัตราการฟื้นตัวของพลาสมิดเชิงเส้นตรง 90%
แพลตฟอร์มสารยาของ mRNA
- เครื่องปฏิกรณ์ขนาด 1 ลิตรหลายเครื่อง (GMP)
- อัตราส่วนการถอดรหัสสูง 1: 120 ช่วยให้สามารถปรับขนาดกระบวนการ IVT ได้
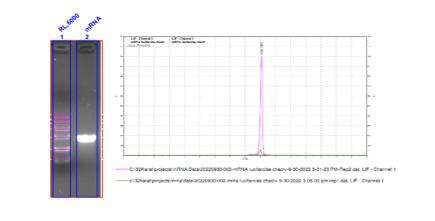
- ความสมบูรณ์ของ mRNA เกิน 98%
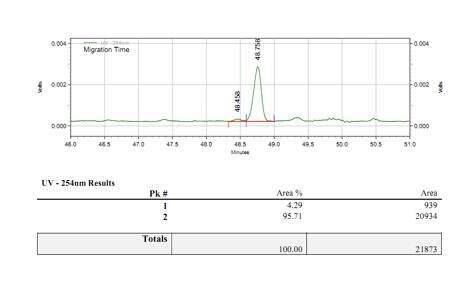
- กระบวนการปิดฝาที่เสถียรด้วยอัตราปิดสูงสุดมากกว่า 95%
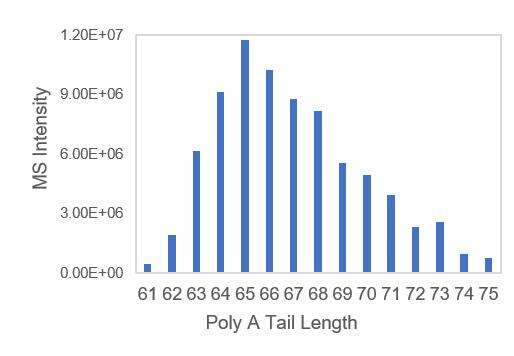
- เทมเพลตการถอดเสียงที่มี A-tails ช่วยให้มั่นใจได้ถึงการกระจายของ poly A tails ที่สม่ำเสมอ
แพลตฟอร์มการห่อหุ้ม LNP
- เทคโนโลยีสิทธิบัตร LNP ที่ได้รับอนุญาตจากพันธมิตรของเราเพื่อหลีกเลี่ยงข้อพิพาทด้านสิทธิบัตรสำหรับลูกค้าของเรา



(พันธมิตรของเรา)
- ใช้กระบวนการห่อหุ้มไมโครฟลูอิดิกที่มีความอเนกประสงค์สูง ทำให้ได้รับประสิทธิภาพการห่อหุ้มมากกว่า 95%
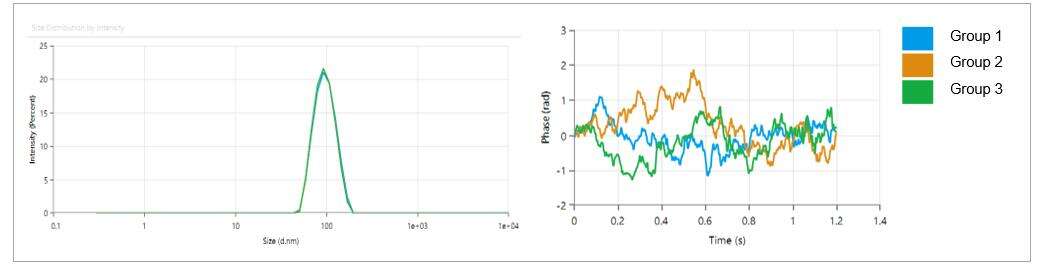
- ขนาดอนุภาค LNP อยู่ในช่วง 80-100 นาโนเมตร โดยมีดัชนีการกระจายตัว (PDI) ต่ำที่ 0.05 ซึ่งบ่งชี้ถึงการกระจายขนาดอนุภาคที่สม่ำเสมอ
- อนุภาค LNP มีประจุอ่อน โดยมีศักย์ซีตาประมาณ -2.18 mV
| รายการทดสอบ |
วิธีทดสอบ |
ผลการทดสอบ |
| ประสิทธิภาพการห่อหุ้ม |
ริโบกรีน |
92.7%
|
| ขนาดอนุภาค |
เวิร์น |
นาโนเมตร 92.07 |
| PDI |
เวิร์น |
0.05 |
| ซีตา |
เวิร์น |
-2.18 มิลลิโวลต์ |
แพลตฟอร์มการพัฒนาวิธีการ
เรานำเสนอแพลตฟอร์มการพัฒนาวิธีการที่ครอบคลุมสำหรับการวิเคราะห์พลาสมิดแบบวงกลมและเชิงเส้นตรง วัตถุดิบ mRNA และผลิตภัณฑ์ LNP-mRNA สำเร็จรูป การวิเคราะห์ของเราครอบคลุมพารามิเตอร์ที่หลากหลาย เช่น ความสมบูรณ์ ความบริสุทธิ์ ประสิทธิภาพการจำกัด การกระจายโพลี A ประสิทธิภาพการห่อหุ้ม ขนาดอนุภาค ส่วนประกอบ LNP และกระบวนการตกค้างต่างๆ (HCP, HCD, HCR, dsRNA, สารปฏิชีวนะ, DNase I, T7 RNA โพลีเมอเรส, เอนไซม์ปิดฝาวัคซีน, 2-O เมทิลทรานสเฟอเรส ฯลฯ)
วิธีการบางส่วนจะแสดงดังต่อไปนี้:
การตรวจจับความสมบูรณ์ของ mRNA (Capillary Electrophoresis)
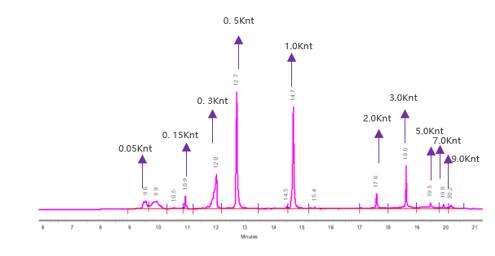
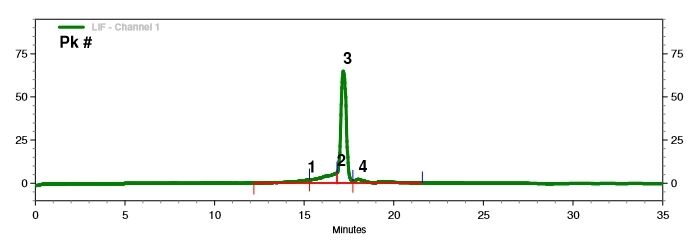
เราได้พัฒนาเงื่อนไขการแยกที่เหมาะสมที่สุดเพื่อแยกโมเลกุล mRNA ที่มีความยาวต่างกันได้อย่างแม่นยำ
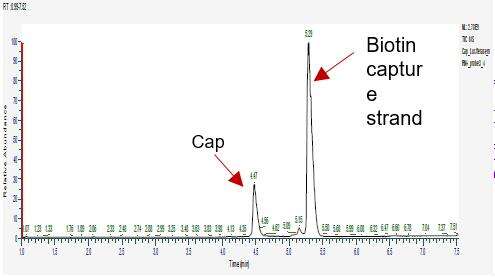
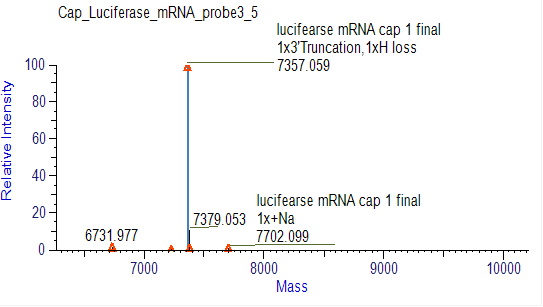
การตรวจจับประสิทธิภาพการกำหนด mRNA (LC-MS)
เราได้พัฒนาสภาวะที่เหมาะสมสำหรับการแยกชิ้นส่วนที่ปลาย 5' และการแยกโอลิโกนิวคลีโอไทด์ที่ปลาย 5' เพื่อให้สามารถแยกชิ้นส่วนที่มีฝาปิดและไม่มีฝาปิดได้อย่างแม่นยำ
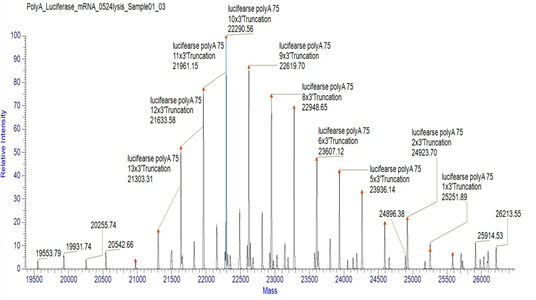
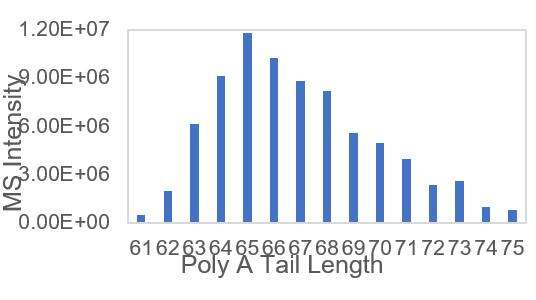
การตรวจจับการกระจายส่วนหางที่เหมาะสมของ mRNA PolyA (LC-MS)
เราได้พัฒนาสภาวะที่เหมาะสมสำหรับการแตกแยกของปลาย 3' และการแยกโอลิโกนิวคลีโอไทด์ที่ปลาย 3' ซึ่งช่วยให้สามารถตรวจจับการกระจายของส่วนหางของ polyA ได้อย่างแม่นยำ
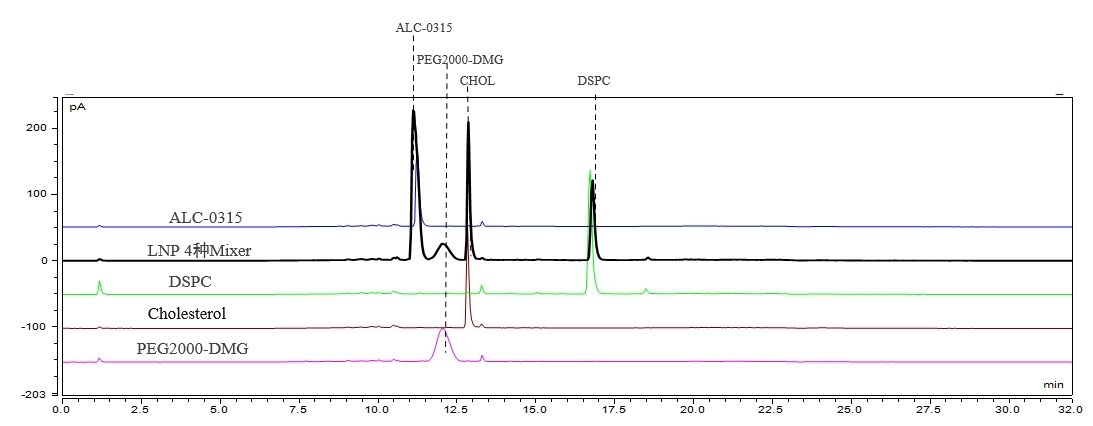
การตรวจจับส่วนประกอบ LNP และเนื้อหา (HPLC-CAD)
เราได้กำหนดวิธีโครมาโตกราฟีที่เหมาะสมเพื่อให้สามารถแยกส่วนประกอบ LNP สี่ชิ้นในระดับพื้นฐานได้ วิธีนี้แสดงให้เห็นถึงความสามารถในการทำซ้ำที่ดีเยี่ยม
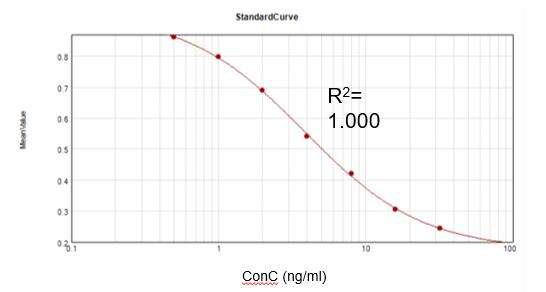
ความเข้มข้นของคานามัยซินที่ตกค้าง (ELISA)
จากชุดทดสอบเชิงพาณิชย์ เราได้รับเส้นโค้งการสอบเทียบที่เหมาะสม (R2 = 1.000) และบรรลุอัตราการฟื้นตัวที่ 104.8%
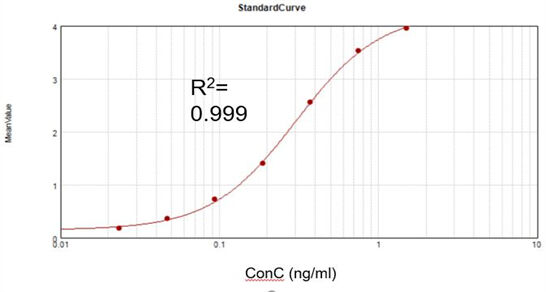
ความเข้มข้นของ dsRNA ที่เหลือ
จากชุดทดสอบเชิงพาณิชย์ เราได้รับกราฟการปรับเทียบที่เหมาะสม (R2 = 0.999) และบรรลุอัตราการฟื้นตัวที่ 105.5%
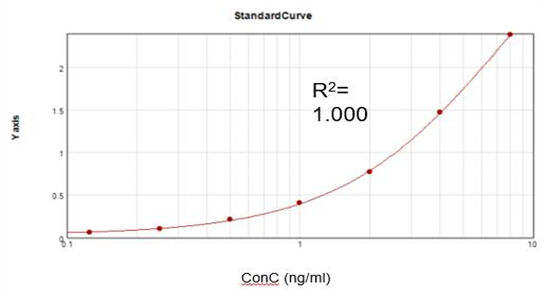
T7 RNA Polymerase ที่ตกค้าง (เอลิซา)
จากชุดทดสอบเชิงพาณิชย์ เราได้รับกราฟการปรับเทียบที่เหมาะสม (R2 = 1.000) และบรรลุอัตราการฟื้นตัวที่ 107.9%
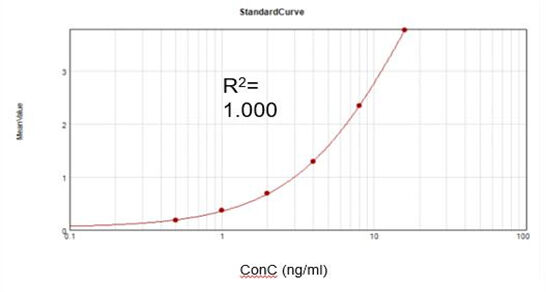
เอนไซม์ปิดฝาไวรัสวัคซีนตกค้าง (ELISA)
จากชุดทดสอบเชิงพาณิชย์ เราได้รับกราฟการปรับเทียบที่เหมาะสม (R2 = 1.000) และบรรลุอัตราการฟื้นตัวที่ 92%

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN






















