ตามแนวทางของ WHO, USP, และ NMPA สำหรับวัคซีน mRNA การควบคุมคุณภาพ (QC) ของเทมเพลต DNA, สารออกฤทธิ์ mRNA (DS) และผลิตภัณฑ์ยา nanoparticle-lipid-mRNA (LNP-mRNA) (DP) ได้รับการแนะนำ
Yaohai Bio-Pharma สามารถให้บริการควบคุมระหว่างกระบวนการและโซลูชันการปล่อยแบทช์สำหรับพลาสมิดวงกลมและเส้นตรง mRNA DS และ LNP-mRNA เสร็จสิ้น เพื่อตอบสนองความต้องการด้านกฎระเบียบ
เราออกแบบการทดสอบ QC สำหรับลักษณะทางกายภาพ การระบุตัว ประสิทธิภาพ ความบริสุทธิ์ และสารปนเปื้อน โดยปฏิบัติตามแนวทางคุณภาพ ICH ฟาร์มาโคเปียที่เกี่ยวข้อง (EU และ US monographs) แนวทางด้านกฎระเบียบ (ICH, FDA และ EMA) และการปฏิบัติตาม GMP/GLP
คำย่อ:
ICH: International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use
FDA: องค์การอาหารและยา
EMA: หน่วยงานยาแห่งยุโรป
GMP: Good Manufacturing Practice
GLP: Good Laboratory Practice
รายละเอียดบริการ
การควบคุมคุณภาพของพลาสมิดเทมเพลต
|
หมวดหมู่
|
คุณสมบัติทางคุณภาพ
|
เทคนิคการวิเคราะห์
|
ระดับการวิจัย
|
อุปทานทางคลินิก
|
|
คุณสมบัติทางกายภาพเคมี
|
ลักษณะที่ปรากฏ วัสดุแปลกปลอมที่มองเห็นได้
|
การมองเห็น
|
√
|
√
|
|
พีเอช
|
ศักย์ไฟฟ้า
|
√
|
√
|
|
คุณสมบัติทางชีวเคมี
|
ความเข้มข้นของ DNA
|
UV/A260
|
√
|
√
|
|
ความเป็นตัวตน
|
การลำดับจีโนมยีนเป้าหมาย
|
การลำดับ
(บุคคลที่สาม)
|
--
|
√
|
|
การย่อยเอนไซม์รีสทริกชัน
|
การแยกไฟฟ้าเจลอะแกโรส (AGE)
|
√
|
√
|
|
สิ่งปนเปื้อนที่เกี่ยวข้องกับผลิตภัณฑ์
|
ความบริสุทธิ์ของพลาสมิดซูเปอร์เฮลิกซ์ หรือ ความบริสุทธิ์ของพลาสมิดเชิงเส้น
|
อายุ
|
√
|
√
|
|
โครมาโทกราฟีของเหลวประสิทธิภาพสูง (HPLC)
|
--
|
√
|
|
การแยกไฟฟ้าแบบแคปิลารี (CE)
|
--
|
√
|
|
สิ่งปนเปื้อนที่เกี่ยวข้องกับกระบวนการ
|
เอนโดท็อกซินที่เหลืออยู่
|
วิธีเจล
|
--
|
√
|
|
วิธีโครโมจีนิก
|
√
|
--
|
|
โปรตีนของเซลล์โฮสต์, HCP
|
การตรวจวิเคราะห์ด้วยภูมิคุ้มกันเชื่อมโยงเอนไซม์ (ELISA)
|
--
|
√
|
|
ดีเอ็นเอของเซลล์โฮสต์ - HCD
|
การตอบสนองเชิงโซนARING ปริมาณ (qPCR) )
|
--
|
√
|
|
อาร์เอ็นเอของโฮสต์
|
การถอดกลับ-การตอบสนองเชิงโซนARING ปริมาณ (RT-qPCR )
|
--
|
√
|
|
แอนติบัยโอติกที่เหลืออยู่
|
ELISA
|
--
|
√
|
|
ไบโอเบิร์เด้น
|
ไบโอเบิร์เด้น
|
การนับจาน, การกรองเยื่อหุ้ม
|
--
|
√
|
|
ความปลอดภัยจากเชื้อโรค
|
การปลูกเชื้อโดยตรง การกรองเยื่อหุ้ม
|
--
|
√
|
|
"√" :R แนะนำ ,"--": ตัวเลือก
|
การควบคุมคุณภาพของ mRNA
|
หมวดหมู่
|
คุณสมบัติทางคุณภาพ
|
เทคนิคการวิเคราะห์
|
ระดับการวิจัย
|
อุปทานทางคลินิก
|
|
คุณสมบัติทางชีวเคมี
|
ความเข้มข้นของ mRNA
|
UV/A260
|
√
|
√
|
|
ความบริสุทธิ์ของ mRNA
|
A 260/280
|
√
|
√
|
|
ความเป็นตัวตน
|
การจัดลำดับ mRNA
|
การลำดับ
(บุคคลที่สาม)
|
--
|
√
|
|
S ความสมบูรณ์ของโครงสร้าง
|
m ความสมบูรณ์ของ RNA
|
C E
|
--
|
√
|
|
การแยกสารด้วยเจลแบบร่องพร้อมเครื่องตรวจวัดความเรืองแสงที่กระตุ้นด้วยเลเซอร์ (C GE-LIF )
|
--
|
√
|
|
A จีอี
|
√
|
√
|
|
m ประสิทธิภาพของการปิดห่วงโซ่ RNA
|
โครมาโทกราฟีแบบของเหลว-สเปกโตรมิเตอร์มวล (LC-MS )หลังการย่อยสลาย
|
--
|
√
|
|
m การกระจายตัวของ RNA polyA
|
LC-MS หลังการย่อยสลาย
|
--
|
√
|
|
สิ่งปนเปื้อนที่เกี่ยวข้องกับผลิตภัณฑ์
|
ก้อนรวม s
|
โครมาโทกราฟีแยกตามขนาดแบบ высокоสมรรถนะ (SEC-HPLC )
|
--
|
√
|
|
ชิ้นส่วน mRNA
|
โครมาโทกราฟีเฟสกลับแบบเหลวความดันสูง (RP-HPLC )
|
--
|
√
|
|
d sRNA
|
E ลิซ่า
|
--
|
√
|
|
สิ่งปนเปื้อนที่เกี่ยวข้องกับกระบวนการ
|
เอนโดท็อกซินที่เหลืออยู่
|
วิธีเจล
|
√
|
√
|
|
โปรตีนของเซลล์โฮสต์, HCP
|
ELISA
|
--
|
√
|
|
ดีเอ็นเอของเซลล์โฮสต์ - HCD
|
qPCR
|
--
|
√
|
|
"√" :R แนะนำ ,"--": ตัวเลือก
|
การควบคุมคุณภาพของ LNP
|
หมวดหมู่
|
คุณสมบัติทางคุณภาพ
|
เทคนิคการวิเคราะห์
|
ระดับการวิจัย
|
อุปทานทางคลินิก
|
|
คุณสมบัติทางชีวเคมี
|
ประสิทธิภาพการห่อหุ้ม
|
Ribogreen
|
√
|
√
|
|
ฉัน ระบุ
|
L เนื้อหาของลิพิด
|
โครมาโทกราฟีของของเหลวความดันสูงพร้อมตัวตรวจจับละอองไฟฟ้าสถิต ( PLC-CAD)
|
--
|
√
|
|
คุณสมบัติทางกายภาพเคมี
|
ลักษณะที่ปรากฏ วัสดุแปลกปลอมที่มองเห็นได้
|
การมองเห็น
|
√
|
√
|
|
อนุภาคที่ไม่ละลาย
|
การบดบังแสง
|
√
|
√
|
|
ไม่ระบุ ไม่ กว้างของอนุภาค
|
การกระจายแสงแบบไดนามิก (DLS )
|
√
|
√
|
|
PDI, ดัชนีความหลากหลายของโพลิเมอร์
|
DLS
|
√
|
√
|
|
ศักย์เซต้า
|
DLS
|
√
|
√
|
|
พีเอช
|
ศักย์ไฟฟ้า
|
√
|
√
|
|
ออสโมลาลิตี้
|
การวัดจุดเยือกแข็ง
|
√
|
√
|
|
ปริมาตรที่สามารถจ่ายได้
|
ตามปริมาตร ตามน้ำหนัก
|
--
|
√
|
|
S ความปลอดภัย
|
เอนโดท็อกซินที่เหลืออยู่
|
วิธีเจล
|
√
|
√
|
|
ความเป็นพิษผิดปกติ
|
หนู豚
|
--
|
√
|
|
"√" :R แนะนำ ,"--": ตัวเลือก
|
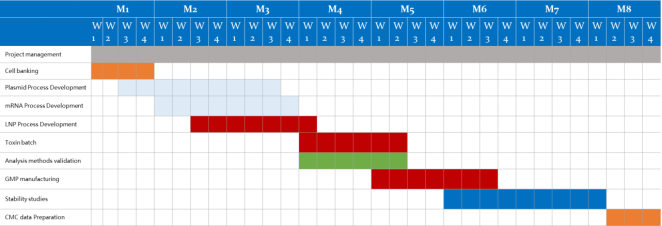
ไทม์ไลน์ของโซลูชัน CDMO mRNA

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN