ด้วยการใช้งานอย่างแพร่หลายของวัคซีน mRNA โควิด-19 ในประชากรจำนวนมาก ความปลอดภัยของวัคซีน mRNA ได้รับการยืนยันแล้ว mRNA มีความสามารถในการแสดงโปรตีนใดๆ ก็ตาม มอบทางออกที่เป็นไปได้สำหรับความต้องการทางคลินิกที่ยังไม่ได้รับการตอบสนองหลากหลายประการ
ยาหǎอไบโอ-ฟาร์มาให้บริการโซลูชันแบบครบวงจรสำหรับการวิจัยและพัฒนา mRNA และการผลิต GMP โดยมีแพลตฟอร์มวิจัยที่แข็งแกร่งและระบบ GMP ที่สอดคล้องกับข้อกำหนด บริการของเราออกแบบมาเพื่อตอบสนองความต้องการเฉพาะของลูกค้าแต่ละราย โดยมอบสารยา mRNA คุณภาพสูงและผลิตภัณฑ์ LNP-mRNA เสร็จสมบูรณ์ในปริมาณตั้งแต่มิลลิกรัมถึงกรัม นอกจากนี้ยังมีรายงานการพัฒนาและการผลิตโดยละเอียด และรายงานการทดสอบ
เราได้รับอนุญาตสำหรับเทคโนโลยีสิทธิบัตร LNP จากหุ้นส่วนของเรา NanoStar Pharmaceuticals เพื่อหลีกเลี่ยงข้อพิพาททางสิทธิบัตรที่อาจเกิดขึ้นในอนาคต
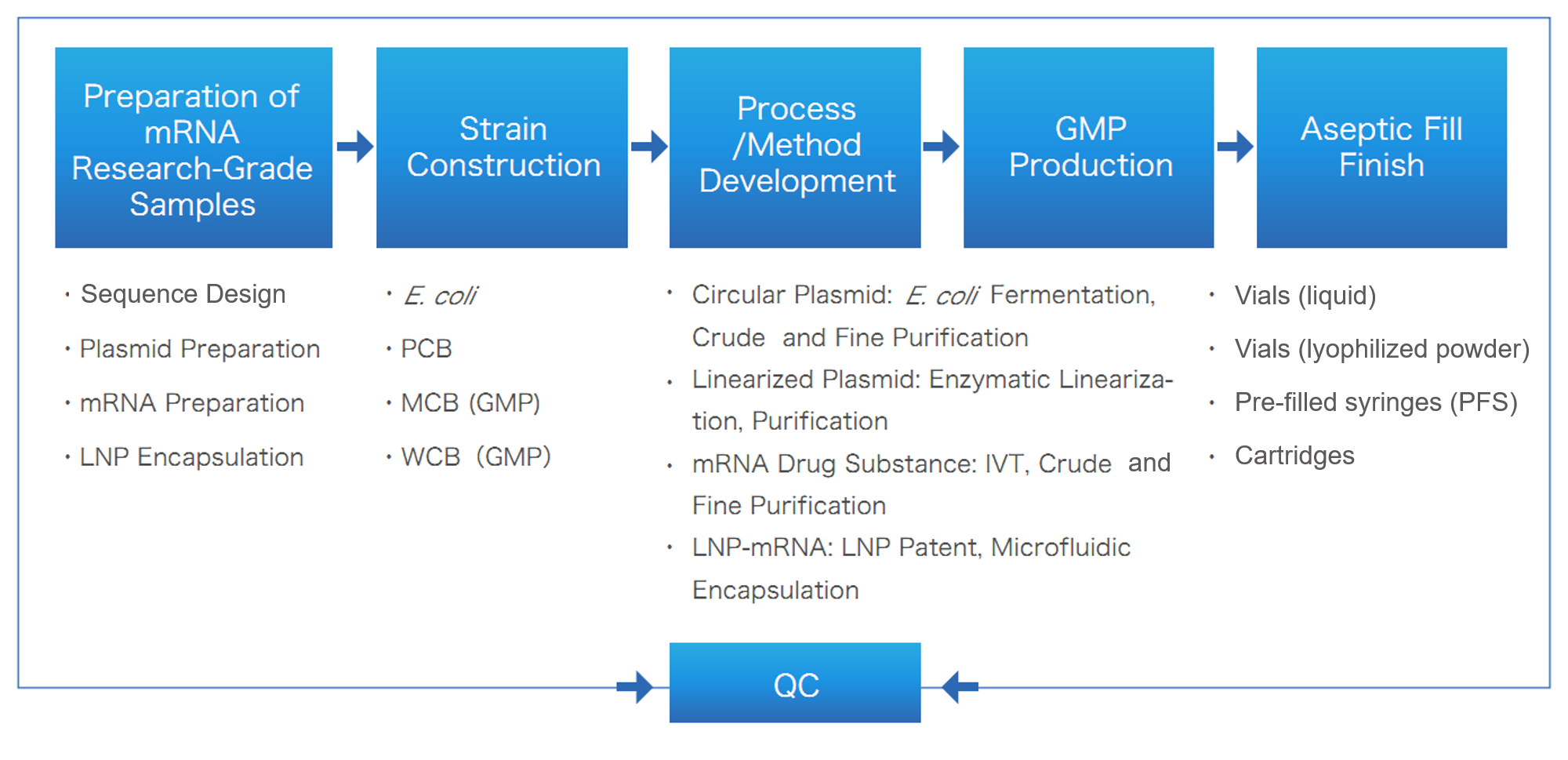
โซลูชันแบบครบวงจร mRNA/LNP ของยาหǎอไบโอ-ฟาร์มา
สิ่งที่จะได้รับ
| เกรด |
สิ่งที่จะได้รับ |
ข้อมูลจำเพาะ |
การประยุกต์ใช้ |
| non-GMP |
สารยา, mRNA |
0.1~10 mg (mRNA) |
การวิจัยก่อนคลินิก เช่น การส่งเซลล์ การพัฒนาวิธีการวิเคราะห์ การศึกษาความเสถียรเบื้องต้น การพัฒนาสูตร |
| ผลิตภัณฑ์ยา, LNP-mRNA |
| GMP, ความปลอดเชื้อ |
สารยา, mRNA |
10 มก.~70 กรัม |
ยาใหม่สำหรับการทดลอง (IND), การอนุมัติการทดลองทางคลินิก (CTA), การจัดหาสำหรับการทดลองทางคลินิก, การขอใบอนุญาตสำหรับชีวภาพ (BLA), การจัดหาเชิงพาณิชย์ |
| ผลิตภัณฑ์ยา, LNP-mRNA |
5000 ขวดหรือเข็มฉีดยา/กระบอกบรรจุล่วงหน้า |
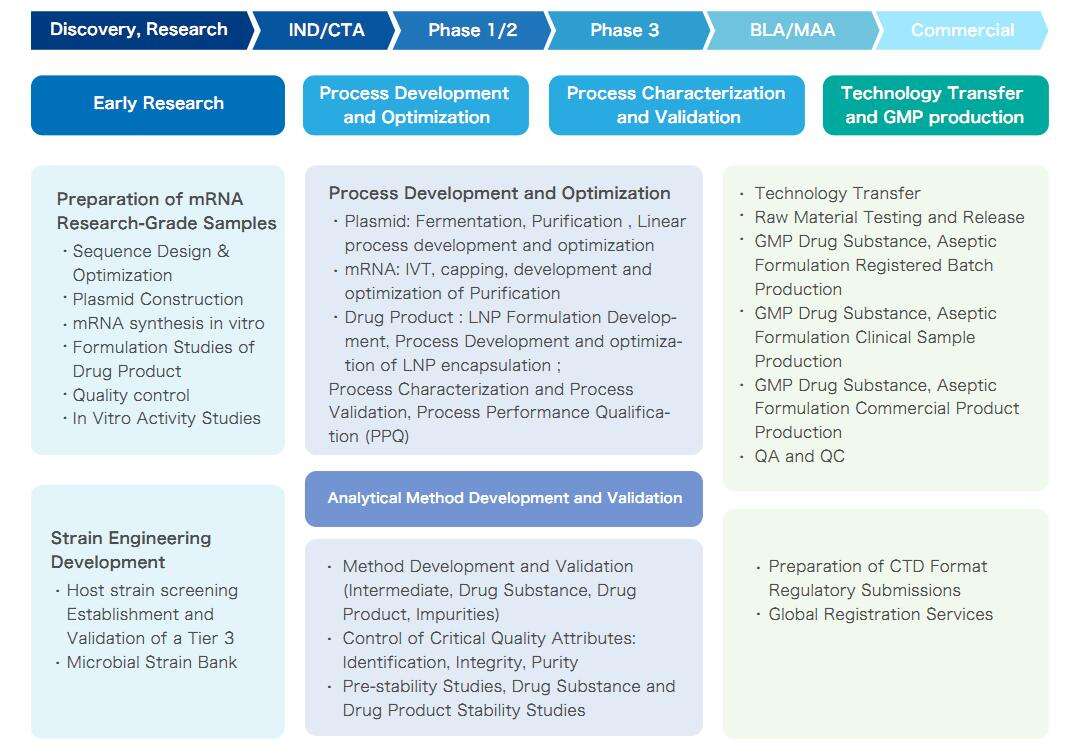
บริการ mRNA CRDMO ของ Yaohai ครอบคลุมวงจรชีวิตทั้งหมดของ mRNA
คุณสมบัติของแพลตฟอร์ม
แพลตฟอร์ม DNA พลาสมิด
- ระบบหมักหลายขนาด 7 ลิตร โดยไม่มีส่วนประกอบจากสัตว์ตลอดกระบวนการ
- สามารถติดตามพลาสมิดและแบคทีเรียโฮสต์ได้อย่างชัดเจน ไม่มีอุปสรรคในการยื่นข้อมูล
- ผลผลิตของพลาสมิดที่มี poly A สูงกว่า 500 มก./ล.
- อัตราการสูญเสีย poly A น้อยกว่า 5 bp
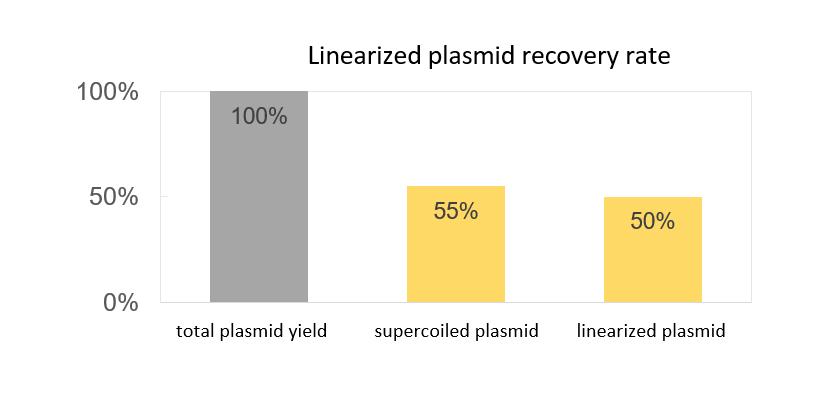
- สัดส่วนพลาสมิดแบบซูเปอร์คอยล์มากกว่า 90% อัตราการกู้คืนเกิน 55%
- ประสิทธิภาพของการทำให้เป็นเส้นตรงเกิน 99% อัตราการกู้คืนพลาสมิดที่ถูกทำให้เป็นเส้นตรงอยู่ที่ 90%
แพลตฟอร์มสารออกฤทธิ์ทางเภสัชกรรมของ mRNA
- เครื่องปฏิกรณ์ขนาด 1 ลิตรหลายตัว (GMP)
- อัตราการถอดรหัสสูงถึง 1:120 ช่วยให้กระบวนการ IVT สามารถปรับขนาดได้
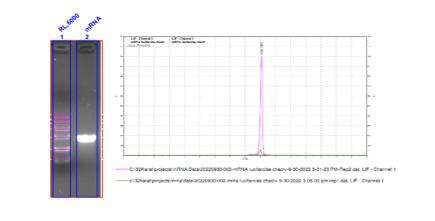
- ความสมบูรณ์ของ mRNA สูงกว่า 98%
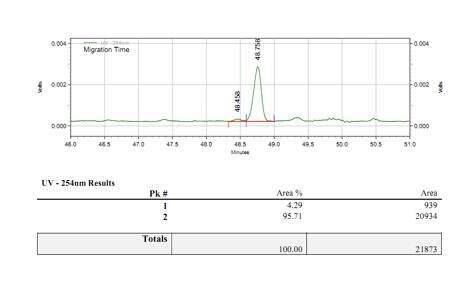
- กระบวนการปิดห่วงโซ่ที่มั่นคงด้วยอัตราการปิดห่วงโซ่มากกว่า 95%
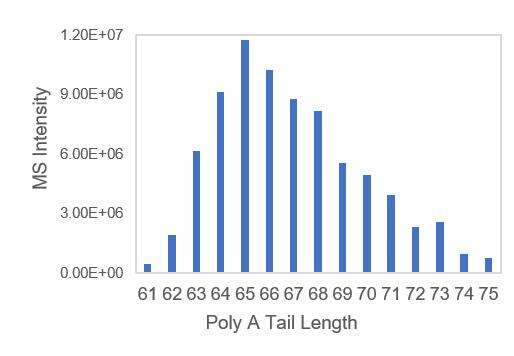
- แม่พิมพ์การถอดรหัสที่มี A-tails รับรองการกระจายตัวของ poly A tails อย่างสม่ำเสมอ
แพลตฟอร์มการห่อหุ้ม LNP
- เทคโนโลยีสิทธิบัตร LNP ที่ได้รับอนุญาตจากพันธมิตรของเราเพื่อรับประกันการหลีกเลี่ยงข้อพิพาทด้านสิทธิบัตรสำหรับลูกค้าของเรา



(พันธมิตรของเรา)
- ใช้กระบวนการห่อหุ้มแบบไมโครฟลูอิดิกที่มีความหลากหลายสูง บรรลุประสิทธิภาพการห่อหุ้มมากกว่า 95%
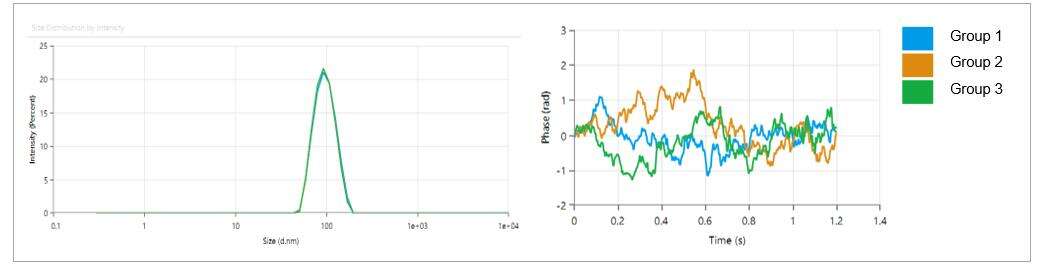
- ขนาดอนุภาค LNP อยู่ในช่วง 80-100 นาโนเมตร พร้อมดัชนีการกระจายตัวต่ำ (PDI) ที่ 0.05 แสดงถึงการกระจายตัวของขนาดอนุภาคที่สม่ำเสมอ
- อนุภาค LNP มีประจุอ่อน โดยมีศักย์ Zeta ประมาณ -2.18 mV
| รายการทดสอบ |
วิธีการทดสอบ |
ผลการทดสอบ |
| ประสิทธิภาพการห่อหุ้ม |
Ribogreen |
92.7% |
| ขนาดอนุภาค |
Malvern |
92.07 นาโนเมตร |
| PDI |
Malvern |
0.05 |
| Zeta |
Malvern |
-2.18 มิลลิโวลต์ |
แพลตฟอร์มพัฒนาวิธีการ
เราให้บริการแพลตฟอร์มพัฒนาวิธีการที่ครอบคลุมสำหรับการวิเคราะห์พลาสมิดวงกลมและพลาสมิดเชิงเส้น อาร์เอ็มเอ็นเอดิบเบอร์ และผลิตภัณฑ์ LNP-mRNA ที่เสร็จแล้ว การวิเคราะห์ของเราครอบคลุมพารามิเตอร์หลากหลาย เช่น ความสมบูรณ์ ความบริสุทธิ์ ประสิทธิภาพการปิดห่วง การกระจายของ poly A ประสิทธิภาพการห่อหุ้ม ขนาดอนุภาค องค์ประกอบของ LNP และสารตกค้างจากกระบวนการต่าง ๆ (HCP, HCD, HCR, dsRNA, แอนติบัยโอติก, DNase I, T7 RNA polymerase, vaccinia capping enzyme, 2-O methyltransferase เป็นต้น)
ตัวอย่างของวิธีการบางส่วนแสดงดังนี้:
การตรวจจับความสมบูรณ์ของ mRNA (การอิเล็กโทรโฟรีซิสในท่อแคปิลารี)
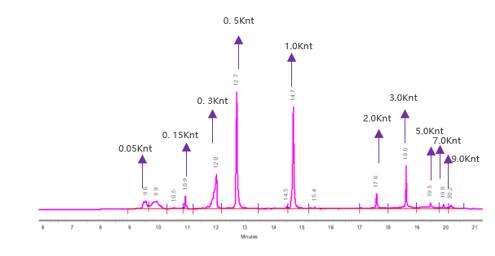
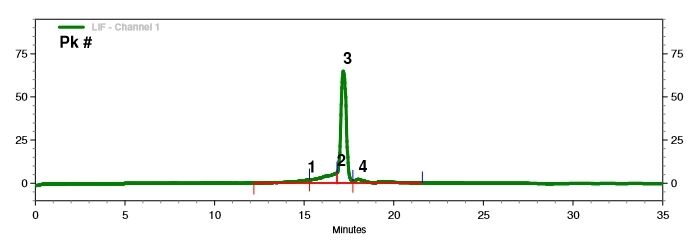
เราได้พัฒนาเงื่อนไขการแยกที่เหมาะสมที่สุดเพื่อแยกโมเลกุล mRNA ที่มีความยาวแตกต่างกันอย่างแม่นยำ
การตรวจจับประสิทธิภาพการ戴上หมวกของ mRNA (LC-MS)
เราได้พัฒนาเงื่อนไขที่เหมาะสมสำหรับการตัดและแยก oligonucleotides ปลาย 5' ซึ่งช่วยให้แยกชิ้นส่วนที่戴上หมวกและไม่ได้戴上หมวกได้อย่างถูกต้อง
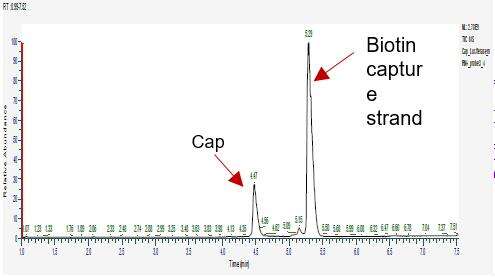
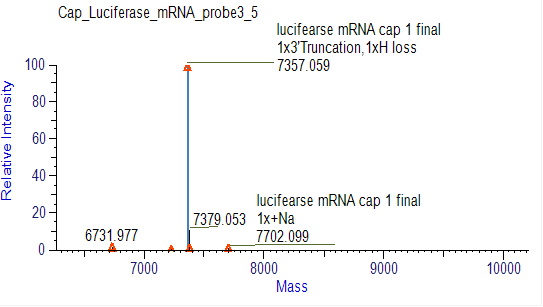
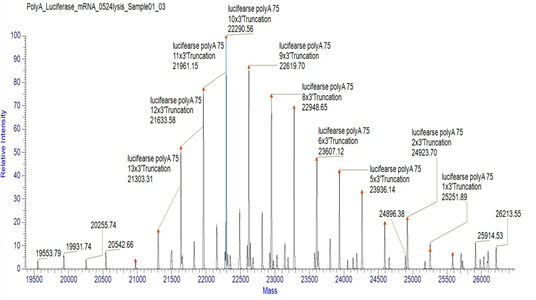
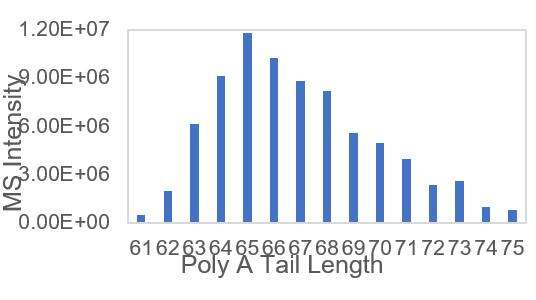
การตรวจจับการกระจายหาง PolyA ของ mRNA (LC-MS)
เราได้พัฒนาเงื่อนไขที่เหมาะสมสำหรับการตัดปลาย 3' และการแยก oligonucleotides ปลาย 3' ซึ่งช่วยให้ตรวจจับการกระจายของหาง polyA ได้อย่างแม่นยำ
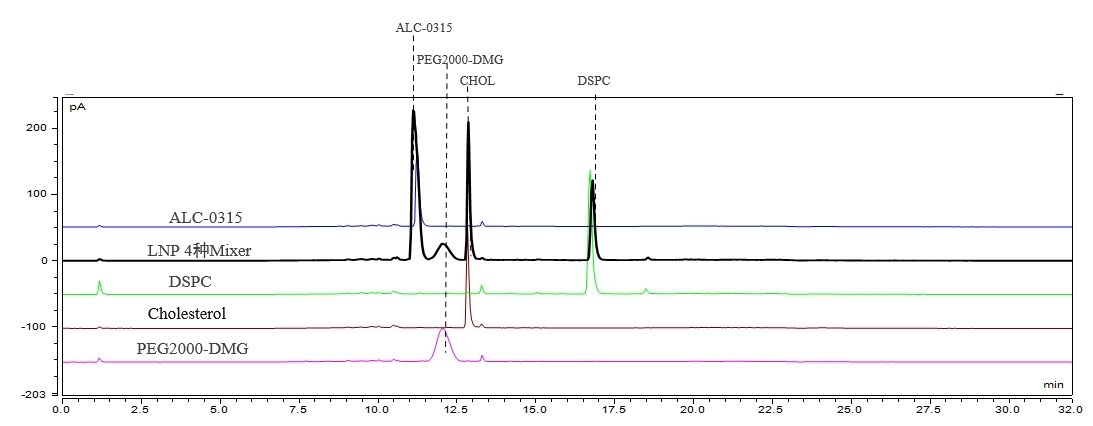
การตรวจจับองค์ประกอบและเนื้อหาของ LNP (HPLC-CAD)
เราได้สร้างวิธีโครมาโทกราฟีที่เหมาะสมซึ่งสามารถแยกองค์ประกอบของ LNP สี่ชนิดได้ตามระดับฐาน และวิธีนี้แสดงถึงความสามารถในการทำซ้ำที่ยอดเยี่ยม
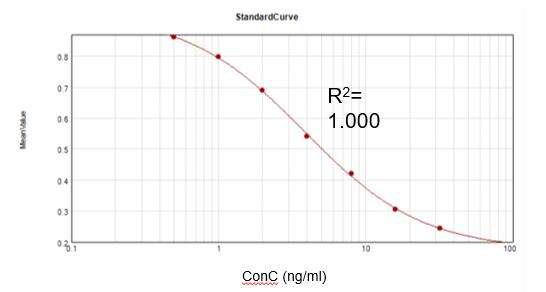
ความเข้มข้นของ Kanamycin ที่เหลืออยู่ (ELISA)
จากชุดทดสอบเชิงพาณิชย์ เราได้รับเส้นโค้งการ较บราที่เหมาะสม (R2 = 1.000) และบรรลุอัตราการกู้คืนที่ 104.8%
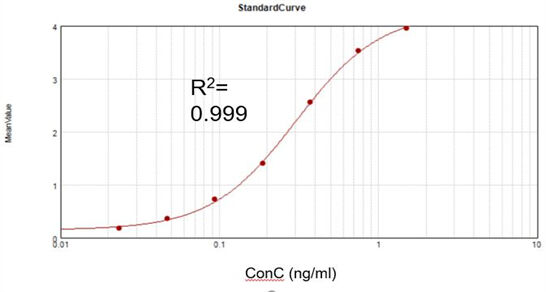
ความเข้มข้นของ dsRNA เหลืออยู่
จากชุดทดสอบเชิงพาณิชย์ เราได้รับเส้นโค้งการ较บราที่เหมาะสมและสมดุล (R2 = 0.999) และบรรลุอัตราการกู้คืนที่ 105.5%
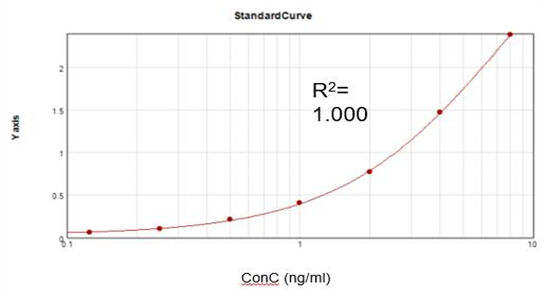
T7 RNA Polymerase เหลืออยู่ (Elisa)
จากชุดทดสอบเชิงพาณิชย์ เราได้รับเส้นโค้งการ较บราที่เหมาะสมและสมดุล (R2 = 1.000) และบรรลุอัตราการกู้คืนที่ 107.9%
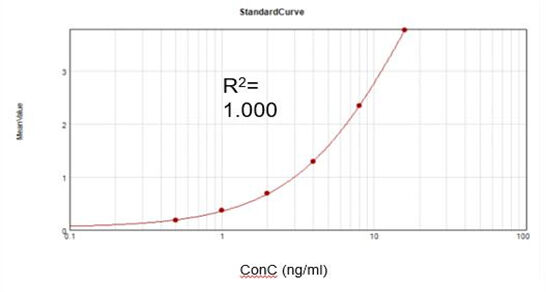
เอนไซม์ปิดห่วงโซ่ของไวรัส Vaccinia เหลืออยู่ (ELISA)
จากชุดทดสอบเชิงพาณิชย์ เราได้รับเส้นโค้งการ较บราที่เหมาะสมและสมดุล (R2 = 1.000) และบรรลุอัตราการกู้คืนที่ 92%

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN






















