Les fragments d'anticorps sont utilisés comme substituts des anticorps monoclonaux conventionnels (mAbs) dans les applications diagnostiques et thérapeutiques, parmi lesquels les scFvs sont l'un des types les plus populaires. Les scFvs peuvent être produits dans divers systèmes d'expression et modifiés en de nombreux formats d'Ab différents. Comme ils peuvent être exprimés chez les bactéries (par exemple, Escherichia Coli ), les scFvs sont plus petits et donc plus faciles et moins coûteux à fabriquer, tandis que les mAbs nécessitent généralement un système d'expression mammifère. De plus, la taille des scFvs offre encore des avantages en recherche clinique, y compris une immunogénicité réduite lorsqu'ils sont administrés in vivo en raison de l'absence d'une région Fc ; une meilleure pénétration tissulaire, ce qui est utile pour les applications thérapeutiques et d'imagerie ; et une élimination rapide du sang, ce qui est utile pour les applications d'imagerie.
Les sites de liaison complets aux antigènes sont inclus dans les scFvs, tels que les domaines variables lourds (VH) et légers (VL) d'un anticorps. Grâce à l'introduction d'un peptide linker flexible (par exemple, (GGGGS)3), le domaine structural VH est lié au domaine structural VL. Des fragments monovalents alternatifs aux scFv incluent les dsFv qui constituent des chaînes VH et VL connectées par des liaisons disulfure insérées dans la région cadre. Les dsFvs présentent un degré plus élevé de stabilité et ne s'agrègent pas, contrairement aux scFvs.
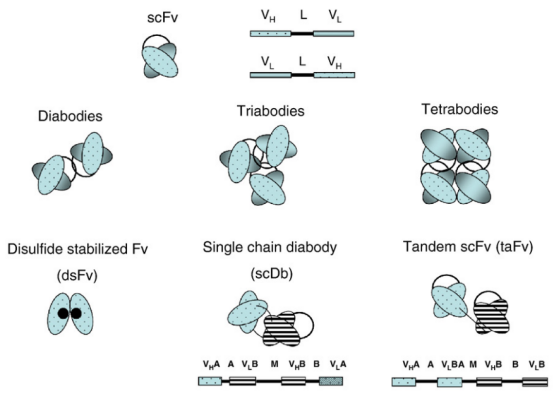
Fig 1 . Structure du scFv et dérivés
fragment scFv pour utilisation thérapeutique
Après des années de découverte et d'ingénierie, les fragments scFv et basés sur scFv sont apparus comme des alternatives thérapeutiques et diagnostiques viables aux AcM contre le cancer, les maladies auto-immunes, l'inflammation, les maladies virales chroniques, etc. Plusieurs fragments scFv ont été approuvés pour une utilisation thérapeutique, tels que Blinatumomab (Blincyto), Moxetumomab pasudotox (Lumoxiti), Brolucizumab (Beovu) et Tebentafusp (Kimmtrak).
Moxetumomab pasudotox
Moxetumomab pasudotox (Lumoxiti) est un cytotoxine ciblant le CD22. Il est constitué d'un domaine variable d'immunoglobuline murine recombinante fusionné à une exotoxine tronquée de Pseudomonas, PE38, qui inhibe la synthèse des protéines. Moxetumomab pasudotox a un poids moléculaire d'environ 63 kDa et est produit par technologie d'ADN recombinant en E. coli . Il a été développé par Medimmune (branche R&D d'AstraZeneca) et approuvé pour traiter les adultes atteints de leucémie à cellules cheveux récidivante ou réfractaire (HCL).
Brolucizumab
Brolucizumab a été développé par Novartis pour traiter les patients souffrant de dégénérescence maculaire liée à l'âge exsudative (humide) (DMLA), d'œdème maculaire diabétique et d'œdème maculaire secondaire à une occlusion de la veine rétinienne. Brolucizumab est un E. coli -produit fragment d'anticorps humanisé scFv qui cible le facteur de croissance endothéliale vasculaire humain (VEGF) avec un poids moléculaire d'environ 26 kDa.
Tebentafusp (Kimmtrak)
En tant que récepteur bispécifique de la protéine gp100 peptide-HLA dirigé vers les cellules T CD3, le Tebentafusp (Kimmtrak) est indiqué pour traiter les patients adultes HLA-A*02:01-positifs atteints d'un mélanome de l'uvée irréductible ou métastatique. Le Tebentafusp a été développé par Immunocore et produit en E. coli cellules avec un poids moléculaire de 77 kDa.
Yaohai Bio-Pharma Propose une Solution CDMO Complète pour les Fragments d'Anticorps
pipelines de Fragments scFv
|
Nom Générique
|
Nom de Marque / Nom Alternatif
|
Cible
|
Système d'Expression
|
Indications
|
Fabricant
|
Étape de R&D
|
|
Blinatumomab
|
BiTE-MT-103, bscCD19xCD3, AMG-103, MEDI-538, ビーリンサイト, Blincyto, 倍利妥
|
CD19, CD3
|
Cellule CHO
|
Leucémie lymphoblastique aiguë (LLA), lymphome
|
Amgen, BeiGene
|
Approbation
|
|
Brolucizumab-dbll
|
AL-86810, XSZ53G39H5 (code UNII), RTH-258, ESBA-1008, DLX-1008, Beovu, ベオビュ
|
VEGF-A
|
Escherichia coli (E. coli)
|
Dégénérescence maculaire
|
Novartis
|
Approbation
|
|
Moxetumomab pasudotox
|
Lumoxiti, scFv-PE38
|
CD22
|
E. coli
|
Leucémie à cellules chevelues
|
AstraZeneca, Innate
|
Approbation
|
|
Tebentafusp
|
Kimmtrak, CD3, gp100
|
CD3, gp100
|
E. coli
|
Mélanome de l'uvée non résectable ou métastatique
|
Immunocore
|
Approbation
|
|
Licaminlimab
|
ESBA-1622, LME-636, OCS 02, ESBA 1622
|
TNF-α
|
Mise à jour en attente
|
xérophtalmie, uvéite antérieure
|
Novartis Pharma AG, Oculis SA, Alcon AG
|
Phase II
|
|
SAR-443726
|
nanocorps anti-IL13/OX40L (Sanofi)
|
IL13R, OX40L
|
Mise à jour en attente
|
Maladies génétiques et malformationsTroubles de la peau et du squelette
|
Sanofi
|
Phase I
|
|
Deoxymab
|
3E10, PAT-DX1
|
ADN
|
Mise à jour en attente
|
Cancer pancréatique,Lupus érythémateux systémique
|
Patrys Ltd.
|
Phase I
|
|
VTx 002
|
Mise à jour en attente
|
TDP43
|
Mise à jour en attente
|
Sclérose latérale amyotrophique
|
VectorY BV
|
Préclinique
|
|
VH-7Vk9
|
Anticorps à chaîne unique ciblant la TDP-43, VH-7Vk9
|
TDP43
|
Mise à jour en attente
|
Démence frontotemporale
|
ImStar Therapeutics, Inc.
|
Préclinique
|
|
scFv-h3D6
|
dérivé de bapineuzumab, scFv-h3D6
|
APP
|
Mise à jour en attente
|
Maladie d'Alzheimer
|
Universitat Autonoma de Barcelona
|
Préclinique
|
|
Fv-Hsp70
|
RBB-001, Fv-Hsp72
|
ADN, HSP70
|
Mise à jour en attente
|
Accident vasculaire cérébral ischémique
|
Rubicon
|
Préclinique
|
|
SMET-D1
|
Mise à jour en attente
|
Mise à jour en attente
|
Mise à jour en attente
|
Arthrite, eczéma, psoriasis
|
CentryMed
|
Préclinique
|
|
PMC-401s
|
ScFv humain complet anti-ANG2 antagoniste, PMC-401s
|
Ang2
|
Mise à jour en attente
|
Rétinopathie diabétique, Dégénérescence maculaire
|
PharmAbcine Inc.
|
Préclinique
|
|
T-1649
|
Mise à jour en attente
|
TNF-α
|
Mise à jour en attente
|
Psoriasis
|
Teraclon
|
Préclinique
|
|
IMX-120
|
Nanoparticules contenant un anticorps ScFv contre le GLUT-1
|
GLUT1
|
Mise à jour en attente
|
Colite ulcéreuse, maladie de Crohn, ostéarthrite
|
Immix Biopharma, Inc.
|
Préclinique
|
|
CGX-208
|
scFv anti-alpha-synucléine mal repliée
|
α-synucléine
|
Mise à jour en attente
|
Maladie de Parkinson
|
Cognyxx Pharmaceuticals
|
Préclinique
|
|
GTB-5550
|
GTB-5550 TriKE, GTB-5550
|
CD276
|
Mise à jour en attente
|
Carcinome épidermoïde de la tête et du cou, Myélome multiple
|
GT Biopharma
|
Préclinique
|
|
scFv-235
|
fragment d'antibody à chaîne unique variable, scFv-235
|
TAU
|
Mise à jour en attente
|
Maladie d'Alzheimer
|
Fondation Lundbeck
|
Préclinique
|
|
TA-101
|
fragment d'antibody à domaine unique recombinant, TA-101
|
TNF-α
|
Mise à jour en attente
|
Arthrite rhumatoïde
|
TechnoPhage
|
Préclinique
|
|
DNX-214
|
Mise à jour en attente
|
Mise à jour en attente
|
Mise à jour en attente
|
Dégénérescence maculaire liée à l'âge humide
|
DNX
|
Préclinique
|
|
NI-205
|
Mise à jour en attente
|
TDP43
|
Mise à jour en attente
|
Démence frontotemporale
|
Biogen, Neurimmune
|
Préclinique
|
|
ARA-8
|
Mise à jour en attente
|
Mise à jour en attente
|
Mise à jour en attente
|
Inflammation
|
|
Préclinique
|
|
P-1000
|
Mise à jour en attente
|
Mise à jour en attente
|
Mise à jour en attente
|
Cancer
|
Centre allemand de recherche sur le cancer
|
Préclinique
|
|
MRT-201
|
anticorps synthétique contre la granzyme B, GranzymeB-Fc-scFv4D5, MRT-201
|
HER2
|
Mise à jour en attente
|
Cancer
|
Clayton, Mirata
|
Préclinique
|
|
MRT-101
|
Protéine de fusion Granzyme B/anticorps, GrB-Fc-IT4
|
TWEAK
|
Mise à jour en attente
|
Cancer
|
Clayton, Mirata
|
Préclinique
|
Référence :
[1] Weisser NE, Hall JC. Applications des fragments variables uniques d'anticorps dans les thérapeutiques et les diagnostics. Biotechnol Adv. 2009 juil-août;27(4):502-20. doi: 10.1016/j.biotechadv.2009.04.004.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN


