L’importance du développement de processus en amont
Le processus en amont (USP), également connu sous le nom de processus de fermentation, est l'une des phases initiales du biotraitement en amont. Le processus de fermentation microbienne est crucial pour la culture cellulaire à haute densité et l’expression de gènes exogènes, ce qui affecte directement le rendement et le coût des produits biologiques.
Dans les premières étapes du développement de produits biologiques (préclinique ou phase 1/2), l'accent est mis sur le développement de processus évolutifs sans animaux avec un rendement intermédiaire et répondant à toutes les normes de qualité des produits.
Aux stades avancés (phase 3 ou commerciale), nous nous concentrerons sur le rendement, la robustesse, l'évolutivité et la reproductibilité, générant ainsi un processus rentable. Les activités qui répondent à ces questions sont les études de caractérisation et de validation des procédés. Parallèlement, les outils de qualité par conception (QbD) et de conception d'expériences (DoE) sont généralement appliqués.
Mots clés : développement, optimisation et validation de processus, processus de fermentation, fermentation de cellules microbiennes, fermentation bactérienne, fermentation de levures, fermentation à haute densité, fermentation par souches artificielles
Application : Industrie biopharmaceutique, médecine humaine, médecine animale, vaccin, produits biologiques recombinants à grosses molécules, produits biologiques recombinants, réactif biologique
Solutions USP de Yaohai Bio-Pharma
Bénéficiant de plus de 10 ans d’expérience en fermentation microbienne, Yaohai Bio-Pharma possède l’expertise nécessaire pour aider à résoudre les défis des processus de fermentation. Nous pouvons rapidement établir des stratégies de fermentation à haute densité pour Escherichia coli (E. coli) sécrétion périplasmique, expression intracellulaire de corps solubles ou d'inclusion et expression extracellulaire ou intracellulaire de levure.
Nos services généraux de développement de fermentation disponibles comprennent :
- Conception du processus de fermentation réalisé à petite échelle de 7 L en mode fed-batch
- Validation du procédé en trois lots dans des fermenteurs de 7 L
- Une mise à l'échelle du procédé intermédiaire jusqu'à 30L/70L
Nous pouvons effectuer de manière flexible une optimisation multiparamétrique pour atteindre le rendement ou la proportion souhaitée, en utilisant One-Time-A-Factor (OTAF) ou la conception d'expériences (DoE).
Les principaux paramètres de fermentation sont répertoriés comme suit :
Compositions de milieux de fermentation sans animaux
Sans antibiotique ou non, Volume d'inoculum
Température de croissance, pH, niveau d'oxygène dissous (OD)
Mode d'alimentation (par exemple, fed-batch)
Concentration de l'inducteur (par exemple, IPTG, méthanol), point d'induction (poids humide de la cellule/OD600),
Température d'induction, temps d'induction
et ainsi de suite
Détails du service
| Services |
Process Flow |
| Culture en flacon shake (500 ml) |
Préparation de milieux sans animaux → Culture de graines microbiennes → Culture en shaker → Induction → Récolte |
| Culture en fermenteur (7 L) |
Préparation de milieux sans animaux → Culture de graines microbiennes → Fermentation cellulaire haute densité dans un bioréacteur de 7 L → Induction → Récolte |
| Contrôle qualité des protéines/peptides |
Prétraitement Expression soluble intracellulaire : Récolte et remise en suspension des cellules microbiennes → Concassage par ultrasons → Élimination des débris cellulaires → Extrait brut Expression du corps d'inclusion : Récolte et remise en suspension des cellules microbiennes → Concassage par ultrasons → Préparation du corps d'inclusion → Extrait brut Expression soluble extracellulaire : Collecte du surnageant de culture → Concentration et tampon échange → Extrait brut Analyse qualité Extrait brut comme échantillon → Analyse des protéines cibles par SDS PAGE ou Western blot (WB) |
| Contrôle qualité des plasmides |
Prétraitement et analyse qualitéExtraction des plasmides → Analyse de l'ADN par électrophorèse sur gel d'agarose |
Étude de cas
Notre client nous demande d’augmenter le rendement en hormones polypeptidiques cibles de 8 g/L à 10 g/L.
Sur la base du plan factoriel complet et du plan de surface de réponse des outils DoE, nous avons rapidement reconnu et optimisé les paramètres clés de fermentation. Dans le cadre du processus de fermentation optimisé à haute densité cellulaire, le niveau d’expression a augmenté jusqu’à 10 g/L.
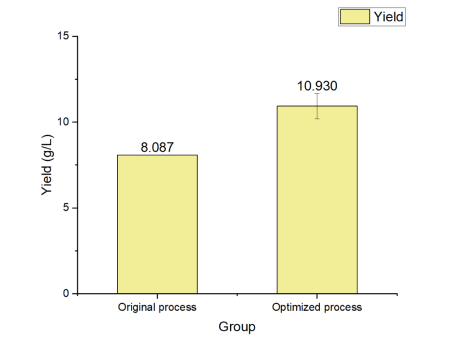
Nos expériences
- Nous avons travaillé sur différents types d'hôtes microbiens, par exemple, d'E. coli DH5α, TOP10, Trans10, BL21 ; Pichia pastoris (P. pastoris) SMD1168H, X-33, GS115, souche PichiaPink1/2/3/4 ; Saccharomyces cerevisiae (S. cerevisiae) ainsi que Hansenula polymorpha (H. polymorpha).
- Nous sommes expérimentés avec E. coli sécrétion périplasmique, expression des corps solubles et d'inclusion, ainsi que expression intracellulaire ou extracellulaire de la levure. Le rendement en corps d'inclusion peut atteindre 10 g/L, tandis que le rendement en protéines solubles varie de 0.5 à 15 g/L.
- Nous avons participé au développement et à la fabrication de diverses grosses molécules, notamment des vaccins sous-unitaires recombinants, des particules pseudo-virales (VLP), des hormones (insuline, GLP-1, hormone de croissance), des cytokines (Interleukine-2/IL-2, IL -15, IL-21), facteurs de croissance (EGF, FGF, NGF), nanobodies/anticorps monodomaines (sdAbs), enzymes, etc.
- neuf
Système de fermentation 7L*16

Cedex Bio Analyser, analyseur de bioprocédés


 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NON
NON
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN




