با کاربرد گسترده واکسنهای mRNA علیه کووید-19 در جمعیتهای بزرگ، ایمنی واکسنهای mRNA تأیید شده است. mRNA قابلیت بیان هر پروتئین را دارد و راهحلهای بالقوهای برای نیازهای بالینی غیرمقضی ارائه میدهد.
یائوهای بیو-فارما راهحل کاملی برای توسعه mRNA و تولید GMP ارائه میدهد که توسط یک-platform تحقیقاتی قوی و سیستم GMP مطابق پشتیبانی میشود. خدمات ما برای برآورده کردن نیازهای منحصر به فرد مشتریان خود طراحی شده است و محصولات دارویی mRNA با کیفیت بالا و محصولات نهایی LNP-mRNA را از میلیگرم تا گرم، همچنین گزارشات دقیق توسعه و تولید و گزارشات آزمایش ارائه میدهد.
ما اجازه استفاده از فناوری پتنت LNP را از شرکت همکار خود، نانوستار فارما، دریافت کردهایم که اطمینان حاصل کند از جدالهای پتانسیل پتنت در آینده جلوگیری شود.
راهحل یکپارچه mRNA/LNP از یائوهای بیو-فارما
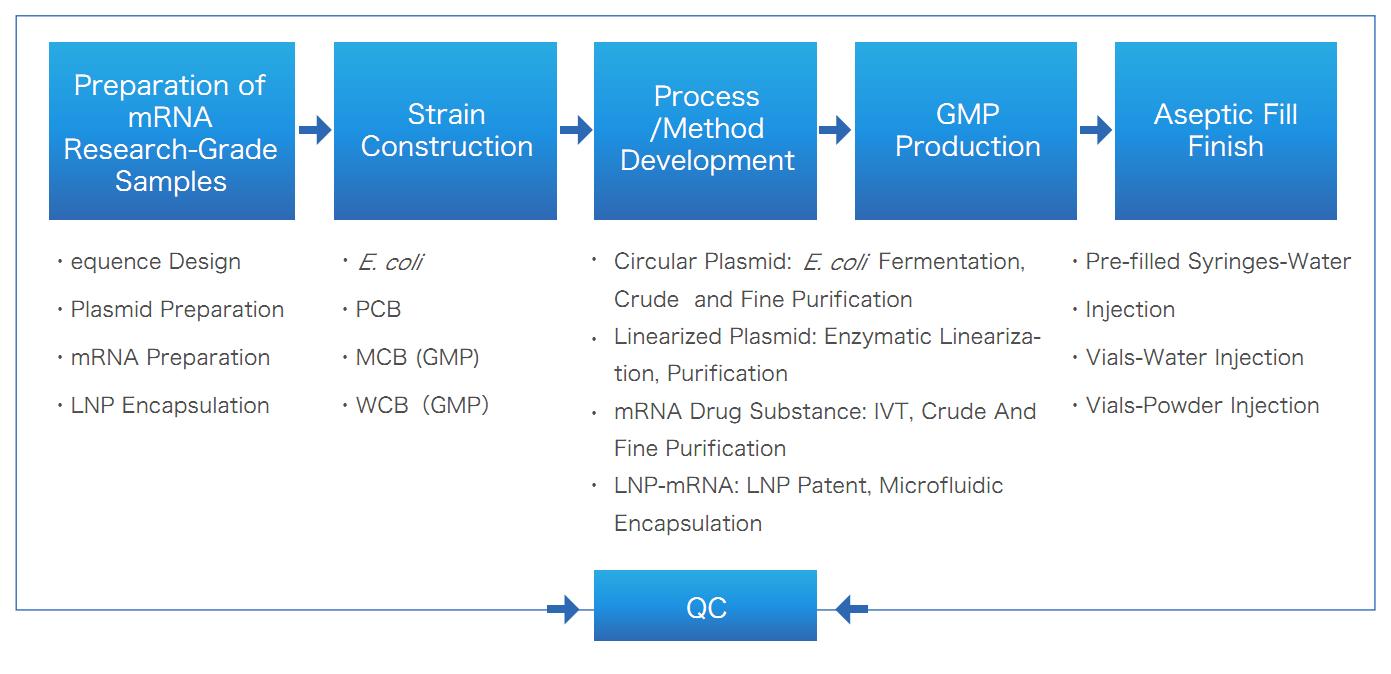
محصولات تحویلی
| دسته بندی |
محصولات تحویلی |
مشخصات |
کاربردها |
| غیر-GMP |
مواد دارویی، mRNA |
0.1~10 میلیگرم (mRNA) |
تحقیقات پیش از بالینی مانند تراسپکشن سلولی، توسعه روش تحلیلی، مطالعات پیش از ثبات، توسعه فرمولاسیون |
| محصول دارویی، LNP-mRNA |
| GMP، استریلیته |
مواد دارویی، mRNA |
10 میلیگرم ~ 70 گرم |
داروی نوین تحقیقی (IND)، مجوز آزمایش بالینی (CTA)، تأمین آزمایش بالینی، درخواست مجوز تجاری زیستی (BLA)، تأمین تجاری |
| محصول دارویی، LNP-mRNA |
5000 شیشه یا سیرینهای پیشآماده/کارتidgeها |
خدمات mRNA CRDMO Yaohai، که شامل حیاتنامه کامل mRNA میباشد
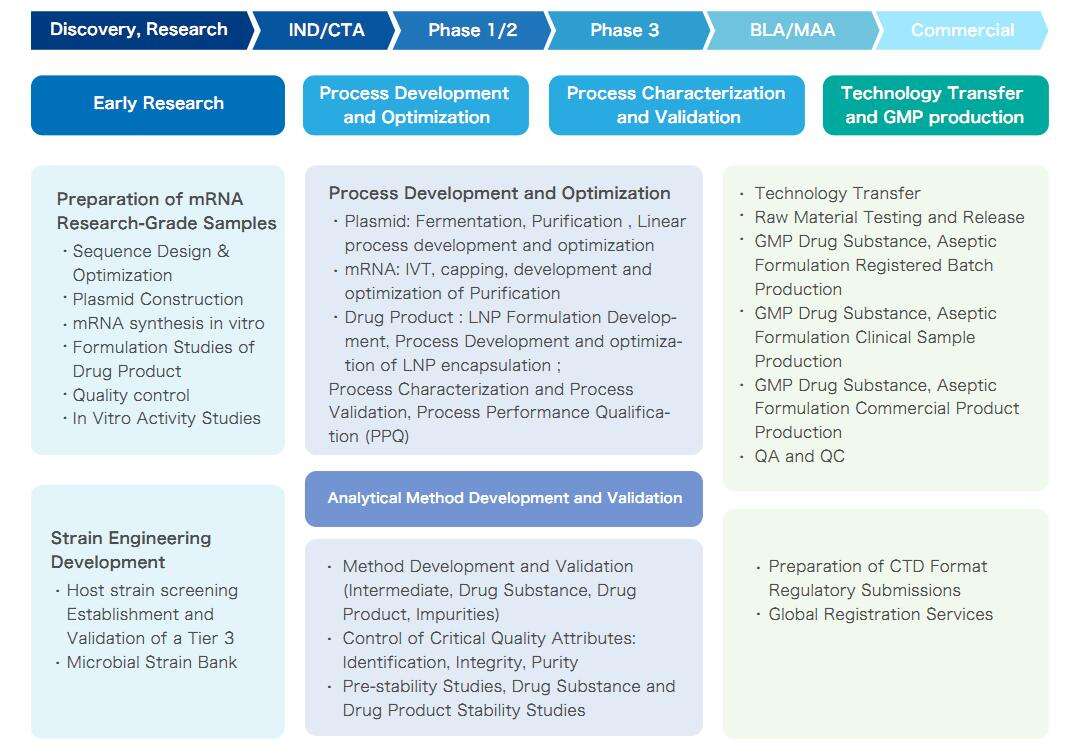
ویژگیهای پلتفرم
پلتفرم DNA پلاسمید
- سیستمهای چندگانه فرآورش 7 لیتری، بدون استفاده از مواد حیوانی در طول فرآیند
- پیگیری روشن پلاسمیدها و باکتری میزبان، بدون موانع تعریف
- سودمندی پلاسمید شامل پلی A بیش از 500 میلیگرم در لیتر
- نرخ از دست دادن پلی A کمتر از 5 bp
- نسبة پلاسمید سوپراکویلد بیش از 90٪؛ نرخ بازیابی بیش از 55٪
- کارایی خطیسازی بیش از 99٪؛ نرخ بازیابی پلاسمید خطی 90٪
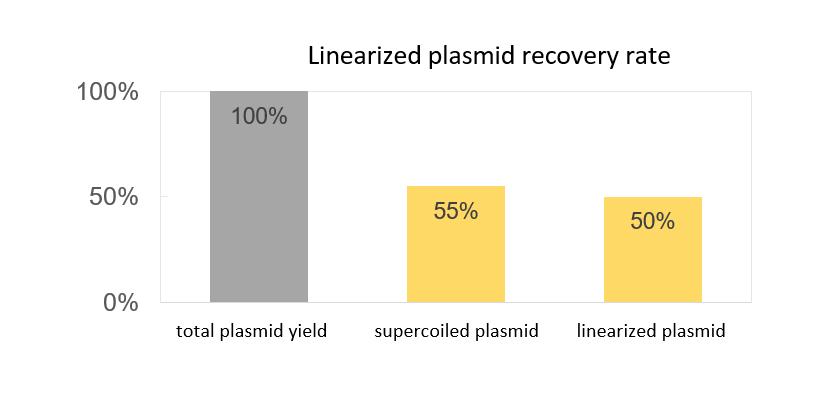
پلتفرم ترکیب داروی mRNA
- چندین راکتور 1 لیتری (GMP)
- نسبة ترجمه بالگرم 1:120، امکان پذیرسازی فرآیند IVT را فراهم می کند
- بیشتری از 98 درصد از بیوژنیت mRNA
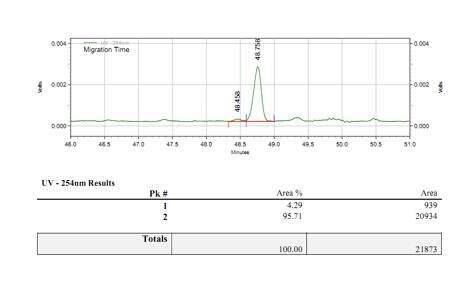
- فرآیند پایدار قطع با نرخ قطع بیش از 95 درصد
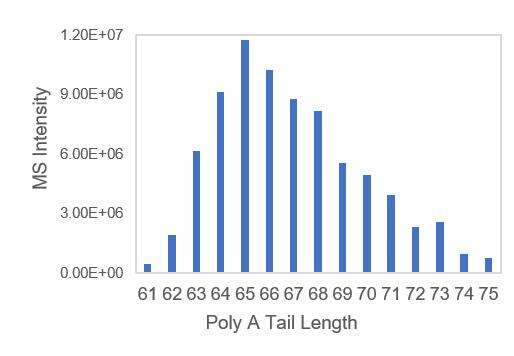
- الگوهای ترجمه با دنباله های A، که توزیع یکنواخت دنباله های poly A را تضمین می کند.
پلتفرم جوشاندن LNP
- فناوری پتنت LNP توسط شرکای ما مجوز داده شده است تا از تضاد پتنت برای مشتریان ما جلوگیری شود.



(شرکای ما)
- استفاده از فرآیند جوشاندن میکروفلویدیک بسیار انعطاف پذیر، که به کارایی جوشاندن بیش از 95 درصد دست می یابد.
- اندازه ذرات LNP در بازه 80-100 نانومتر است، با شاخص پلیدی پایین (PDI) 0.05، که توزیع یکنواخت اندازه ذرات را نشان می دهد.
- ذرات LNP بار ضعیفی دارند، با پتانسیل زتا تقریباً -2.18 میلی ولت.
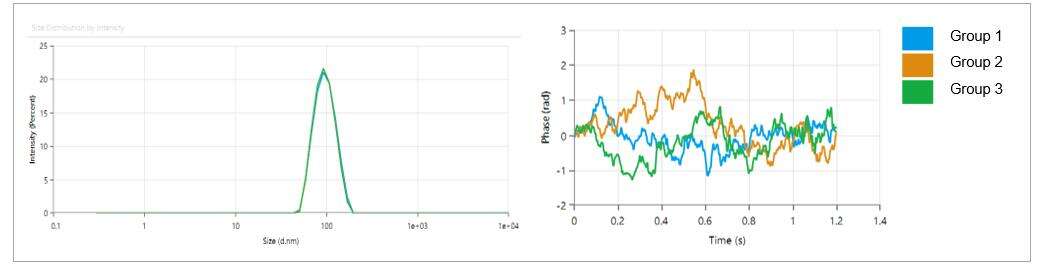
| مورد آزمایش |
روش آزمایش |
نتیجه آزمایش |
| کارایی بستهبندی |
ریبوگرین |
92.7% |
| اندازه ذرات |
مالورن |
92.07 نانومتر |
| PDI |
مالورن |
0.05 |
| زتا |
مالورن |
-2.18 mV |
پلتفرم توسعه روش
ما یک-platform روش توسعه جامع برای تحلیل پلاسمید های دایره ای و خطی، مواد خام mRNA و محصولات نهایی LNP-mRNA ارائه می دهیم. تحلیل ما شامل انواع پارامترهاست، مانند سلامت، خالصی، کارایی کاپینگ، توزیع پلی A، کارایی بسته بندی، اندازه ذرات، مولفه های LNP و باقی مانده های مختلف فرآیند (HCP، HCD، HCR، dsRNA، آنتی بیوتیک ها، DNase I، پلیمراز RNA T7، آنزیم کاپینگ وکسیانا، متیل ترانسفراز 2-O و غیره).
برخی از روش ها به شرح زیر است:
تشخیص سلامت mRNA (الکتروفورز کپیلاری)
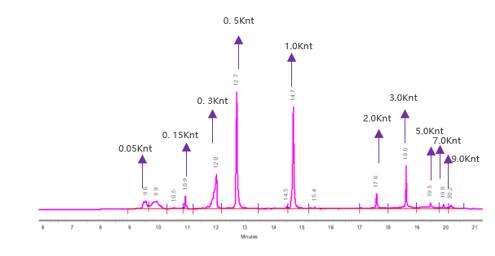
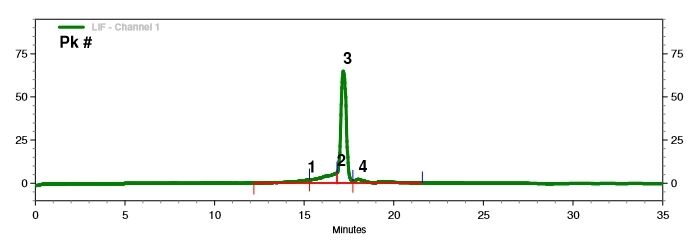
ما شرایط جدایش بهینه را برای جدایش دقیق مولکول های mRNA با طول های مختلف توسعه داده ایم.
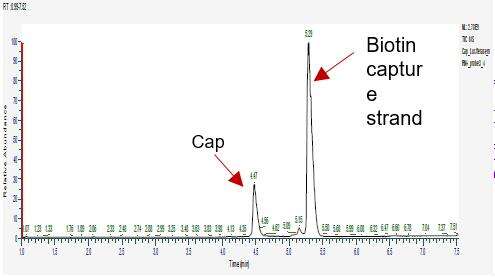
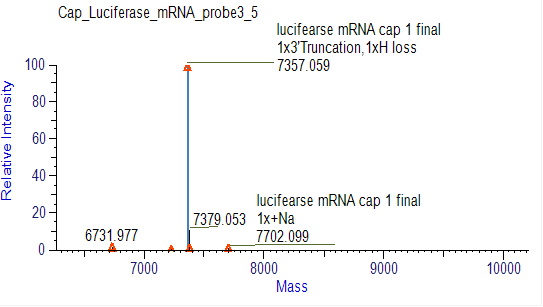
تشخیص کارایی کاپینگ mRNA (LC-MS)
ما شرایط مناسبی برای قطع و جدایش انتهای 5' و جدایش دقیق فراگмент های کاپ شده و ناکاپ شده توسعه داده ایم.
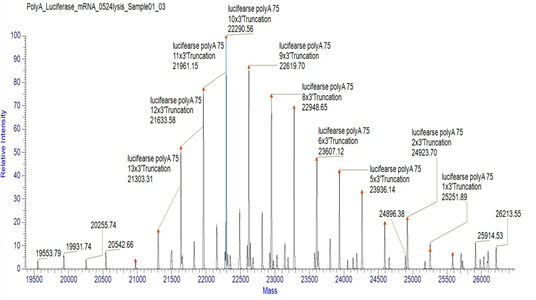
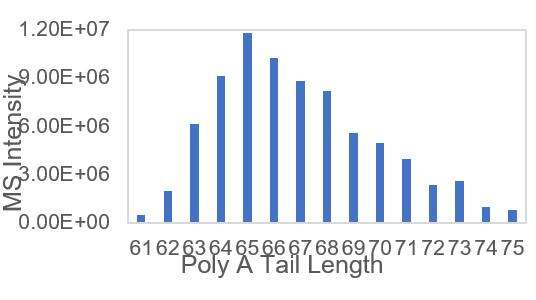
تشخیص توزیع دنباله پلیA مناسب mRNA (LC-MS)
ما شرایط مناسبی برای شکست گزینههای انتهای 3' و جداسازی اولیگونوکلئوتیدهای انتهای 3' توسعه دادهایم که به تشخیص دقیق توزیع دنبالههای polyA کمک میکند.
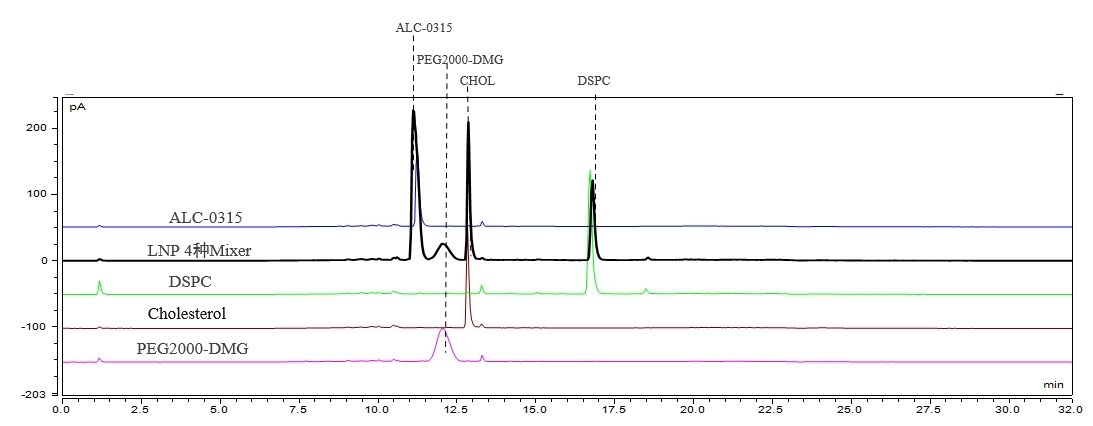
تشخیص مولفهها و محتوای LNP (HPLC-CAD)
ما روش کروماتوگرافی مناسبی برقرار کردهایم که جداسازی پایهای چهار مولفه LNP را امکانپذیر میسازد. این روش قابلیت تکرارشدن ممتازی نشان میدهد.
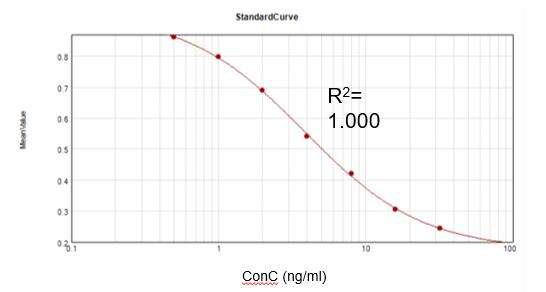
Carthy کانامایسین باقیمانده (ELISA)
بر اساس کیت آزمایش تجاری، منحنی استانداردسازی مناسبی به دست آوردیم (R2 = 1.000) و نرخ بازیابی 104.8% را دستیابی کردیم.
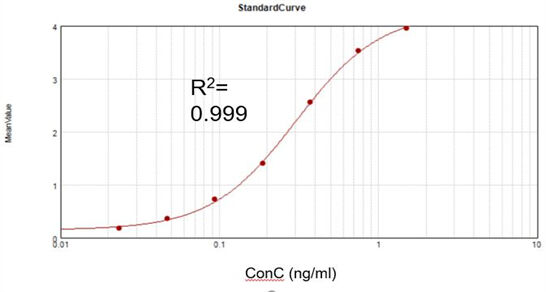
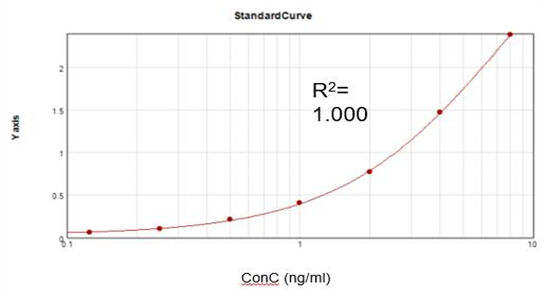
Tsyne dsRNA باقیمانده
بر اساس کیت آزمایش تجاری، منحنی استانداردسازی برازش مناسبی به دست آوردیم (R2 = 0.999) و نرخ بازیابی 105.5% را دستیابی کردیم.
Polimerاز RNA T7 باقیمانده (Elisa)
بر اساس کیت آزمایش تجاری، منحنی استانداردسازی برازش مناسبی به دست آوردیم (R2 = 1.000) و نرخ بازیابی 107.9% را دستیابی کردیم.
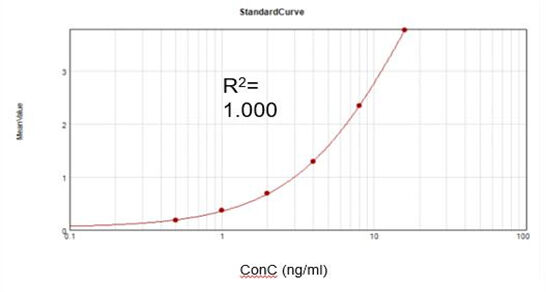
آنزیم کپینگ ویروس Vaccinia باقیمانده (ELISA)
بر اساس یک کیت آزمایش تجاری، منحنی کالیبراسیون مناسبی به دست آوردیم (R2 = 1.000) و نرخ بازیابی 92% را دستیابی کردیم.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN






















