Sự kết hợp kháng nguyên đích với protein vận chuyển cũng là một chiến lược phát triển vắc xin, chẳng hạn như vắc xin liên hợp. Liên kết với protein vận chuyển có thể tăng cường khả năng miễn dịch của vắc xin. Hiện nay, các protein mang đã được phê duyệt trên thị trường bao gồm độc tố bạch hầu (DT), độc tố bạch hầu đột biến không độc hại CRM197, độc tố uốn ván (TT), v.v..
Với nền tảng phát triển quy trình mạnh mẽ, các xưởng BSL-1 và BSL-2 ở cấp độ an toàn sinh học cũng như hệ thống chất lượng GMP, Yaohai Bio-Pharma có thể cung cấp cho khách hàng giải pháp toàn diện từ phát triển chủng vi khuẩn đến sản xuất protein vận chuyển theo tiêu chuẩn GMP.
Chúng tôi cung cấp protein vận chuyển ở quy mô gam đến kilôgam đáp ứng các tiêu chuẩn chất lượng, cũng như hồ sơ sản xuất và báo cáo thử nghiệm GMP cho khách hàng của chúng tôi.
Vắc xin liên hợp đã được phê duyệt bao gồm các protein mang sau (không tái tổ hợp):
|
Các loại protein
|
Protein vận chuyển
|
Các loại căng thẳng
|
Nền tảng
|
|
Protein vận chuyển, được chiết xuất
|
Độc tố bạch hầu đột biến không độc CRM197
|
Corynebacteriae bạch hầu
|
Hệ thống lên men vi sinh vật
Thiết bị ly tâm và đồng nhất
Hệ thống sắc ký cao/áp suất thấp
Bể phản ứng liên hợp
Cấp độ an toàn sinh học: BSL-2
Hệ thống chất lượng GMP
|
|
Giải độc tố bạch hầu (DT)
|
Corynebacteriae bạch hầu
|
|
Độc tố uốn ván (TT)
|
Clostridium tetani
|
|
Phức hợp protein màng ngoài não mô cầu (OMPC)
|
Neisseria meningitidis
|
|
Các protein vận chuyển khác từ nguồn vi sinh vật (BSL-1, BSL-2)
|
|
Các dịch vụ liên quan: Giải pháp CDMO Protein mang tái tổ hợp.
|
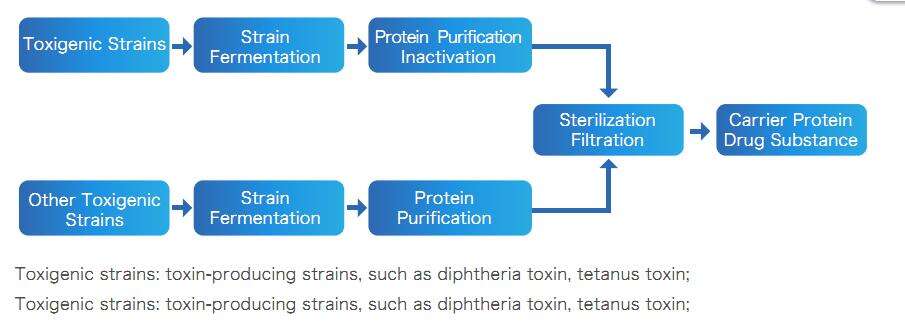
Quy trình sản phẩm thuốc Protein mang
Có thể giao được
| Lớp |
Phân phôi |
Đặc điểm kỹ thuật |
Ứng dụng |
| GMP, BSL-1/BSL-2 |
Chất trung gian |
Protein mang có nguồn gốc từ vi khuẩn |
Nguyên liệu sản xuất vắc xin liên hợp |
| Thành phẩm vắc xin |
Bột đông khô |
Thuốc mới nghiên cứu (IND),
Ủy quyền thử nghiệm lâm sàng (CTA),
Cung cấp thử nghiệm lâm sàng,
Đơn xin giấy phép sinh học (BLA),
Cung cấp thương mại
|

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 KHÔNG
KHÔNG
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN


