ความสำคัญของการพัฒนากระบวนการทางท้าย (DSP)
สารหมักทั้งหมดประกอบด้วยโปรตีนเป้าหมายหรือพลาสมิด รวมถึงสิ่งปนเปื้อนที่เกี่ยวข้องกับผลิตภัณฑ์และกระบวนการ เช่น อณูรวม (aggregates) ส่วนประกอบของเซลล์จุลินทรีย์ โปรตีนของเซลล์แม่พันธุ์ (HCP) ดีเอ็นเอของเซลล์แม่พันธุ์ (HCD) เอนโดท็อกซิน และยาปฏิชีวนะ
ดังนั้น การออกแบบกระบวนการ DSP ที่มีประสิทธิภาพและการทำให้บริสุทธิ์เพื่อขจัดสิ่งปนเปื้อนบางอย่างและผลิตสารออกฤทธิ์ทางเภสัชกรรมที่บริสุทธิ์สูงและมีคุณภาพสูงจึงเป็นสิ่งสำคัญ นอกจากนี้ การปรับปรุงกระบวนการทำให้บริสุทธิ์ยังสามารถช่วยเพิ่มการฟื้นตัวของผลิตภัณฑ์ ลดต้นทุน และปรับปรุงความสามารถในการขยายขนาดและความสามารถในการทำซ้ำของกระบวนการได้อีกด้วย
คำสำคัญ: การพัฒนากระบวนการ, การเพิ่มประสิทธิภาพและการตรวจสอบ, กระบวนการการฟอกสิ่งปนเปื้อน, โครมาโทกราฟี, การกำจัดสิ่งปนเปื้อน, การกำจัด HCP, การกำจัด HCD, การกำจัดเอนโดท็อกซิน, การเปลี่ยนรูปร่างโปรตีนและการพับใหม่, การประกอบ VLP, การเชื่อมโยง
การประยุกต์ใช้: อุตสาหกรรมไบโอฟาร์มา, ยาสำหรับมนุษย์, ยาสำหรับสัตว์, วัคซีน, ชีวโมเลกุลขนาดใหญ่ที่สร้างขึ้นใหม่, ชีวโมเลกุลที่สร้างขึ้นใหม่, เรจินที่เกี่ยวข้องกับชีวภาพ
โซลูชัน DSP ของ Yaohai Bio-Pharma
เรามีประสบการณ์มากมายในการแยกโปรตีนเป้าหมายหรือพลาสมิดจากเมทริกซ์ที่ซับซ้อนโดยการพัฒนาและเพิ่มประสิทธิภาพกระบวนการฟอกในลำดับถัดไป มีการดำเนินงานหน่วยประเภทต่าง ๆ ที่เหมาะสมสำหรับการฟอกชีวโมเลกุล เช่น การหมุนเหวี่ยง, การกรอง, การโฮโมจีไนเซชัน, การแตกตัวด้วยด่าง, การกรองแบบอัลตรา, การตกตะกอน, การเปลี่ยนรูปร่างโปรตีนและการพับใหม่, โครมาโทกราฟี เป็นต้น
บริการพัฒนาการฟอกที่เรามีให้ ได้แก่:
- การพัฒนากระบวนการฟอกทั้งหมดตั้งแต่การรวบรวมเซลล์หรือสารละลายจนถึงส่วนประกอบที่ใช้งานได้ในที่สุด
- การปรับปรุงกระบวนการฟอกให้เหมาะสมตามความไม่บริสุทธิ์ที่เกี่ยวข้องกับผลิตภัณฑ์และกระบวนการ เพื่อเพิ่มคุณภาพและความปลอดภัยของผลิตภัณฑ์ เช่น HCP, HCD, เอนโดท็อกซิน
- การกำหนดและปรับปรุงพารามิเตอร์สำคัญในหนึ่งหรือหลายกระบวนการปฏิบัติการ รวมถึงการแตกเซลล์ การกรองแบบ dòng เรเดียล การคัดเลือกเรซิน การแยกด้วยโครมาโทกราฟี การทำให้โปรตีนเสื่อมสภาพและการพับใหม่ เป็นต้น
- การปรับปรุงกระบวนการในแง่ของคุณภาพ ผลผลิต การกู้คืน ต้นทุน และความสามารถในการขยายขนาด
- การตรวจสอบความถูกต้องของกระบวนการฟอกทางปลายน้ำ
- การประเมินช่วงพารามิเตอร์ตามหลักการจัดการความเสี่ยงและการออกแบบการทดลอง (DoE) ในโมเดลกระบวนการ
รายละเอียดบริการ
แพลตฟอร์มการฟอกโปรตีนหรือพลาสมิดมาตรฐานจะอาศัยขั้นตอนการฟอกคร่าวหลายขั้นตอนและน้อยกว่า 4 ขั้นตอนของการแยกด้วยโครมาโทกราฟี รวมถึงการจับตัว การฟอกกลาง และการขัดเงา
| รายละเอียดบริการ |
หน่วยการดำเนินงาน |
พารามิเตอร์ |
| การฟอกคร่าว |
การแยกสารด้วยแรงเหวี่ยง |
ความเร็วในการหมุน ระยะเวลา |
| การ.homogenization ความดันสูง |
ปริมาณของแข็งทั้งหมด, ความดัน, รอบ |
| กระบวนการ Lysis กรดในต่อเนื่อง |
อัตราส่วนของเซลล์ที่ถูกย่อยใหม่ต่อสารละลายสำหรับการทำลายเซลล์, เวลาการทำลายเซลล์ |
| การกรองแบบ Tangential Flow |
วัสดุเยื่อหุ้มและขนาดรูพรุน, อัตราการไหลของสารละลาย, ความดันข้ามเยื่อหุ้ม (TMP), อัตราส่วนปริมาตรของฟิลเทรตต่อพื้นที่ของเยื่อหุ้ม |
| การตกตะกอน |
ชนิดและความเข้มข้นของสารทำให้ตกตะกอน, สารเสริม, pH, อุณหภูมิ, เวลา |
| การเปลี่ยนรูปและทำให้กลับมาเป็นรูปเดิม |
การละลายโปรตีนจาก inclusion body |
ความเข้มข้นของสารทำให้เปลี่ยนสภาพ (เช่น Urea, Guanidine HCl, สบู่ไอออนิกแรง), สบู่ (เช่น Sodium dodecyl sulfate, SDS), ตัวช่วยลด (เช่น Dithiothreitol, DTT), สารจับโลหะ (Ethylenediaminetetraacetic acid, EDTA), อุณหภูมิ, เวลา |
| การพับโปรตีนกลับ |
วิธีการพับกลับ (การเจือจาง, การดายาลิซิส หรือ SEC refolding), ความเข้มข้นของโปรตีน, บัฟเฟอร์, pH, อุณหภูมิ, เวลา, สารออกซิไดซ์และตัวช่วยลด (เช่น Glutathione, GSH/ Glutathione ออกซิไดซ์, GSSH, DTT/GSSH, Cysteine/Cystine), สารเสริมโมเลกุลขนาดเล็ก (L-arginine, Urea, Guanidine/HCl, และสบู่) |
| การเก็บกัก, การกรองกลาง และการทำให้บริสุทธิ์ในขั้นสุดท้าย |
AC (Affinity Chromatography) |
ประเภทต่าง ๆ ของเรซิน/คอลัมน์โครมาโทกราฟี (เช่น AC, IEX, HIC, SEC, RPC, MMC), ความยาวและความกว้างของคอลัมน์, องค์ประกอบของบัฟเฟอร์, ปริมาตรการฉีด, องค์ประกอบของเฟสเคลื่อนที่ (การดูดซึมและการปลดปล่อย), pH, อัตราการไหล, เงื่อนไขของการผูกพัน, การล้าง และการชะล้าง |
| IEX (โครมาโทกราฟีแลกเปลี่ยนประจุบวกหรือลบ) |
| HIC (Hydrophobic Interaction chromatography) |
| การแยกเกลือและ/หรือโครมาโทกราฟีการแยกตามขนาด (SEC) |
| RPC (โครมาโทกราฟีเฟสกลับ) |
| MMC, โครมาโทกราฟีแบบผสม |
กรณีศึกษา
กรณีที่ 1
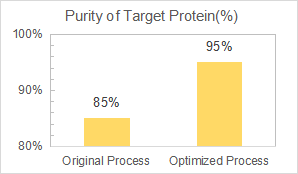
เราได้รับมอบหมายให้พัฒนาและปรับแต่งกระบวนการเพิ่มความบริสุทธิ์ของโปรตีนจาก 85% เป็น 90% ในขณะที่ลดขั้นตอนของการทำโครมาโทกราฟี
ยาหัยได้ส่งมอบกระบวนการเพิ่มความบริสุทธิ์ที่แข็งแรงและสามารถขยายขนาดได้ด้วย 3 ขั้นตอนของการทำโครมาโทกราฟีสำหรับโปรตีนเป้าหมายซึ่งเป็นสารก่อภูมิแพ้ในแบคทีเรีย และความบริสุทธิ์สุดท้ายถึง 95%
กรณีที่ 2
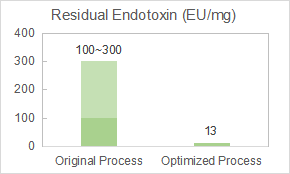
ยาหัยได้รับมอบหมายจากลูกค้าของเราให้ปรับแต่งกระบวนการกำจัดเอนโดทอกซินของวัคซีน VLP (อนุภาคคล้ายไวรัส)
ทีมของเราได้ทำการปรับแต่งพารามิเตอร์ของการทำโครมาโทกราฟีและเตรียมสารยาที่มีความบริสุทธิ์ 98% และเศษเหลือของเอนโดทอกซิน 12.8EU/mg
ประสบการณ์ของเรา
- เราได้มีส่วนร่วมในการพัฒนาและการผลิตโมเลกุลขนาดใหญ่หลายชนิด รวมถึงวัคซีนย่อยที่สร้างขึ้นใหม่ (recombinant subunit vaccines), VLPs, ฮอร์โมน (อินซูลิน, GLP-1, ฮอร์โมนการเจริญเติบโต), ไซโตไคน์ (Interleukin-2/IL-2, IL-15, IL-21), แฟคเตอร์การเจริญเติบโต (EGF, FGF, NGF), นาโนบอดี้/แอนติบอดีโดเมนเดี่ยว (sdAbs), เอนไซม์ ฯลฯ
อุปกรณ์
เราใช้ระบบ AKTA Pure, AKTA Avant และ Preparative HPLC ที่เป็นผู้นำในอุตสาหกรรมสำหรับการดำเนินงานวิธีโครมาโทกราฟีหลากหลายประเภท เช่น โครมาโทกราฟีแบบพันธะเฉพาะ, แบบแลกเปลี่ยนไอออน, แบบปฏิกิริยาไฮโดรโฟบิก, แบบเฟสกลับ และแบบแยกตามขนาด




 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN






