Med den utbredda tillämpningen av mRNA COVID-19-vacciner i stora populationer har säkerheten för mRNA-vacciner validerats. mRNA har förmågan att uttrycka vilket protein som helst och erbjuder potentiella lösningar för olika otillfredsställda kliniska behov.
Yaohai Bio-Pharma tillhandahåller en heltäckande lösning för mRNA FoU och GMP-produktion, uppbackad av en robust forskningsplattform och ett kompatibelt GMP-system. Våra tjänster är skräddarsydda för att möta våra kunders unika krav, och erbjuder dem högkvalitativa mRNA-läkemedelssubstanser och LNP-mRNA färdiga produkter i mängder från milligram till gram, samt detaljerade utvecklings- och produktionsrapporter och testrapporter.
Vi har erhållit auktorisation för LNP-patentteknologi från vår partner, NanoStar Pharmaceuticals, vilket säkerställer att vi kan undvika potentiella patenttvister i framtiden.
mRNA/LNP One-Stop Solution av Yaohai Bio-Pharma
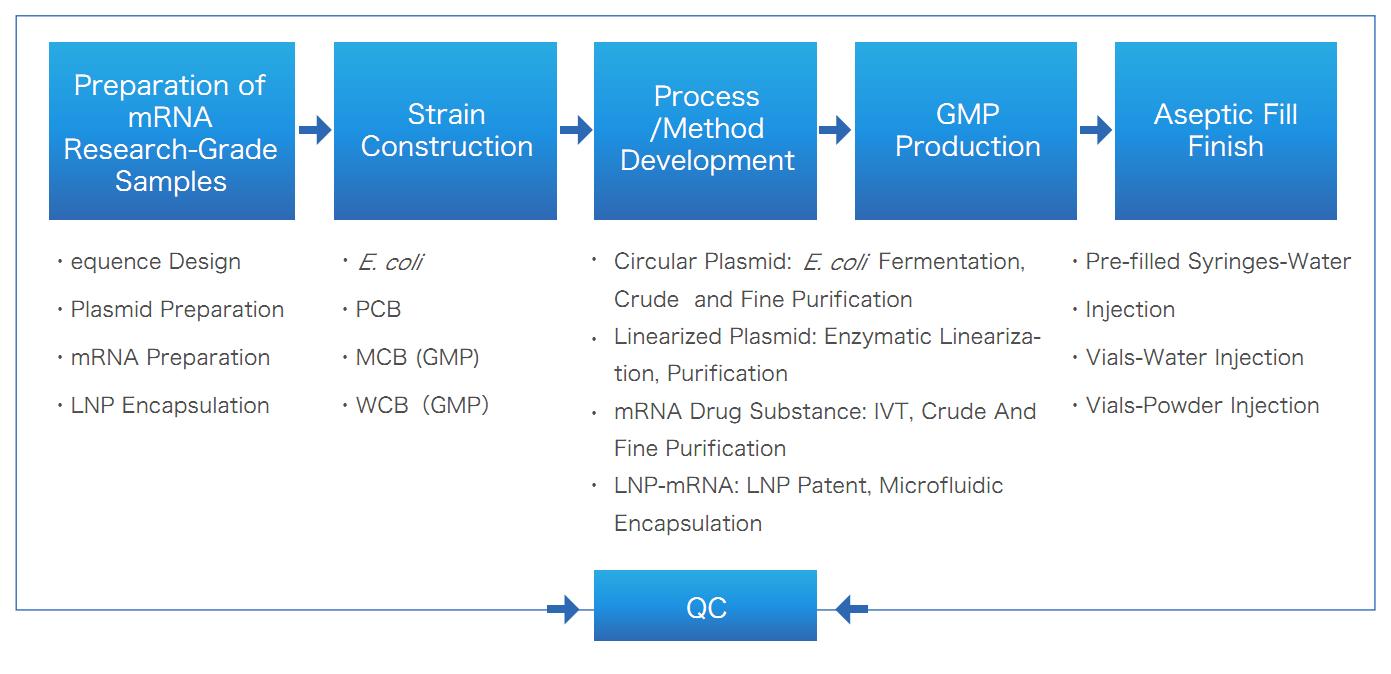
Deliverables
| Grade |
Deliverables |
Specifikation |
Tillämpningar |
| icke-GMP |
Läkemedelssubstans, mRNA |
0.1~10 mg (mRNA) |
Preklinisk forskning såsom celltransfektion, Analytisk metodutveckling, Pre-stabilitetsstudier, Formuleringsutveckling |
| Läkemedelsprodukt, LNP-mRNA |
| GMP, Sterilitet |
Läkemedelssubstans, mRNA |
10 mg~70 g |
Undersökande nytt läkemedel (IND), auktorisation för kliniska prövningar (CTA), leverans av kliniska prövningar, ansökan om biologisk licens (BLA), Kommersiell leverans |
| Läkemedelsprodukt, LNP-mRNA |
5000 injektionsflaskor eller förfyllda sprutor/patroner |
Yaohais mRNA CRDMO-tjänst som täcker hela livscykeln för mRNA
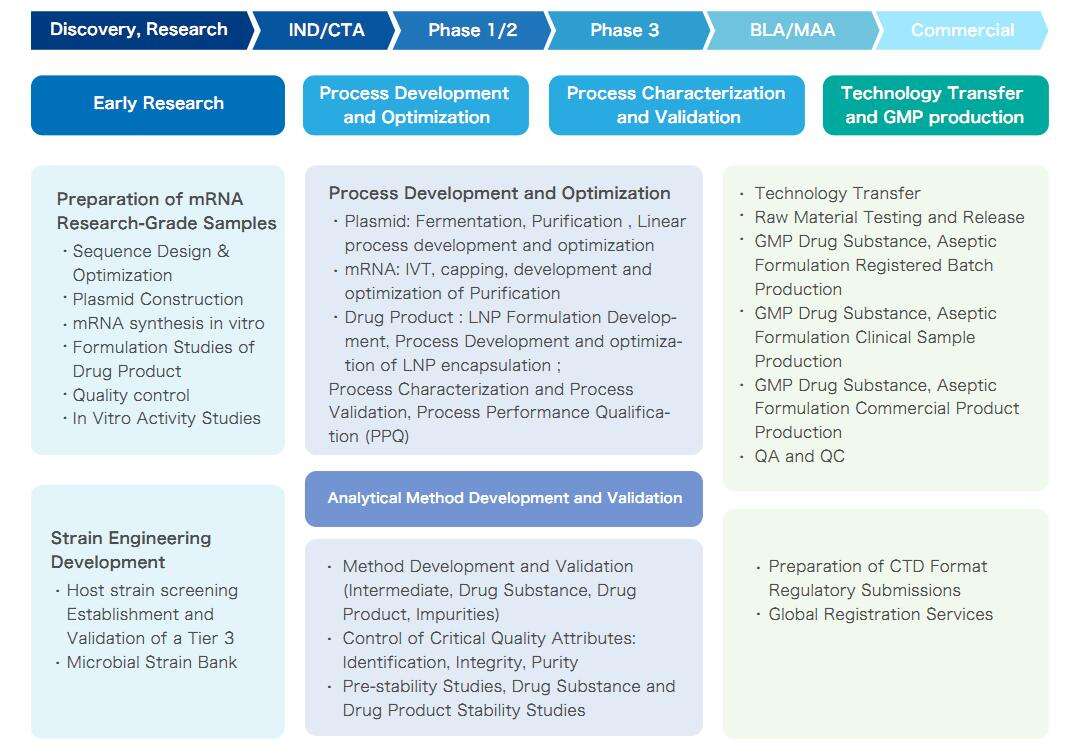
Platformfunktioner
Plasmid DNA-plattform
- Flera 7L fermenteringssystem, djurfria under hela processen
- Tydlig spårbarhet av plasmider och värdbakterier, utan deklarationshinder
- Utbytet av plasmid innehållande poly A som överstiger 500 mg/L
- Poly A förlusthastighet mindre än 5 bp
- Superspolad plasmidandel större än 90 %; återvinningsgrad över 55 %
- Linjäriseringseffektivitet som överstiger 99 %; linjäriserad plasmidåtervinningshastighet på 90 %
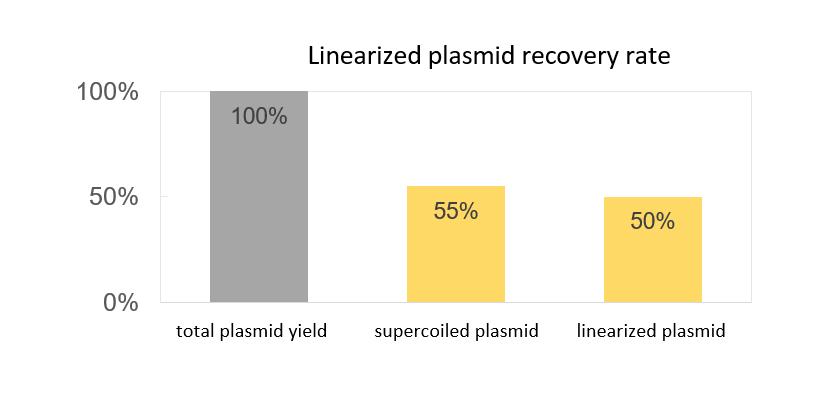
Läkemedelssubstans Plattform av mRNA
- Flera 1L reaktorer (GMP)
- Ett högt transkriptionsförhållande på 1:120, möjliggör en skalbar IVT-process
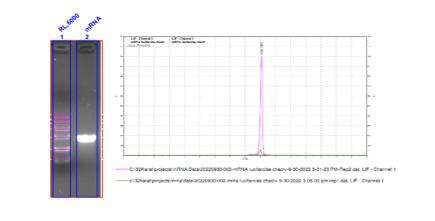
- mRNA-integritet överstiger 98 %
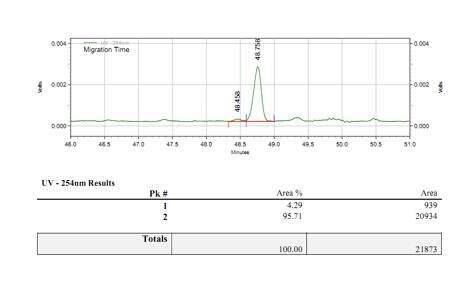
- Stabil övertäckningsprocess med en täckningsgrad på över 95 %
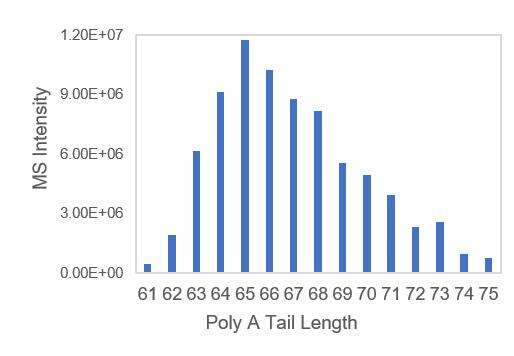
- Transkriptionsmallar med A-svansar, säkerställer enhetlig fördelning av poly A-svansar.
LNP Inkapslingsplattform
- LNP-patentteknologi godkänd av våra partners för att säkerställa undvikande av patenttvister för våra kunder.



(Våra partners)
- Använder en mycket mångsidig mikrofluidisk inkapslingsprocess, vilket uppnår en inkapslingseffektivitet på över 95 %.
- LNP-partikelstorlek är inom 80-100 nm, med ett lågt polydispersitetsindex (PDI) på 0.05, vilket indikerar en enhetlig fördelning av partikelstorlekar.
- LNP-partiklar uppvisar en svag laddning, med en Zeta-potential på cirka -2.18 mV.
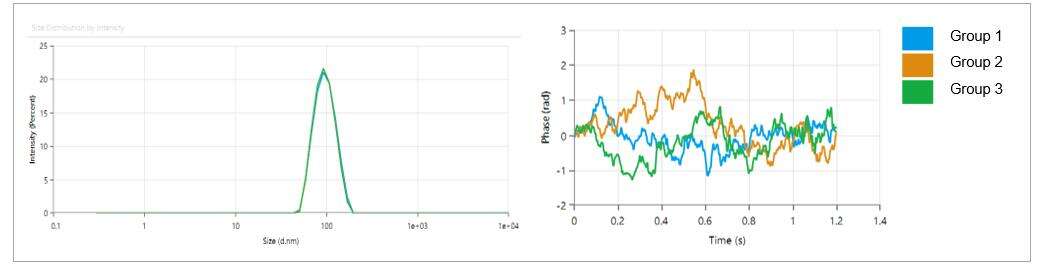
| Testobjekt |
Testmetod |
Testresultat |
| Inkapslingseffektivitet |
Ribogreen |
92.7% |
| Partikelstorlek |
Malvern |
92.07 nm |
| PDI |
Malvern |
0.05 |
| Zeta |
Malvern |
-2.18 mV |
Metodutvecklingsplattform
Vi erbjuder en omfattande metodutvecklingsplattform för att analysera cirkulära och linjäriserade plasmider, mRNA-råmaterial och färdiga LNP-mRNA-produkter. Vår analys täcker en mängd olika parametrar, såsom integritet, renhet, kapslingseffektivitet, poly A-fördelning, inkapslingseffektivitet, partikelstorlek, LNP-komponenter och olika processrester (HCP, HCD, HCR, dsRNA, antibiotika, DNas I, T7 RNA polymeras, vacciniatäckningsenzym, 2-O-metyltransferas, etc.).
Delmetoder demonstreras enligt följande:
Detektion av mRNA-integritet (kapillärelektrofores)
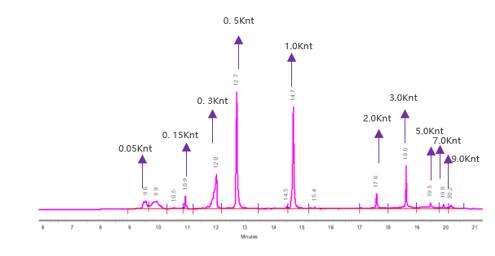
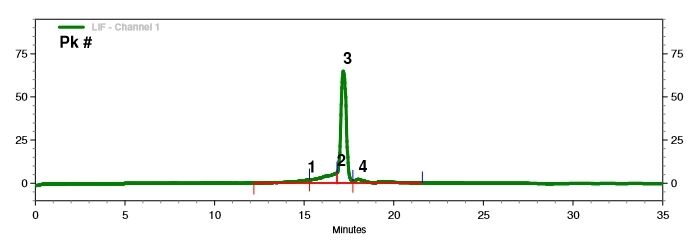
Vi har utvecklat optimala separationsförhållanden för att exakt separera mRNA-molekyler av varierande längd.
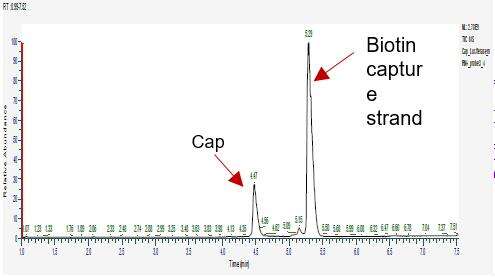
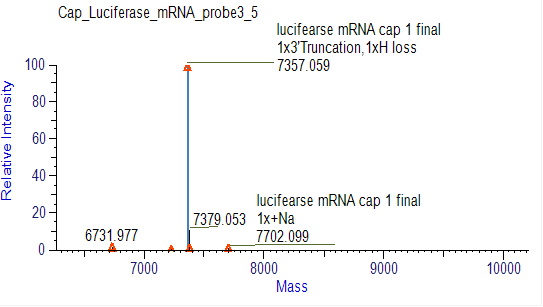
Detektion av mRNA-kapslingseffektivitet (LC-MS)
Vi har utvecklat lämpliga betingelser för 5'-ändsklyvning och separation av 5'-ändeoligonukleotider, vilket möjliggör noggrann separation av kapslade och oskyddade fragment.
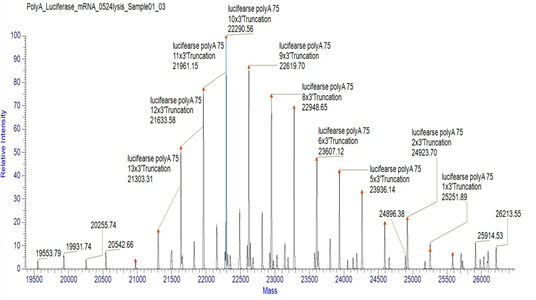
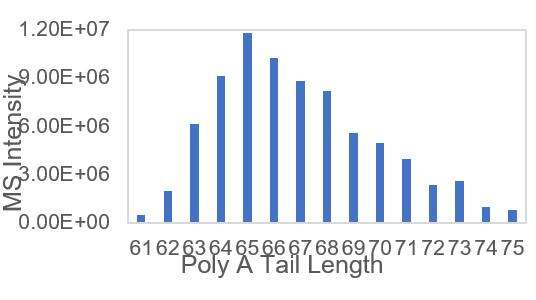
Detektion av mRNA PolyA lämplig svansfördelning (LC-MS)
Vi har utvecklat lämpliga betingelser för klyvning av 3'-ändar och separation av 3'-ände-oligonukleotider, vilket möjliggör exakt detektion av fördelningen av polyA-svansar.
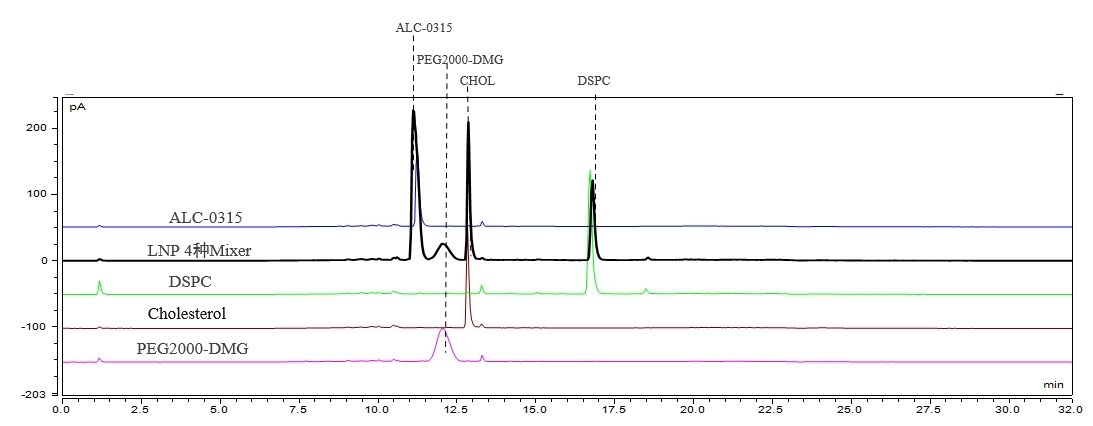
LNP-komponent- och innehållsdetektering (HPLC-CAD)
Vi har etablerat en lämplig kromatografisk metod som uppnår baslinjeseparation av fyra LNP-komponenter. Denna metod visar utmärkt reproducerbarhet.
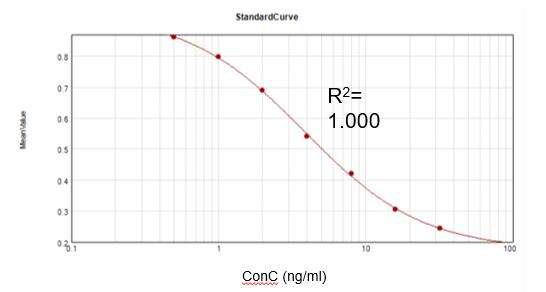
Återstående kanamycinkoncentration (ELISA)
Baserat på ett kommersiellt analyskit erhöll vi en lämplig kalibreringskurva (R2 = 1.000 104.8) och uppnådde en återhämtningsgrad på XNUMX %.
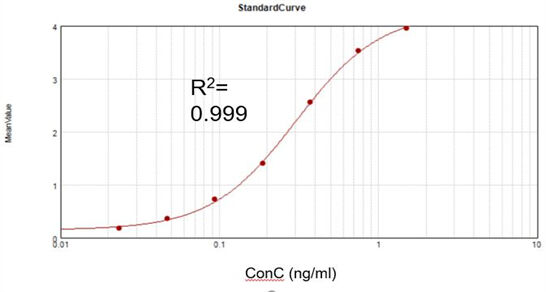
Kvarvarande dsRNA-koncentration
Baserat på ett kommersiellt analyskit erhöll vi en lämplig passningskalibreringskurva (R2 = 0.999) och uppnådde en återhämtningsgrad på 105.5%.
Kvarvarande T7 RNA-polymeras (Elisa)
Baserat på ett kommersiellt analyskit erhöll vi en lämplig passningskalibreringskurva (R2 = 1.000) och uppnådde en återhämtningsgrad på 107.9%.
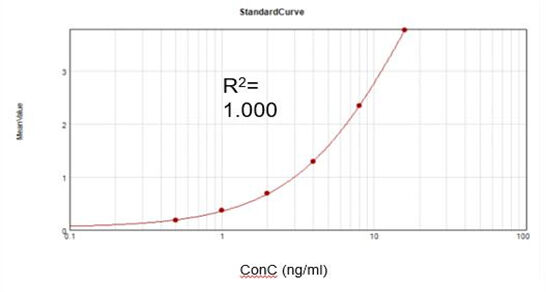
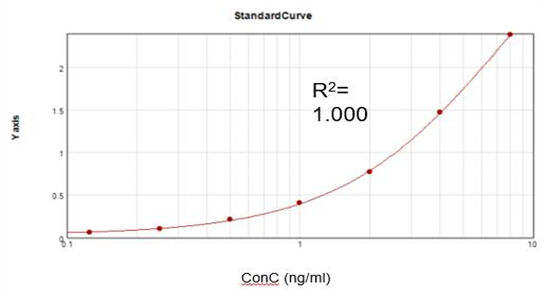
Residual Vaccinia Virus Capping Enzyme (ELISA)
Baserat på ett kommersiellt analyskit erhöll vi en lämplig passningskalibreringskurva (R2 = 1.000) och uppnådde en återhämtningsgrad på 92%.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NEJ
NEJ
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN






















