Med den utbredte bruken av mRNA COVID-19-vaksiner i store populasjoner, har sikkerheten til mRNA-vaksiner blitt validert. mRNA har evnen til å uttrykke ethvert protein, og tilbyr potensielle løsninger på ulike udekkede kliniske behov.
Yaohai Bio-Pharma gir en omfattende løsning for mRNA FoU og GMP-produksjon, støttet av en robust forskningsplattform og et kompatibelt GMP-system. Tjenestene våre er skreddersydd for å møte de unike kravene til våre kunder, og tilbyr dem høykvalitets mRNA-legemiddelstoffer og LNP-mRNA-ferdige produkter i mengder fra milligram til gram, samt detaljerte utviklings- og produksjonsrapporter og testrapporter.
Vi har fått autorisasjon for LNP-patentteknologi fra vår partner, NanoStar Pharmaceuticals, for å sikre å unngå potensielle patenttvister i fremtiden.
mRNA/LNP One-Stop Solution av Yaohai Bio-Pharma
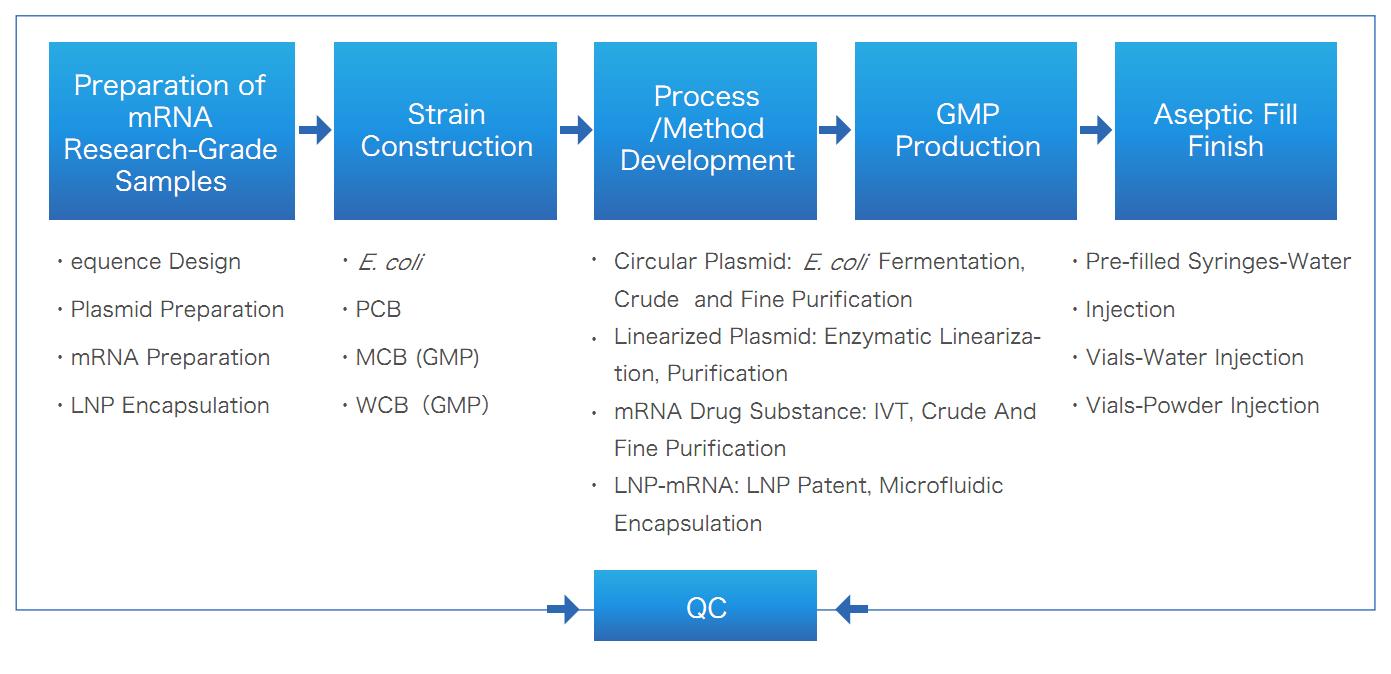
leveransen
| Klasse |
leveransen |
Spesifikasjon |
Applikasjoner |
| ikke-GMP |
Legemiddelstoff, mRNA |
0.1~10 mg (mRNA) |
Preklinisk forskning som celletransfeksjon, Analytisk metodeutvikling, Pre-stabilitetsstudier, Formuleringsutvikling |
| Medikamentprodukt, LNP-mRNA |
| GMP, Sterilitet |
Legemiddelstoff, mRNA |
10 mg~70 g |
Undersøkende nytt medikament (IND), autorisasjon for klinisk utprøving (CTA), forsyning av kliniske forsøk, søknad om biologisk lisens (BLA), Kommersiell forsyning |
| Medikamentprodukt, LNP-mRNA |
5000 hetteglass eller ferdigfylte sprøyter/ampuller |
Yaohais mRNA CRDMO-tjeneste, som dekker hele livssyklusen til mRNA
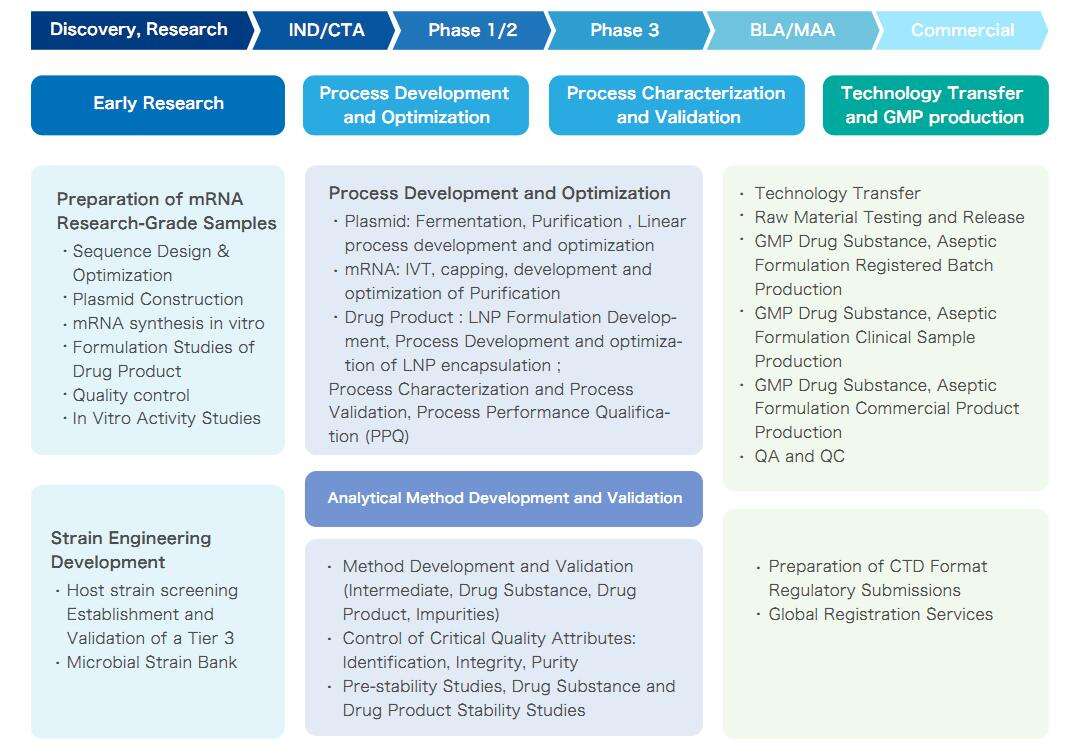
Plattformfunksjoner
Plasmid DNA-plattform
- Flere 7L gjæringssystemer, dyrefrie gjennom hele prosessen
- Tydelig sporbarhet av plasmider og vertsbakterier, uten deklarasjonshindringer
- Utbyttet av plasmid som inneholder poly A som overstiger 500 mg/L
- Poly A tapsrate mindre enn 5 bp
- Supercoiled plasmidandel større enn 90%; utvinningsgrad over 55 %
- Lineariseringseffektivitet over 99 %; linearisert plasmidgjenvinningshastighet på 90 %
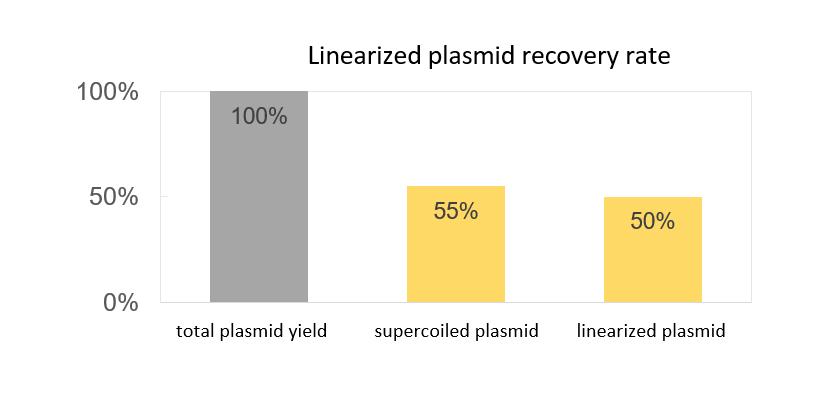
Legemiddelstoff Plattform av mRNA
- Flere 1L reaktorer (GMP)
- Et høyt transkripsjonsforhold på 1:120, muliggjør en skalerbar IVT-prosess
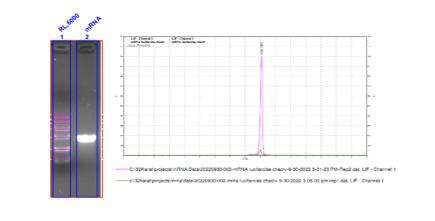
- mRNA-integritet over 98 %
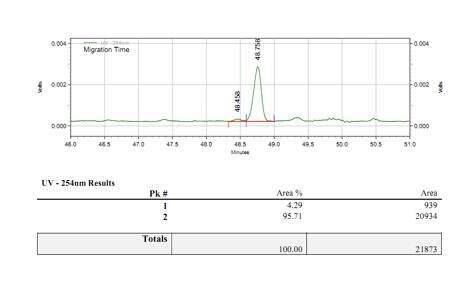
- Stabil avdekningsprosess med en avgrensningsgrad på over 95 %
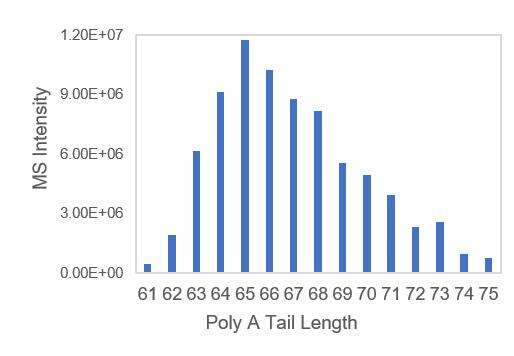
- Transkripsjonsmaler med A-haler, sikrer jevn fordeling av poly A-haler.
LNP-innkapslingsplattform
- LNP patentteknologi autorisert av våre partnere for å sikre unngåelse av patenttvister for våre kunder.



(Våre partnere)
- Bruker en svært allsidig mikrofluidisk innkapslingsprosess, som oppnår en innkapslingseffektivitet på over 95 %.
- LNP-partikkelstørrelse er innenfor 80-100 nm, med en lav polydispersitetsindeks (PDI) på 0.05, noe som indikerer en jevn fordeling av partikkelstørrelser.
- LNP-partikler viser en svak ladning, med et Zeta-potensial på omtrent -2.18 mV.
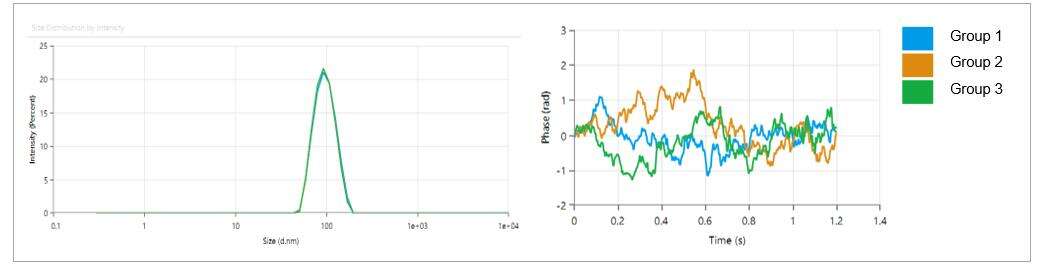
| Testing av vare |
Testmetode |
Testresultat |
| Innkapslingseffektivitet |
Ribogreen |
92.7% |
| Partikkelstørrelse |
Malvern |
92.07 nm |
| PDI |
Malvern |
0.05 |
| Zeta |
Malvern |
-2.18 mV |
Metodeutviklingsplattform
Vi tilbyr en omfattende metodeutviklingsplattform for å analysere sirkulære og lineariserte plasmider, mRNA-råmaterialer og ferdige LNP-mRNA-produkter. Analysen vår dekker en rekke parametere, som integritet, renhet, kapslingseffektivitet, poly A-fordeling, innkapslingseffektivitet, partikkelstørrelse, LNP-komponenter og ulike prosessrester (HCP, HCD, HCR, dsRNA, antibiotika, DNase I, T7 RNA polymerase, vaccinia-kappingsenzym, 2-O-metyltransferase, etc.).
Delmetoder demonstreres som følger:
Påvisning av mRNA-integritet (kapillærelektroforese)
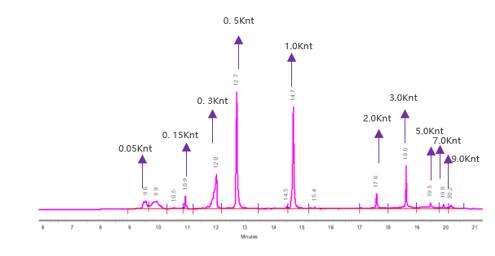
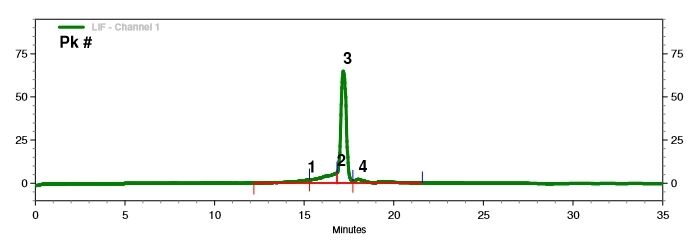
Vi har utviklet optimale separasjonsforhold for nøyaktig å skille mRNA-molekyler av varierende lengde.
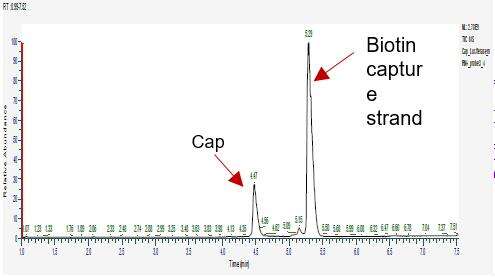
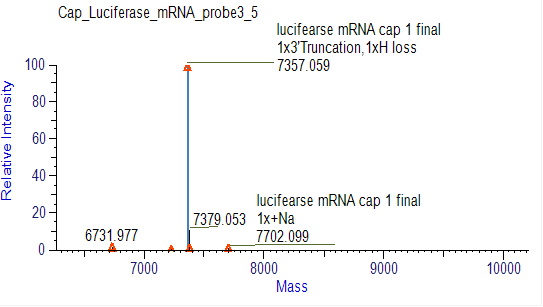
Påvisning av mRNA-dekningseffektivitet (LC-MS)
Vi har utviklet egnede forhold for 5'-endespalting og separasjon av 5'-endeoligonukleotider, noe som muliggjør nøyaktig separasjon av avdekkede og ikke-avdekkede fragmenter.
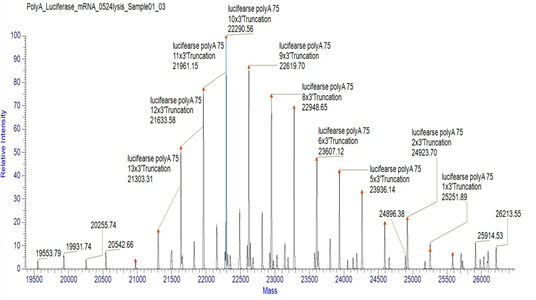
Påvisning av mRNA PolyA egnet halefordeling (LC-MS)
Vi har utviklet egnede forhold for spaltning av 3'-ender og separasjon av 3'-ende-oligonukleotider, som muliggjør presis påvisning av fordelingen av polyA-haler.
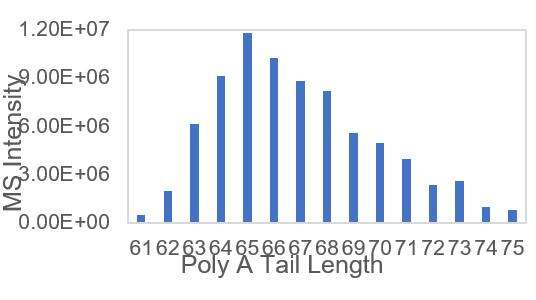
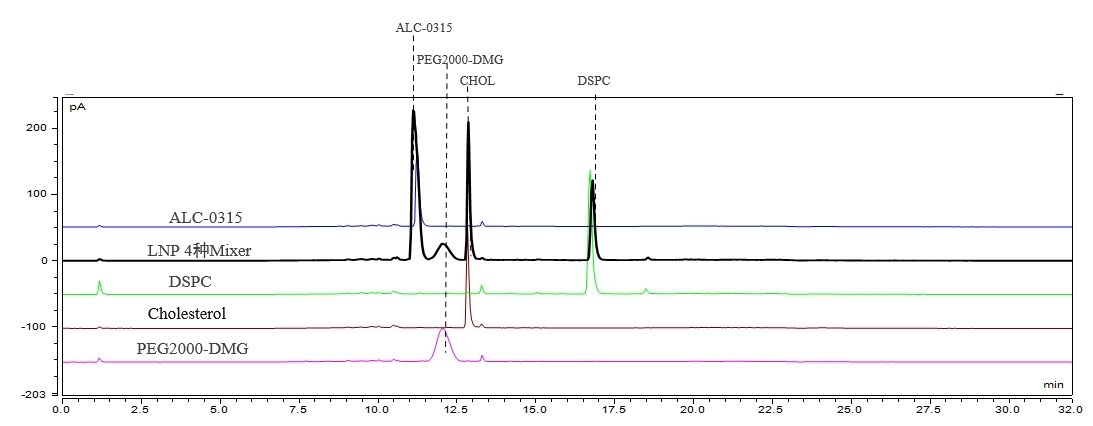
LNP-komponent- og innholdsdeteksjon (HPLC-CAD)
Vi har etablert en egnet kromatografisk metode som oppnår grunnlinjeseparasjon av fire LNP-komponenter. Denne metoden viser utmerket reproduserbarhet.
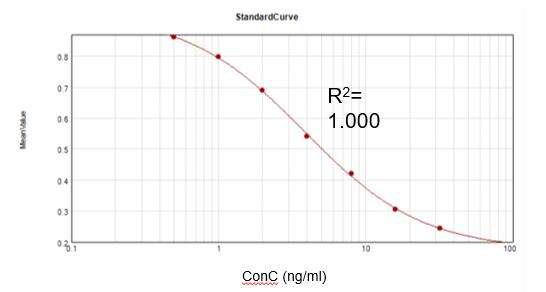
Resterende kanamycinkonsentrasjon (ELISA)
Basert på et kommersielt analysesett oppnådde vi en passende kalibreringskurve (R2 = 1.000) og oppnådde en utvinningsgrad på 104.8 %.
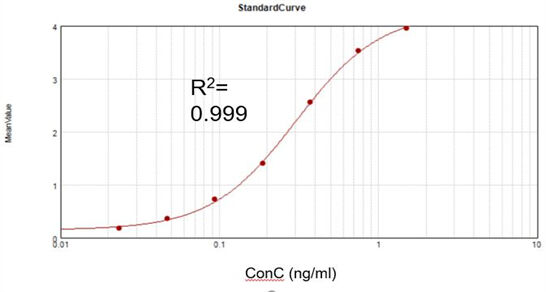
Gjenværende dsRNA-konsentrasjon
Basert på et kommersielt analysesett oppnådde vi en passende tilpasningskalibreringskurve (R2 = 0.999) og oppnådde en utvinningsgrad på 105.5 %.
Resterende T7 RNA-polymerase (Elisa)
Basert på et kommersielt analysesett oppnådde vi en passende tilpasningskalibreringskurve (R2 = 1.000) og oppnådde en utvinningsgrad på 107.9 %.
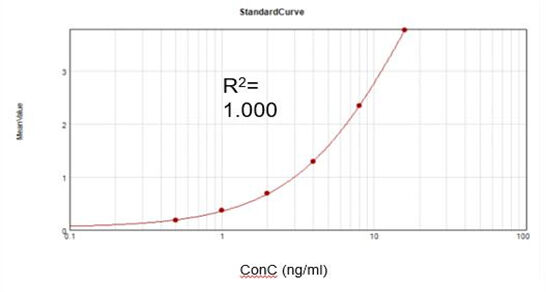
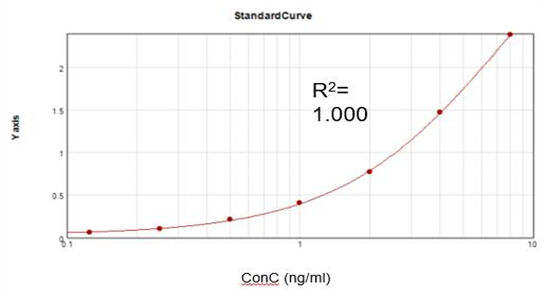
Residual Vaccinia Virus Capping Enzyme (ELISA)
Basert på et kommersielt analysesett oppnådde vi en passende tilpasningskalibreringskurve (R2 = 1.000) og oppnådde en utvinningsgrad på 92 %.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NEI
NEI
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN






















