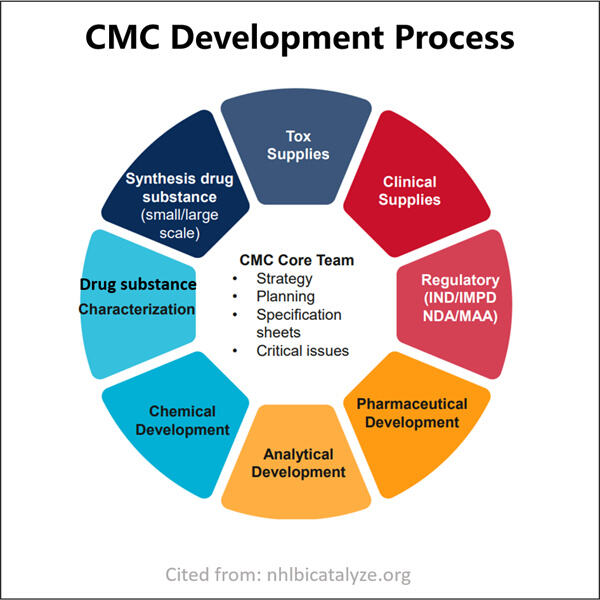
CMC ย่อมาจาก Chemistry, Fabricating & Control องค์ประกอบนี้อาจเป็นส่วนสำคัญของกระบวนการจัดการสารระงับสำหรับยาใหม่ มันบอกให้คุณทราบว่ายาถูกสร้างขึ้นอย่างไรและได้รับการทดสอบอย่างไรเพื่อให้มั่นใจว่ามันเป็นทางเลือกการรักษาที่ปลอดภัยและมีคุณภาพสูงสำหรับผู้ที่จะใช้ยา การเข้าใจเกี่ยวกับ Yaohai CMC Explanatory การทดสอบประสิทธิภาพการปิดห่วง MRNA สำหรับ Plasmid DNA อาจช่วยให้มุมมองใหม่เกี่ยวกับวิธีที่บริษัทต่างๆ รับรองความเชื่อถือในผลิตภัณฑ์ของพวกเขา
มีกฎระเบียบที่ละเอียดอ่อนสำหรับการเสนอขายยา บริษัทจำเป็นต้องแสดงให้เห็นว่ายาถูกพัฒนามาอย่างดีและเหมาะสมสำหรับคุณ FDA ซึ่งย่อมาจาก Nourishment and Medicate Organization มีแนวทางในการเตรียมและการยื่นคำขออนุมัติยา กฎเหล่านี้ปกป้องสุขภาพและความปลอดภัยของประชาชน และรับประกันว่ามียาที่ปลอดภัยเท่านั้นที่สามารถวางตลาดได้

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN