Het ontwerprichtlijn van bacteriële vector (live bacteriële vector) vaccins is om afgeschuwdde padogenen of symbiotische bacteriën te modifieren op basis van genetische technologie om doelwitantigenen te leveren en het immuunsysteem van het lichaam te activeren. Het grootste voordeel van live bacteriële vectoren is dat ze een breed scala aan humeurale immuniteit en celmatige immuniteit kunnen stimuleren. De ontwikkelingsrichting van bacteriële vectorvaccins omvat de preventie van infectieuze ziekten en de behandeling van tumoren.
Yaohai Bio-Pharma heeft meer dan tien jaar ervaring in microbiële CDMO. We hebben een GMP-werkplaats met Biologische Veiligheidsniveau 1 (BSL-1) en Biologische Veiligheidsniveau 2 (BSL-2) opgezet, en een volledige oplossing voor CDMO van microbiële vectorvaccins gelanceerd, die reikt van de ontwikkeling van microbiële stammen tot GMP-productie. Op basis van de aangepaste behoeften van klanten bieden we klanten bacteriële lichamen (DS, API) of levende bacteriële geneesmiddelen (DP) aan die voldoen aan kwaliteitsnormen, evenals GMP-productierecords en testrapporten.
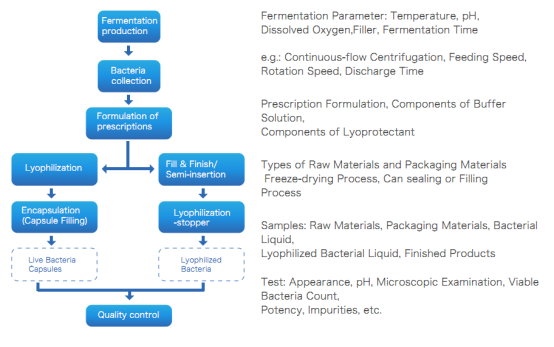
Productieproces van Microbiële Vectorvaccins
Microbiële vectorvaccins zijn ook levende bacteriële preparaten, en hun bereidingsproces komt overeen met het [verzwaktingsproces van levende vaccins].
Leveranties
|
Kwaliteit
|
Leveranties
|
Specificatie
|
Toepassingen
|
|
GMP, BSL-1/BSL-2
|
Bacteriële Cel (DS, drug substance)
|
Bacteriële suspensie
|
Investigational new drug (IND),
Clinical trial authorisation (CTA),
Klinische proefvoorziening,
Biologische licensaanvraag (BLA),
Commerciële voorziening
|
|
Gedroogde bacteriële cel
|
|
Levende bacterie (DP, geneesmiddel)
|
Flessen (vloeistof)
|
|
Flessen (lyofilisate)
|
|
Andere doservormen
|

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN


