Die Bedeutung der Entwicklung des Nachbearbeitungsprozesses (DSP)
Das gesamte Fermentat enthält das Zielprotein oder Plasmid sowie produktspezifische und prozessbezogene Verunreinigungen, z. B. Aggregate, mikrobielle Zellsubstrate, Host Cell Proteins (HCP), Host Cell DNA (HCD), Endotoxine und Antibiotika.
Daher ist es entscheidend, einen effizienten DSP- und Reinformationsprozess zu entwickeln, um bestimmte Verunreinigungen zu entfernen und ein hochreines und hohe Qualität aufweisendes Wirkstoff zu produzieren. Darüber hinaus kann die Optimierung des Reinformationsprozesses helfen, die Produktrückgewinnung zu erhöhen, Kosten zu senken und die Prozessskalierbarkeit und -wiederholbarkeit zu verbessern.
Schlüsselwörter: Prozessentwicklung, Optimierung und Validierung, Reinigungsprozess, Chromatographie, Beseitigung von Verunreinigungen, HCP-Entfernung, HCD-Beseitigung, Endotoxin-Entfernung, Protein-Denaturierung und -refolding, VLP-Assembly, Konjugation
Anwendung: Biopharmazeutische Industrie, Humane Medizin, Tiermedizin, Impfstoffe, rekombinante Makromoleküle, rekombinante Biologika, biologische Reagenzien
DSP Lösungen von Yaohai Bio-Pharma
Wir haben umfangreiche Erfahrung in der Isolierung von Zielproteinen oder Plasmiden aus komplexen Matrizen durch die Entwicklung und Optimierung des nachgelagerten Reinigungsprozesses. Es gibt verschiedene Arten von Einzeloperationen, die für die Reinigung von Biologika geeignet sind, einschließlich Zentrifugation, Filtration, Homogenisierung, alkalische Lyse, Ultrafiltration, Präzipation, Protein-Denaturierung und -refolding, Chromatographie usw.
Unsere verfügbaren Reinigungsentwicklungsleistungen umfassen:
- Entwicklung des gesamten Reinigungsprozesses von der Zell- oder Sumpfsammlung bis zum finalen Wirkstoff.
- Optimierung des Reinigungsprozesses auf Basis von produktspezifischen und prozessbezogenen Verunreinigungen zur Steigerung der Produktqualität und -sicherheit, z. B. HCP, HCD, Endotoxin.
- Definition und Optimierung von Schlüsselparametern in einer oder mehreren Einzeloperationen, einschließlich Zelllyse, tangentialer Fließfiltration, Resinzusammenstellung, Chromatographie, Proteindenaturierung und -refaltung usw.
- Optimierung des Prozesses hinsichtlich Qualität, Ausbeute, Rückgewinnung, Kosten und Skalierbarkeit.
- Validierung des nachgelagerten Reinigungsprozesses.
- Risikobasierende Bewertung des Parameterbereichs und Versuchsplanung (DoE) in der Prozessmodellierung.
Service Details
Standardisierte Proteinpurifikations- oder Plasmidpurifikationsplattformen basieren auf mehreren rohen Purifikationsschritten und weniger als 4 Chromatographieschritten, einschließlich Aufnahme, Zwischenreinigung und Polieren.
| Service Details |
Einzeloperationen |
Parameter |
| Rohreinigung |
Zentrifugation |
Drehzahl, Zeit |
| Hochdruck-Homogenisierung |
Gesamte Feststoffmenge, Druck, Zyklen |
| Kontinuierliche Alkalische Lysierung |
Verhältnis von Wiederaufgehobenen Zellen zu Lysat-Lösung, Lysierungszeit |
| Tangentialflussfiltration |
Membranmaterial und Porengröße, Durchflussrate des Anströmmediums, Transmembrandruck (TMP), Verhältnis von Filtratvolumen zur Membranfläche |
| Präzipation |
Art und Konzentration des Präzipitans, Zusatzstoff, pH, Temperatur, Zeit |
| Denaturierung und Refolding |
Einschlusskörper-Protein-Solubilisierung |
Denaturierende Konzentration (z. B. Urea, Guanidin-HCl, stark ionisches Waschmittel), Waschmittel (z. B. Natriumlaurylsulfat, SDS), Reduktionsmittel (z. B. Dithiothreitol, DTT), Chelatbildner (Ethylenediamintetraessigsäure, EDTA), Temperatur, Zeit |
| Proteinrefolding |
Refolding-Methoden (Verdünnung, Dialyse oder SEC-Refolding), Proteinkonzentrationen, Puffern, pH, Temperatur, Zeit, Oxidations- und Reduktionsmittel (z. B. Glutathion, GSH/ Oxidiertes Glutathion, GSSH, DTT/GSSH, Cystein/Cystin), Kleinsmoleküladditive (L-Arginin, Urea, Guanidin/HCl und Waschmittel) |
| Fangphase, Zwischenreinigung und Schliff |
AC (Affinitätschromatographie) |
Verschiedene Arten von Chromatographieresin/Spalte (z. B. AC, IEX, HIC, SEC, RPC, MMC), Spaltenlänge und -durchmesser, Pufferzusammensetzung, Injektionsvolumen, Zusammensetzung der mobile Phase (Adsorption und Desorption), pH, Durchflussrate, Bindungs-, Wasch- und Elutionsbedingungen. |
| IEX (Anionen- oder Kationenaustauschchromatographie) |
| HIC (Hydrophobe Wechselwirkungschromatographie) |
| Entsalzung und/oder Größenexklusionschromatographie (SEC) |
| RPC (Reversed Phase Chromatographie) |
| MMC, Mixed Mode Chromatographie |
Fallstudie
Fall 1
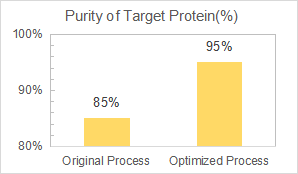
Wir wurden beauftragt, den nachgelagerten Reinigungsprozess zu entwickeln und zu optimieren, um den Proteingehalt von 85 % auf 90 % zu erhöhen, während wir die Chromatographieschritte reduzieren.
Yaohai hat einen robusten und skalierbaren Reinigungsprozess mit drei Chromatographieschritten für das Zielprotein, ein bakterielles Allergen, geliefert. Die endgültige Reinhalt erreichte 95 %.
Fall 2
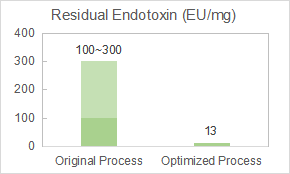
Yaohai wurde von unserem Kunden beauftragt, den Endotoxin-Entfernung-Prozess des Virenartikel-(VLP)-Impfstoffs zu optimieren.
Unser Team optimierte die Chromatographieparameter und bereitete eine Arzneistoffsubstanz mit einer Reinheit von 98 % und einem Endotoxingehalt von 12,8 EU/mg vor.
Unsere Erfahrungen
- Wir sind in die Entwicklung und Herstellung verschiedener großer Moleküle eingebunden, darunter rekombinante Subeinheitsimpfstoffe, VLPs, Hormone (Insulin, GLP-1, Wachstums-hormon), Cytokine (Interleukin-2/IL-2, IL-15, IL-21), Wachstumsfaktoren (EGF, FGF, NGF), Nanobody/Einzel-domänige Antikörper (sdAbs), Enzyme usw.
Ausrüstung
Wir verwenden die branchenführenden AKTA Pure-, AKTA Avant- und Präparativ-HPLC-Systeme zur Durchführung verschiedener Chromatographiemethoden, einschließlich Affinität, Ionen Austausch, hydrophobe Interaktion, Reverse Phase und Größenexklusionschromatographie.




 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN






