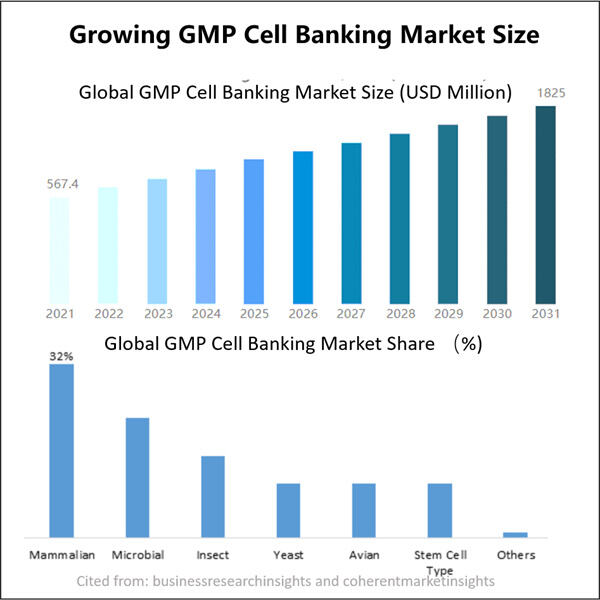
Die Vorteile der GMP-Mikrobiellen Zellbankierung für die Biopharmazeutika-Entwicklung
Was gewinne ich durch die GMP-Mikrobenzellenbank und ihre Nutzung zur Herstellung meines Medikaments? Dies wird effektiv einige Produktionszeit sparen, was einer der wichtigsten Vorteile ist, da es überprüfen kann, ob die Zellen bei mehreren Produktionen konsistent sind. Dies entspricht einer konsistenten Zellqualität von Batch zu Batch innerhalb derselben Batterie. Qualitätskontrolle - ist wichtig, damit das Heilmittel Sie tatsächlich sicher nach Hause begleitet. Mit einer bereitstehenden Zellenbank können Medizinhersteller eine weitere Charge fast sofort produzieren, wenn sie knapp bei ihrer letzten Lieferung werden. Dies dient dazu, sicherzustellen, dass es einen guten und regelmäßigen Bestand an Medikamenten gibt.
Das Unternehmen muss ein patentiertes Verfahren sicherstellen und seine Zellen in einem GMP CMV Antigen Herstellung . Diese Zellen, die benötigt werden, um Medikamente herzustellen, müssen vor Gingivitis und anderen Schadstoffen geschützt werden. Das bedeutet, dass Dinge wie Zellen in einem sauberen und sterilen Raum gezüchtet werden. Das bedeutet auch, dass ihre Umgebung sauber und frei von jeglichen potenziellen Verunreinigungen ist, oder? Die Zellen werden für den Transport und die Erhaltung bei sehr niedrigen Temperaturen kryopräserviert. Auch muss die Zellenbank sicherstellen, dass während der Konservierung nichts Schädliches (wie Bakterien oder Viren, die möglicherweise schädlich sind) in sie gelangt. Solche Sorgfalt zu walten bedeutet, sicherzustellen, dass die Zellen sowohl rein sind als auch bereit zum Einsatz.

 DE
DE
 EN
EN AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN