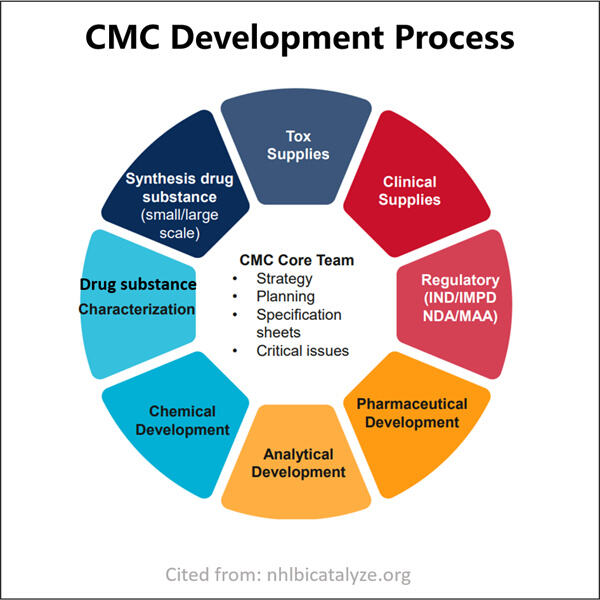
Навигация по техническим требованиям при подаче заявок на лекарства
Это связано с тем, что одним из важнейших базовых принципов медикаментозного одобрения является доказательство того, что продукт является чистым и обладает надежной эффективностью. Поэтому процесс производства лекарств должен быть строго регулируемым, что объясняет, почему некоторые фармацевтические компании с почти одинаковым вариантом s593 совместно работали более десяти лет для выпуска лекарств. Это включает прохождение компаниями пошагового процесса, чтобы убедиться, что конечный продукт также соответствует стандартам высокого качества. Это критично, так как жизни людей зависят от принимаемых ими лекарств.
Компании, подающие заявку на регистрацию лекарства, должны предоставлять данные о том, что входит в состав препарата и как он производится. Это включает химический состав, процесс производства и параметры безопасности. Эти данные также подкрепляются научными доказательствами — демонстрирующими, что препарат является безопасным и эффективным. Чем лучше FDA может понять это протокол ко-транскрипционного закапывания mRNA препарат, тем больше шансов, что они смогут оценить его данные по сравнению с тем, что было использовано в других исследованиях (мета-анализ) const-в другом месте.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN