Neben rekombinanten Subeinheitsimpfstoffen, die auf pathogen-spezifische Antigene abzielen, haben Forscher den Fokus auf Proteine in Tumorzellen oder andere metabolischen Pfadweg-antigenbezogene Ziele gelegt. Diese Antigene können den Körper dazu anregen, spezifische Antikörper zu produzieren, die Tumorzellen töten oder Zielmetabolismuswege blockieren, um das Ziel der Krankheitsbehandlung zu erreichen.
Basierend auf einer umfassenden "Rekombinante Protein-Service-Plattform" kann Yaohai Bio-Pharma Kunden eine einheitliche Lösung von Stammzellentwicklung und Proteinsample-Vorbereitung bis zur GMP-Produktion von rekombinanten Protein-Impfstoffen bieten. Wir können den Serviceprozess nach den individuellen Anforderungen flexibel anpassen und Kunden hochwertige rekombinierte Proteine (Wirkstoff oder Endprodukt) im Bereich von mehreren Gramm oder Zehnern von Gramm sowie Prozessentwicklungs- und GMP-Produktionsdokumentationen und Testberichten liefern.
Yaohai Bio-Pharma bietet eine umfassende CDMO-Lösung für rekombinante Proteine an
Die von Yaohai Bio-Pharma angebotenen Dienstleistungen für rekombinante Protein-/Peptid-Therapieimpfstoffe basieren ebenfalls auf der Plattform für Rekombinante Proteindienstleistungen. Für weitere Details zur Leistung, siehe " CDMO-Lösungen für rekombinierte Subeinheitsimpfstoffe ".
Liefergegenstände
| Qualitätsstufe |
Liefergegenstände |
TECHNISCHE DATEN |
Stichprobenanwendungen |
| Nicht-GMP |
Wirkstoff |
0,2~10 g |
Präklinische Studien, Analysemethodenentwicklung, Prä-Stabilitätstudien, Formulierungsentwicklung |
| Arzneimittel |
| GMP, Steril |
Wirkstoff |
2~100 g |
Investigational new drug (IND), klinische Versuchserlaubnis (CTA), Klinische Versorgung, Kommerzielle Versorgung |
| Arzneimittel |
20.000 Ampullen (flüssig oder lyophylisert), Präfüllspritzen oder Kartuschen |
Fallstudie
| Typen |
Kundenbedarf |
Liefergegenstände |
| Recombinant Protein Therapeutic Impfstoff |
Technologietransfer-Risiken kontrollieren und einen stabilen Produktionsprozess für das Wirkstoff erhalten; Mehrere Gramm rekombinanter Proteins-Wirkstoff liefern; Sicherstellen, dass alle Produktionsaktivitäten den GMP-Vorschriften entsprechen. |
• Rekombinantes Eiweißmedikament, das den Qualitätsstandards entspricht.
• COA des Medikamentsubstanz, Prozessspezifikationen, Qualitätsstandards, Produktionsaufzeichnungen und andere Dokumente, die vollständig den GMP-Richtlinien entsprechen
|
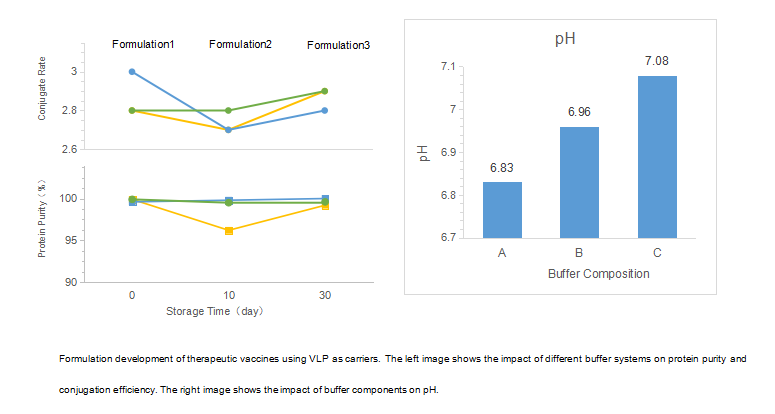
| Therapeutisches Vakzin mit VLP als Träger |
Medikamentensubstanz: Koppelung von Antigen-VLP-Trägerprotein wird in der GMP-Werkstatt durchgeführt. Medikamentenprodukt: Formulierungsentwicklung und steriles Füllen. |
• Bereitstellung einer stabilen Formulierung der Medikamentensubstanz und Medikamentenformulierung (einschließlich Adjuvanten) sowie eines skalierbaren Medikamentenprozesses. • Koppelungsproduktion ist im Gange |
| Verwandte Lösungen: CDMO-Lösungen für Trägerproteine |

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN


