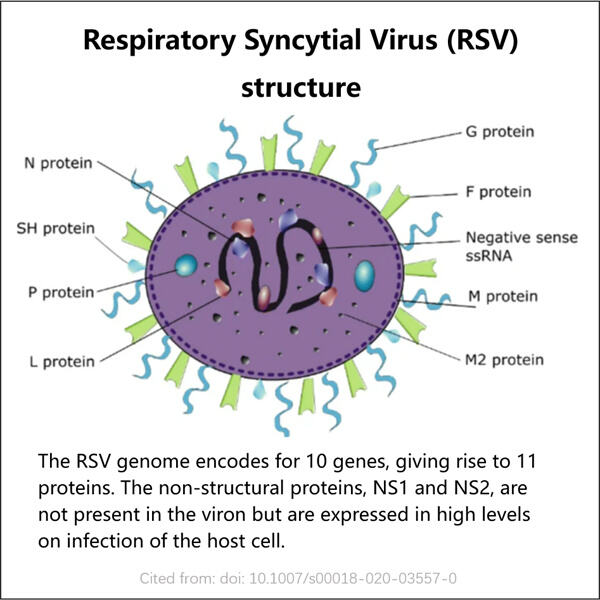
Derfor forstår vi i Yaohai behovet af GMP RSV G Protein Produktion for os. Det giver os mulighed for at verificere, at vores produkter er både sikre og af høj kvalitet. Hvad betyder GMP for RSV G Protein Produktion? Vi vil drøfte, hvordan vi definerer GMP eller god produktionsskik, og de forskellige strategier, vi anvender for at opnå fremragende kvalitet på vores produkter i efterfølgende afsnit.
Forskellige lande har de forskellige standarder For eksempel: *GMP: God Produktionsskik. Dette er retningslinjerne, vi bruger for at producere et sikkert og effektivt RSV G Protein. Et af de meget vigtige produkter er RSV G Protein, som hjælper folk, der er syge på grund af en virus kaldet respiratorisk syncytialvirus eller RSV. AAV-plasmidproduktion truslen kan være særlig alvorlig for spædbørn, små børn og ældre mennesker. Derfor er det af udmærket betydning, at den RSV G-protein, vi leverer, både er sikker og egnet til formålet.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN