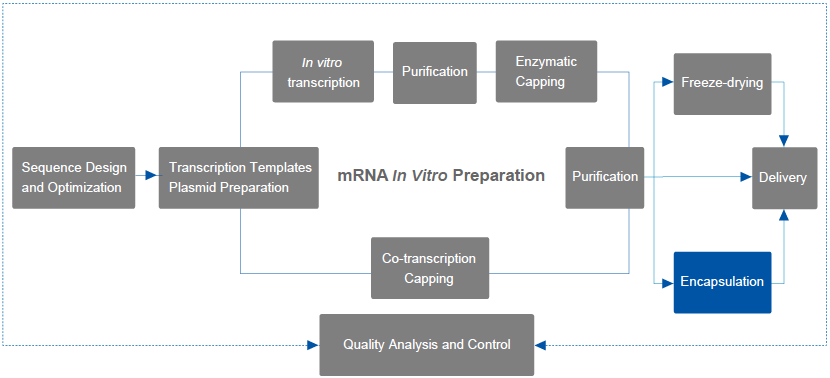
Grundlaget for indkapsling er design og udvikling af leverance-systemet. Et godt design på leverance-systemet giver mRNA-molekyler mulighed for at komme ind i kroppen uden at blive nedbrydt af RNase, og derefter effektivt leveres til målstaden, krydse cellemembranen og frigives intracellelt. Lipidnanopartikler (LNPs) er de optimale leverance-systemer, der findes, med fordele i forhold til indkapsling, levering og sikkerhed sammenlignet med andre leverance-systemer. LNPs med nukleinsyrefragmenter slukkes let op i cellerne og danner intracellelige legemer. Når de er inde i cellen, gør den syreholdige miljø i det intracellelige legeme lipidens ioniserede hoved protoneret og positivt ladet, hvilket fuser med det indre membran af det intracellelige legeme og frigiver den målrettede nukleinsyre i cellen til virkning.
Yaohai Bio-Pharma mRNA service udvider konstant sine muligheder, og kan nu tilbyde en mRNA-LNP indkapslingservice, optimere relevante kritiske procesparametre og forbedre konsistensen og gentageligheden af mRNA-lægemiddelproduktion.
Tjenesteoplysninger
| Service |
Servicedetaljer |
Leveringsperiode (arbejdsdag) |
Leverancer |
| mRNA-LNP indkapsling |
Forberedelse af vandfase (mRNA) og fedtfase |
2 |
mRNA-LNP lægemiddelprodukt (DP) |
| Microfluidic enhedsblanding |
| Ultrafiltrationskoncentration |
1 |
| Steriliséringsfiltrering |
| mRNA-LNP kvalitetskontrol |
Indkapslings-effektivitet |
1 |
Prøvesedling |
| Partikelstørrelse og fordelingsdetektering |
| Overflade ladingsdetektering |
| mRNA-LNP udtryksvalidering |
5-7 |
Vores træk
Hurtig synteses hastighed, høj effektivitet af R&D og forudoptimerede løsninger til rådighed.
mRNA-LNP indkapslingsrate kan nå mere end 90%.
Ved at ændre strømningen af væsker og forholdet, kontrolleres størrelsen på LNP partikler mellem 80 og 100nm, og partikelstørrelsesfordelingen er ensartet (PDI<0.10).
mRNA-LNP bekræftes ved in vitro celleudtrykning og kan effektivt udtrykke det målprotein.
Case studie
Med hjælp fra Yaohai Bio-Pharmas mikrofluidisk indpakningsplatform optimerede vi mRNA-indpakningsbetingelserne, herunder forholdet mellem hver enkelt komponent i LNP, forholdet mellem vandfase og organisk fase samt strømningen af hver mikrofluidisk fase. Partikelstørrelsen og partikelstørrelsesfordelingen af den færdige mRNA-LNP blev derefter undersøgt.
Eksperimentelle resultater viser, at gennem formulering og procesoptimering kontrollerer vi LNP-partikelstørrelsen til 80~100nm, og spredningskoefficienten (PDI) er 0.043, hvilket angiver, at LNP-størrelsesfordelingen er ensartet.
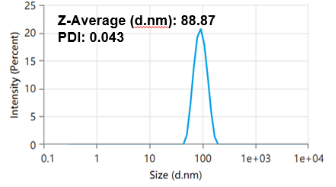
Analyse af et mRNA-LNP-prøveeksemplar

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN