Nasveti in triki
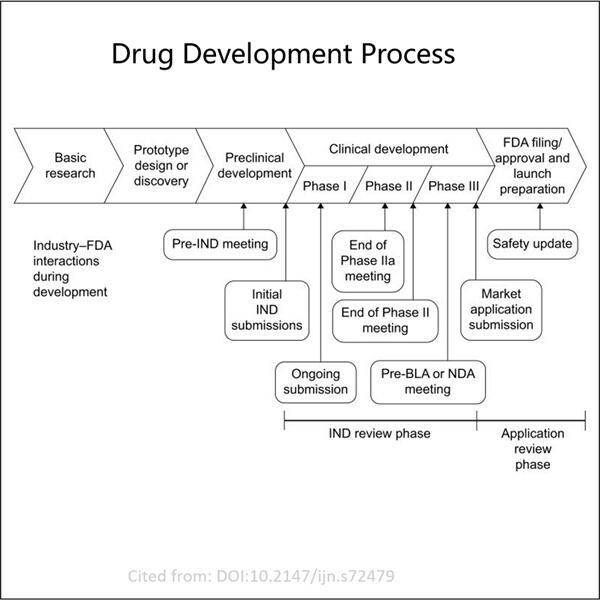
Vendar pa je zahteva za BLA malo bolj zapletena. Preden lahko podjetje zahteva dovoljenje, mora že biti preizkusilo drogo na ljudih, da pokaže, da je varna in učinkovita. To zahteva, da podjetje zbrane velike količine podatkov in informacij iz izvedenih testov. Aplikacija BLA se loti mnogo več konkretnih točk kot aplikacija IND, priprava pa jo traja tradicionalno okoli 1 leta. Traja znatno dlje, ker mora podjetje dokazati, da Visoko učinkovita plazmidna fermentacija da je droga zelo učinkovita in varna za ljudi
Tukaj deli Yaohai nekaj ključnih nasvetov za tiste, ki želijo predložiti uspešno prijavo IND/BLA. Najprej priporočajo sestavitev skupine strokovnjakov, ki lahko mentorjejo drug druge skozi postopek prijave. Ta ekipa naj bi vključevala ljudi, ki razumejo, kako se razvijajo zdravila in pravila, ki jih morajo slediti, ter kdo razumejo, kako deluje klinično raziskovanje. Brez sumnje je, da ima prava ekipa moč spremeniti srečo prijave.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN