Znaczenie rozwoju procesu górnego strumienia
Proces górny (USP), znany również jako proces fermentacji, jest jedną z początkowych faz bioprodukcji górnego strumienia. Proces fermentacji mikrobiologicznej jest kluczowy dla kultury komórkowej o wysokiej gęstości i wyrażania genów obcych, co bezpośrednio wpływa na uzyskiwanie leków biotechnologicznych i ich koszt.
W wczesnych etapach rozwoju leków biotechnologicznych (przedklinicznych lub faz 1/2) nacisk kładziony jest na rozwijanie skalowalnych procesów bez udziału produktów pochodzenia zwierzęcego, zapewniających średnią wydajność i spełniających wszystkie standardy jakości produktu.
W późnych etapach (faza 3 lub komercyjna) skupimy się na wydajności, odporności, skalowalności i powtarzalności, tworząc kosztowo efektywny proces. Aktywności związane z tymi problemami to charakterystyka procesu i badania weryfikacji procesu. W międzyczasie, narzędzia takie jak jakość w projekcie (QbD) i projekt eksperymentów (DoE) są zwykle stosowane.
Słowa kluczowe: rozwój procesu, optymalizacja i weryfikacja, proces fermentacji, fermentacja komórek mikrobiologicznych, fermentacja bakterii, fermentacja drożdży, fermentacja wysokiej gęstości, fermentacja szczepu inżynierowanego
Zastosowanie: przemysł biofarmaceutyczny, medycyna ludzka, medycyna weterynaryjna, szczepionki, rekombinowane wielkie cząsteczki biologiczne, rekombinowane produkty biologiczne, reageny biologiczne
Rozwiązania USP Yaohai Bio-Pharma
Dzięki ponad 10-letniemu doświadczeniu w zakresie fermentacji mikrobiologicznej, Yaohai Bio-Pharma dysponuje kompetencjami niezbędnymi do rozwiązywania wyzwań związanych z procesem fermentacji. Możemy szybko opracować strategie fermentacji wysokiej gęstości dla Escherichia coli (E. coli) sekrecja periplazmatyczna, rozpuszczalne wyrażanie się wewnątrzkomórkowe lub wyrażanie się w postaci ciała inkluzyjnego oraz wyrażanie się zewnętrzne lub wewnętrzne w drodze drożdży.
Nasze dostępne ogólne usługi w zakresie rozwoju fermentacji obejmują:
- Projektowanie procesu fermentacji przeprowadzane w małej skali 7L w trybie podawania dodatkowego pokarmu
- Walidacja trzywsadowego procesu w bioreaktorach o pojemności 7L
- Przeskalowywanie pośredniego procesu do 30L/70L
Możemy elastycznie przeprowadzać optymalizację wielu parametrów, aby osiągnąć pożądaną wydajność lub proporcję, korzystając z metody One-Time-A-Factor (OTAF) lub Design-of-experiments (DoE).
Podstawowe parametry fermentacji wymienione są poniżej:
Skład środka fermentacyjnego bez udziału produktów pochodzenia zwierzęcego
Bez antybiotyków lub nie, objętość nasiennika
Temperatura wzrostu, pH, Poziom tlenku rozpuszczony (DO)
Tryb karmienia (np., fed-batch)
Stężenie induktora (np., IPTG, metanol), Punkt indukcji (mokra masa komórek/OD600),
Temperatura indukcji, Czas indukcji
itd.
Szczegóły usług
| Usługi |
Przepływ procesu |
| Kultywacja w flasze trzęsionej (500 mL) |
Przygotowanie środowiska bez substancji pochodzenia zwierzęcego → Kultywacja nasion mikrobowych → Kultywacja w szynku → Indukcja → Zbiorstwo |
| Kultywacja w fermenterze (7 L) |
Przygotowanie środowiska bez substancji pochodzenia zwierzęcego → Kultywacja nasion mikrobowych → Wysokozańska fermentacja komórek w bioreaktorze o objętości 7L → Indukcja → Zbiorstwo |
| Kontrola jakości białek/peptydów |
Wstępną obróbkę wyrażenia rozpuszczalnego wewnątrzkomórkowego: Pobór i rezyfikacja komórek mikrobowych → Ultradźwiękowe zmielenie → Usuwanie szczątków komórkowych → Surowy ekstrakt Wyrażenie białek w inclusion bodies: Pobór i rezyfikacja komórek mikrobowych → Ultradźwiękowe zmielenie → Przygotowanie inclusion bodies → Surowy ekstrakt Wyrażenie rozpuszczalne pozakomórkowe: Zbieranie surowca kultury (supernatant) → Koncentracja i wymiana buforu → Surowy ekstrakt Analiza jakości Surowy ekstrakt jako próba → Analiza białka docelowego za pomocą SDS PAGE lub western blotting (WB) |
| Kontrola jakości plazmidów |
Wstępna obróbka i analiza jakości Ekstrakcja plazmidów → Analiza DNA przez elektroforezę w gelu agarowym |
Badanie przypadków
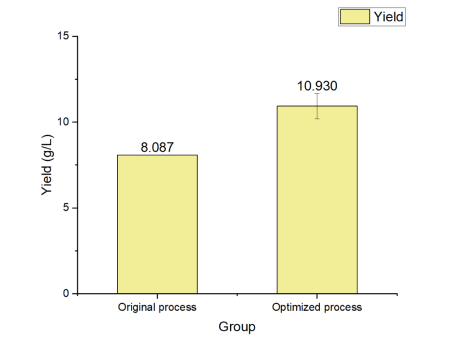
Otrzymaliśmy zlecenie od naszego klienta na zwiększenie wydajności produkcji peptydu hormonowego z 8 g/L do 10 g/L.
Na podstawie Pełnego Projektu Faktorialnego i Projektu Powierzchni Odpowiedzi w narzędziach DoE, szybko zidentyfikowaliśmy i zoptymalizowaliśmy kluczowe parametry fermentacji. W warunkach zoptymalizowanego procesu fermentacji o wysokiej gęstości komórkowej poziom ekspresji wzrósł do 10 g/L.
Nasze doświadczenia
- Pracowaliśmy z różnymi rodzajami mikrobiologicznych gospodarzy, np. E. coli DH5α, TOP10, Trans10, BL21; Pichia pastoris (P. pastoris) SMD1168H, X-33, GS115, PichiaPink strain1/2/3/4; Saccharomyces cerevisiae (S. cerevisiae) i Hansenula polymorpha (H. polymorpha) .
- Mamy doświadczenie w E. coli sekrecji periplazmatycznej, ekspresji rozpuszczalnej i ciał inkluzyjnych oraz ekspresji wewnątrzkomórkowej lub zewnętrznej drożdży. Zwyrodnienie ciała inkluzyjnego wynosi do 10 g/L, podczas gdy wydajność białek rozpuszczalnych mieści się w zakresie od 0,5 do 15 g/L.
- Byliśmy zaangażowani w rozwój i produkcję różnych dużych cząsteczek, w tym szczepionek rekombinacyjnych podjednostkowych, cząstek podobnych do wirusa (VLP), hormonów (insulin, GLP-1, hormon wzrostu), cytokin (Interleukin-2/IL-2, IL-15, IL-21), czynników wzrostu (EGF, FGF, NGF), nanociałek / pojedynczo-domenowych przeciwciał (sdAbs), enzymów itp.
- Sprzęt
7L*16 System fermentacji

Cedex Bio Analyzer, Analizator bioprocesy


 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN




