Optymalizacja czyszczenia sdAb w celu zwiększenia przepustowości
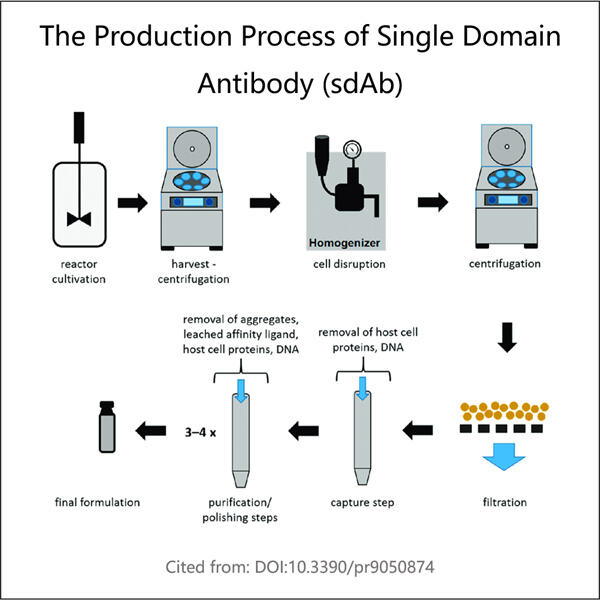
Po zakończeniu produkcji sdAbs przez komórki, Yaohai musi je wydobyć z komórek. To osiąga się za pomocą procedury oczyszczania. Jest to ważny krok oczyszczania, aby upewnić się, że w leku znajdują się wyłącznie sdAbs, a nie pozostałe składniki komórkowe. Jest to kluczowe, ponieważ chcemy, aby lek był czysty i mocny.
Optymalizacja oczyszczania sdAbs została wykonana przez Yaohai szybkim i inteligentnym sposobem. Możliwość szybkiego oczyszczania sdAbs za pomocą tego podejścia jest istotna. Jest to ważne, ponieważ mogą produkować wiele sdAbs w krótkim czasie. Oznacza to, że mogą produkować lek dla większej liczby osób szybciej, dzięki czemu więcej ludzi poczuje się lepiej wcześniej.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN