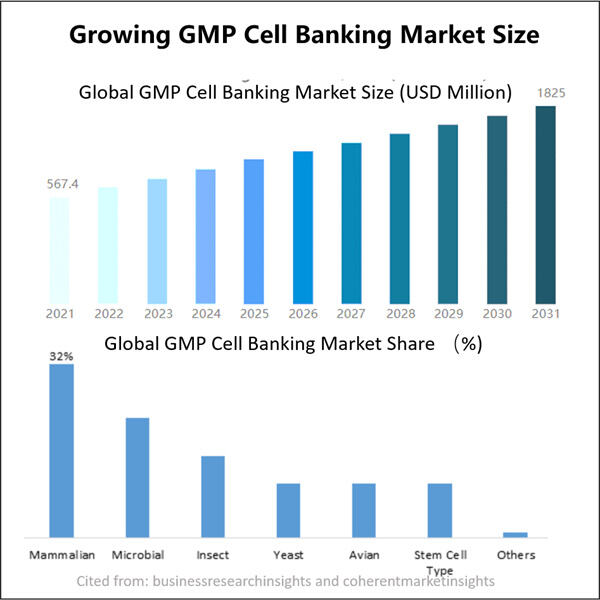
GMP mikrobsete rakubanka eelised biofarmatoodete arendamiseks
Mida saan kasutades GMP mikrobsete rakkubeet ja selle abil oma ravimi valmistamiseks? See majastab tõhusalt mõnda tootmisaega, mis on üks peamisi eeliseid, kuna see võib kontrollida, kas rakud on mitmetes toodangutes ühtlased. See vastab püsivale rakukvaliteedile igas uues seriis samas akus. Kvaliteedikontroll - on oluline, et ravi järgi sulle turvaliselt koju. Rakubanka olemasolul saavad ravimid tootjad toota järgmise seri raaviga peaaegu kohe, kui viimane on lõppenud. See tagab, et ravimeest on piisavalt ja regulaarselt.
Ettevõte peab tagama patenteeritud protseduuri ja hoidma oma rake GMP CMV antogeeni tootmine . Need läbikukkuvad peavad valmistama ravimeid kaitstud olema paremst gingivitsest ja muude kontsentrantide eest. See tähendab, et asjad nagu rakud kasvatatakse puhas ja sterilises ruumis. See tähendab ka seda, et nende keskkond on puhast ja vaba kõigist võimalikest kontsentrantidest, eks? Rakkudeid hoidakse transpordi ja hoidmiseks väga madalatel temperatuuridel krüopreserveerimise teel. Rakubank peab tagama, et rakkude hoidmise ajal ei saa neisse midagi halba (nagu bakteerid või viirused, mis võivad olla ohtlikud). Nii hooldust tegemine tähendab seda, et tagada rakkude puhasus ja valmisolek.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN