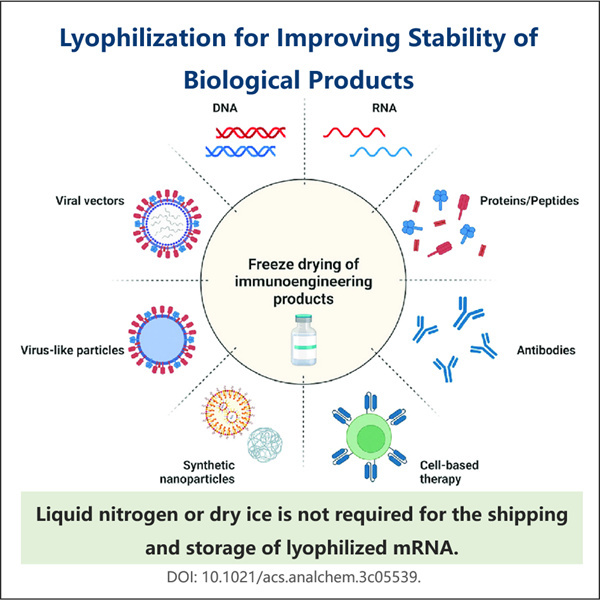
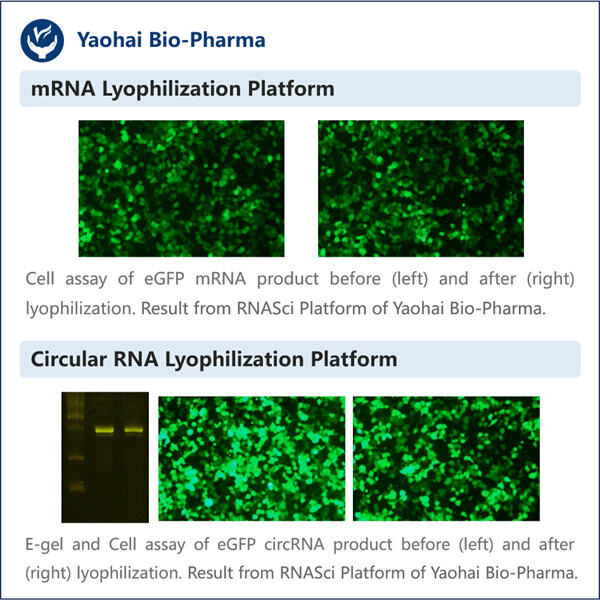
RNA utrzymuje nasze komórki w ruchu lub sprawia, że nadal funkcjonują. To ważne, ponieważ prowadzi do tworzenia długich łańcuchów białek, które pomagają naprawiać uszkodzone tkanki, walkować z chorobami i wzrastać. RNA jest posłańcem, który mówi naszym komórkom, które białka mają budować. Ale RNA jest krucha i łatwo się łamie, gdy spoczywa, podobnie jak délicatny kwiatek może się zwinąć, jeśli nie będzie traktowany z troską. Dlatego musimy uważać na utrzymanie zdrowia i bezpieczeństwa RNA. Można to zrobić poprzez liofilizację. Zapewniamy, że próbki będą miały całą zawartość wody usuniętą dzięki liofilizacji.
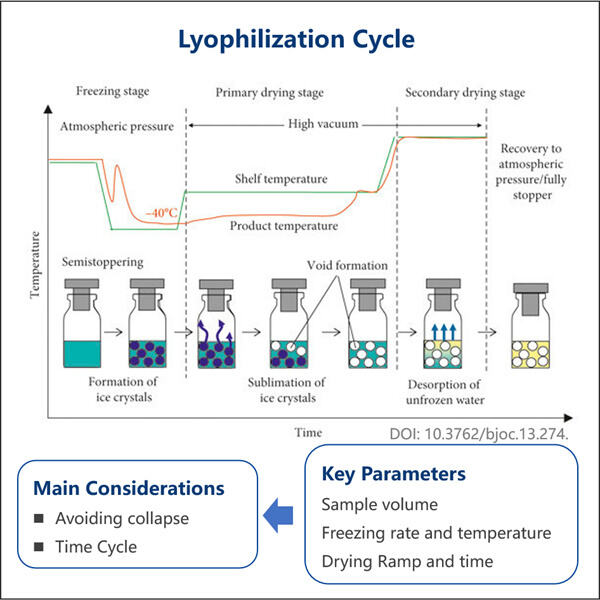
To jakbyś wziął lody i trzymał je w lodówce, ponieważ zaczynają się ochładzać i twardeć, ale gdy tylko wyjmujesz je z temperatury Î 9C lodówki, woda po prostu zanika przez odparowanie. Podobnie ten sposób był dawno używany do konserwacji próbek biologicznych, w tym również RNA. Bardzo niezawodne w unikaniu uszkodzeń RNA, a musimy się upewnić, że dzieje się to dokładnie, jakby te same kroki były powtarzane.

 PL
PL
 EN
EN AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN