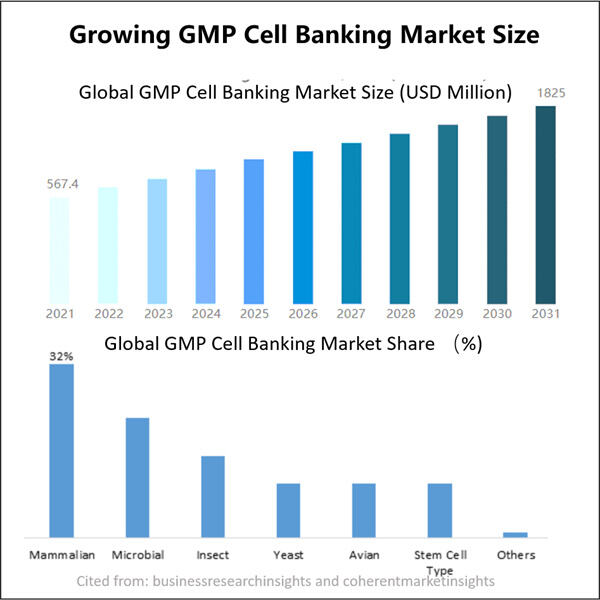
Korzyści wynikające z banku komórek mikrobowych GMP w rozwoju bioprzygotków
Co zyskam dzięki bankowi komórek mikrobowych GMP i jego użyciu do produkcji mojego leku? To skutecznie oszczędza czas produkcyjny, co jest jedną z kluczowych przewag, ponieważ można zweryfikować, czy komórki są spójne w wielu produkcjach. Oznacza to spójną jakość komórek, partia po partii w ramach tego samego zestawu. Kontrola jakości - jest ważna, aby leczenie faktycznie mogło bezpiecznie dotrzeć do pacjenta. Dzięki gotowemu bankowi komórek, producenci leków mogą wyprodukować kolejną partię niemal zaraz po tym, jak zabraknie im ostatniej. Ma to na celu zapewnienie dobrego i regularnego zapasu lekarstw.
Firma musi zagwarantować zapatentowany proces i utrzymywać swoje komórki w Produkcja antygenów CMV GMP . Te komórki, które są potrzebne do produkcji leków, muszą być chronione przed gingiwitą i innymi zanieczyszczeniami. To oznacza, że rzeczy podobne do komórek rosnących w czystym i sterylnym miejscu. To również oznacza, że ich środowisko jest czyste i wolne od jakichkolwiek potencjalnych zanieczyszczeń, prawda? Komórki są kriozachowywane w niskiej temperaturze w celu transportu i zachowania. Bank komórkowy musi również zapewnić, aby podczas przechowywania komórek nic złego (takie jak bakterie lub wirusy, które mogą być szkodliwe) nie dostało się do nich. Taka staranna opieka oznacza zapewnienie, że komórki są zarówno czyste, jak i gotowe do użytku.

 PL
PL
 EN
EN AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN