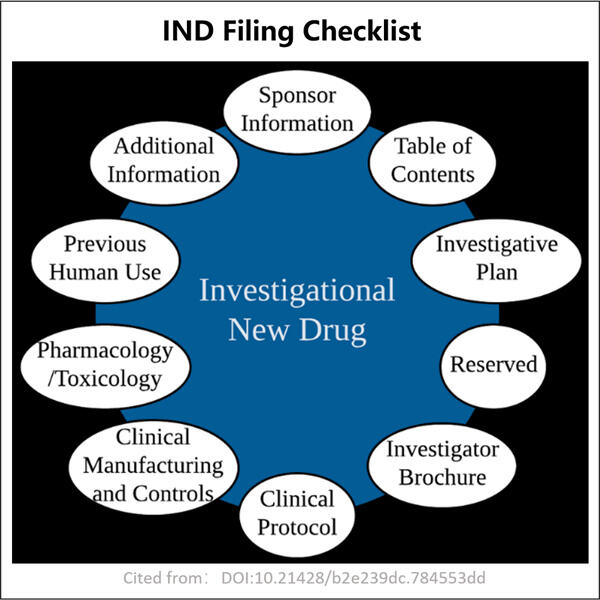
Stellen Sie Genauigkeit und Konformität mit unserer umfassenden Checkliste zum Einreichen von IND- und BLA-Anträgen sicher.
IND- oder BLA-Anträge können langwierig und schwierig zu bearbeiten sein. Mit Yaohais Anleitung einer übersichtlichen Checkliste, der Sie folgen können, werden Fehler reduziert und Sie werden effizienter. Diese Checkliste wurde entwickelt, um bei jedem Schritt der Einreichung so klar und deutlich wie möglich zu sein. HPV-Impfstoff VLP Prozessdefinierung
Die gute Nachricht ist, dass Sie eine vollständige Checkliste haben, mit der Sie sicherstellen können, dass Sie alle Schritte richtig ausführen. Und was noch wichtiger ist: Wir geben für jeden Schritt KLARE ANWEISUNGEN. So wissen Sie ganz einfach, was als Nächstes zu tun ist.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NEIN
NEIN
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN