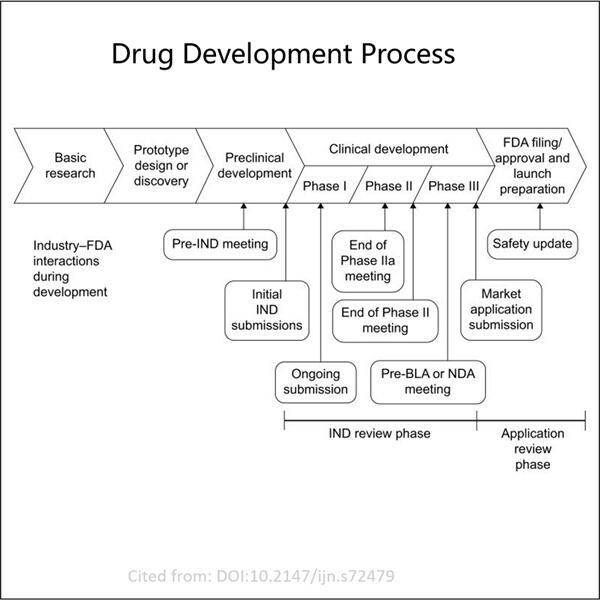
Prilagodba, učinkovitost i isplativost
Yaohai Bio-Pharma ima iskustva u proizvodnji bioloških lijekova dobivenih iz mikroorganizama. Nudimo prilagođena RD rješenja i proizvodnju dok minimaliziramo rizik. Radili smo s različitim metodama, kao što je IND vs BLA, primjena cjepiva (uključujući peptide), faktora rasta, hormona i citokina. Specijalizirali smo se za višestruke mikrobne domaćine, uključujući izvanstanične i intracelularne kvasce (prinos do 15 g/L), periplazmatsku sekreciju bakterija, topiva unutarstanična i inkluzijska tijela (prinos do 10 grama/L). Također imamo BSL-2 fermentacijsku platformu za stvaranje bakterijskih cjepiva. Specijalizirani smo za poboljšanje procesa, povećanje prinosa proizvoda, kao i smanjenje troškova proizvodnje. Imamo učinkovit tehnološki tim koji jamči pravovremenu i kvalitetnu isporuku projekta. To nam omogućuje da vaše ekskluzivne proizvode brže isporučimo na tržište.

 HR
HR
 EN
EN
 AR
AR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NE
NE
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN