La Importancia del Desarrollo del Proceso Aguas Abajo (DSP)
El caldo fermentativo completo contiene la proteína objetivo o el plásmido, así como impurezas relacionadas con el producto y el proceso, por ejemplo, agregados, sustratos celulares microbianos, Proteínas de Células Huésped (HCP), ADN de Células Huésped (HCD), endotoxinas y antibióticos.
Por lo tanto, es fundamental diseñar un DSP eficiente, un proceso de purificación, para eliminar ciertas impurezas y producir una sustancia altamente purificada y de alta calidad. Además, la optimización del proceso de purificación puede ayudar a aumentar la recuperación del producto, reducir costos y mejorar la escalabilidad y reproducibilidad del proceso.
Palabras clave: desarrollo de procesos, optimización y validación, proceso de purificación, cromatografía, eliminación de impurezas, eliminación de HCP, eliminación de HCD, remoción de endotoxinas, denaturación y refoldamiento de proteínas, ensamblaje de VLP, conjugación
Aplicación: Industria biofarmacéutica, medicina humana, medicina animal, vacunas, biológicos recombinantes de gran tamaño, biológicos recombinantes, reagentes biológicos
Soluciones DSP de Yaohai Bio-Pharma
Contamos con amplia experiencia aislado proteínas objetivo o plásmidos de matrices complejas mediante el desarrollo y la optimización del proceso de purificación aguas abajo. Existen diferentes tipos de operaciones unitarias adecuadas para la purificación de biológicos, incluyendo centrifugación, filtración, homogeneización, lisis alcalina, ultrafiltración, precipitación, denaturación y refoldamiento de proteínas, cromatografía, etc.
Nuestros servicios disponibles de desarrollo de purificación incluyen:
- Desarrollo del proceso completo de purificación desde la recolección de células o sobrenadante hasta el ingrediente activo final.
- Optimización del proceso de purificación basado en impurezas relacionadas con el producto y el proceso para aumentar la calidad y seguridad del producto, por ejemplo, HCP, HCD, endotoxina.
- Definición y optimización de parámetros clave en una o varias operaciones unitarias, incluyendo lisis celular, filtración de flujo tangencial, tamizado de resina, cromatografía, denaturación y refoldado de proteínas, etc.
- Optimización del proceso en términos de calidad, rendimiento, recuperación, costo y escalabilidad.
- Validación del proceso de purificación aguas abajo.
- Evaluación basada en riesgos del rango de parámetros y Diseño de Experimentos (DoE) en modelado de procesos.
Detalles del Servicio
Plataformas estandarizadas de purificación de proteínas o plásmidos se basan en múltiples pasos de purificación cruda y menos de 4 pasos de cromatografía, incluyendo captura, purificación intermedia y pulido.
| Detalles del Servicio |
Operaciones Unitarias |
Parámetros |
| Purificación Cruda |
Centrifugación |
Velocidad de Rotación, Tiempo |
| Homogeneización de alta presión |
Contenido total de sólidos, Presión, Ciclos |
| Lisis alcalina continua |
La relación de Células Resuspendidas a la Solución de Lisis, Tiempo de Lisis |
| Filtración de Flujo Tangencial |
Material de la membrana y tamaño de poro, Tasa de flujo de alimentación Presión Transmembrana (TMP), Volumen de filtrado en relación con el área de membrana |
| Precipitación |
Tipo y concentración de precipitante, Aditivo, pH, Temperatura, Tiempo |
| Denaturación y Renaturación |
Solubilización de proteínas de cuerpo de inclusión |
Concentración de denaturante (por ejemplo, Urea, Guanidina HCl, Detergente Iónico Fuerte), Detergentes (por ejemplo, Sodio laurosofato, SDS), Agentes Reductores (por ejemplo, Ditiotreitol, DTT), Agentes quelantes (Ácido etilendiaminotetraacético, EDTA), Temperatura, Tiempo |
| Replegamiento de proteínas |
Métodos de Replegamiento (dilución, dialización o replegamiento por CEC), Concentraciones de Proteína, Buffers, pH, Temperatura, Tiempo, Agentes Oxidantes y Reductores (por ejemplo, Glutationa, GSH/Oxidada Glutationa, GSSH, DTT/GSSH, Cisteína/Cistina), Aditivos de Pequeñas Moléculas (L-arginina, Urea, Guanidina/HCl, y Detergentes) |
| Captura, Purificación Intermedia y Pulido |
CC (Cromatografía por Afinidad) |
Varios tipos de resina/columna de cromatografía (por ejemplo, CC, IEX, HIC, SEC, RPC, MMC), Longitud y Diámetro de la Columna, Composición del Buffer, Volumen de Inyección, Composición de la Fase Móvil (Adsorción y Desorción), pH, Velocidad de Flujo, Condiciones de Enlace, Lavado y Elución. |
| IEX (Cromatografía de Intercambio Aniónico o Catiónico) |
| HIC (Cromatografía de Interacción Hidrofóbica) |
| Desalinización y/o cromatografía de exclusión por tamaño (SEC) |
| CPR (Cromatografía en Fase Inversa) |
| MMC, Cromatografía de modo mixto |
Estudio de Caso
Caso 1
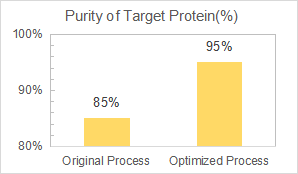
Nos encargan desarrollar y optimizar el proceso de purificación en etapas posteriores para aumentar la pureza de la proteína del 85% al 90% mientras se reducen los pasos de cromatografía.
Yaohai entregó un proceso de purificación robusto y escalable con 3 pasos de cromatografía para la proteína objetivo, una alergia bacteriana. Y la pureza final alcanzó el 95%.
Caso 2
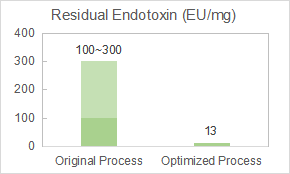
Yaohai fue designado por nuestro cliente para optimizar el proceso de eliminación de endotoxinas de la vacuna de partículas similares a virus (VLP).
Nuestro equipo realizó la optimización de los parámetros de cromatografía y preparó una sustancia farmacéutica con una pureza del 98% y residuos de endotoxinas de 12,8EU/mg.
Nuestras experiencias
- Hemos estado involucrados en el desarrollo y fabricación de varias moléculas grandes, incluidas vacunas de subunidades recombinantes, VLPs, hormonas (insulina, GLP-1, hormona del crecimiento), citocinas (Interleucina-2/IL-2, IL-15, IL-21), factores de crecimiento (EGF, FGF, NGF), nanocuerpos/cuerpos simples (sdAbs), enzimas, etc.
Equipos
Utilizamos los sistemas líderes en la industria AKTA Pure, AKTA Avant y HPLC preparativos para realizar varios métodos de cromatografía, incluidas cromatografías por afinidad, intercambio iónico, interacción hidrofóbica, fase inversa y exclusión por tamaño.




 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN






