יאוהאי יודע הרבה על רפואת הרים. הם פיתחו שני סוגי תוספות חשובים - IND (indole) ו-BLA (blubber). IND הוא קיצור של Investigational New Drug, המשמש כדי לקבל את אישור ה-FDA האמריקאי להetest תרופה חדשה על אנשים. נדרש Biologics License Application (BLA) נדרש נדרש כאשר חברה רוצה למכור תרופה ביולוגית. GMP Semaglutide API הבקשות האלו הן שלבים מכריעים כדי לוודא שתרופות חדשות לבטוחות ויעילות עבור אנשים. מאמר זה ידון כיצד להגיש את שתי הבקשות האלו, והבדלים והדמויות ביניהן.
החברה שברצונה להגיש בקשה ל-IND חייבת תחילה להגיש בקשה מיוחדת למינהל המזון והתרופות (FDA). זה הכרחי מאוד מכיוון שזה יכלול את כל הפרטים החיוניים של התרופה החדשה. הבקשה תועבר עכשיו בפני ה-FDA לביקורת, כאשר החברה מבקשת רשות להתחיל בדיקות על התרופה באנשים. חלק זה של התהליך בדרך כלל לוקח עד 30 ימים. שנית, לאחר שהמידע החסר נשלח ותקבל על ידי ה-FDA - אם הוא יאושר - החברה תוכל להתחיל בבדיקות אנושיות, מה שמייצג צעד גדול בהכנת תרופה חדשה.
עם זאת, הגשת בקשה ל-BLA היא מעט יותר מורכבת. לפני שחברה יכולה להגיש בקשה רשיון, היא חייבת כבר לבנות את התרופה על אנשים כדי להראות שהיא בטוחה ויעילה. זה דורש מהחברה לאסוף כמויות גדולות של נתונים ומידע מהבדיקות שהיא ביצעה. הבקשה ל-BLA נכנסת לפרטיםรายละเอיליות הרבה יותר מאשר הבקשה ל-IND והכנתה לוקחת בערך שנה מסורתית. זה לוקח הרבה יותר זמן כי החברה צריכה להוכיח שה תסיסה של פלזמיד במחזור גבוה תרופה עובדת בצורה מצוינת ואינה מסוכנת לאנשים
כאן, יאוחאי מחלק עצה חיונית לאלו שמחפשים להגיש בקשה מוצלחת של IND / BLA. קודם כל, הם ממליצים להרכיב קבוצה של מקצוענים שיוכלו להדריך אחד את השני דרך תהליך הגשת הבקשה. הקבוצה צריכה לכלול אנשים שמבינים כיצד נפתחות תרופות והחוקים שהם חייבים להישמר בהם ומכירים את אופן פעולתו של מחקר קליני. ללא ספק, להיווצר הקבוצה הנכונה יכולה לשנות את המזל של הבקשה.
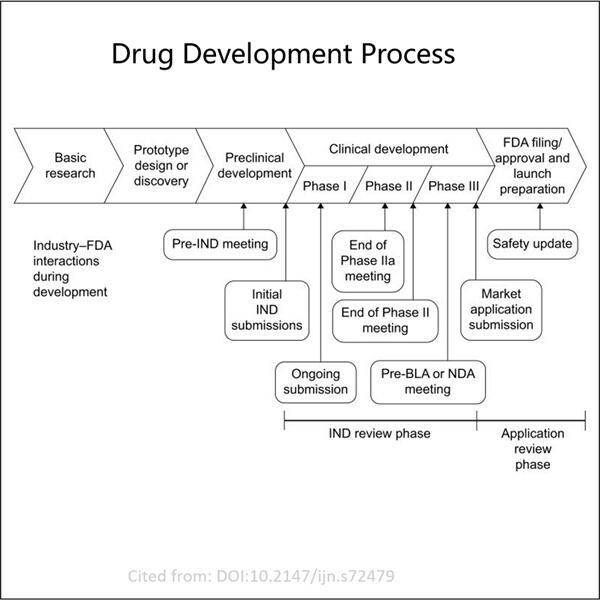
אז, הנה אנחנו הולכים. הבקשה IND מבוססת במקום אחר מאשר BLA ויש להם גם הבדלים גדולים ודמיון מסוים, בואו נראה. ההבדל העיקרי הוא הכמות והאיכות של המידע שהם דורשים. כל מה שהבקשה IND צריכה לעשות הוא לשכנע את ה-FDA שהיא בטוחה להתחיל בבדיקות על בני אדם. מצד שני, בקשה BLA תדרוש מידע מפורט יותר על GMP Semaglutide API ייצור התרופה שלנו, כיצד היא נבדקה, ועקב כך אנו עומדים לסמן אותה לשימוש. לואי: זו תהליך הרבה יותר משלל להגיש את בקשה של BLA.

בנוסף, יאוהי הדגיש כמה מההישגים הטובים ביותר של חברות IND/BLA. ההישג הבא הוא להתקיים עם כל דרישות השיפוט. זה אומר להבין את תקנות ה-FDA וכן הנחיות. למשל, יאוהי מאמין שחברות צריכות לצאת כדי להשתתף בכל מיני כינוסים וכנסים על מנת להבין את התקנות האחרונות. הוא ציין שכשמאכרים נוכחים, החברות צריכות להיות מסוגלות להימנע מכל טעות ולשפר את סיכוייהן להגיש בקשה טובה.

יאוהאי ערך מספר ראיונות מפורטים עם דמויות משני הצדדים 'איך קובעים את קובץ ה-IND וה-BLA' דיברתי. ד"ר סמית, אקסPERT בנושא ענייני שיפוט, ממליץ להתחיל את ייצור מונומר VHH תהליך הבקשה מוקדם מיכאילוב חושב שלהתחיל את התהליך מוקדם יכול לעזור למנוע כלכלי בעיות ברגע האחרון לחברות. הוא גם מציע שהבעלים של עסקים הם יותר טובים בשאלת מומחים שייעצו ויסייעו במהלך כל התהליך.
Yaohai BioPharma, אחת מ-10 המובילות ב-CDMO מיקרוביאלי, אינטגרת ענייני איכות והסדרים התקניים. יש לנו מערכת איכות שמתאימה לחלוטין לסטנדרטים הנוכחיים של GMP, כמו גם להלכות בינלאומיות. צוות האקסPERTS שלנו בתחום ההסדרים הבינלאומיים מחזיק בידע עמוק על מסגרות ההסדרים העולמיות. זה מאפשר לנו להאיץ את השיחות הביולוגיות. אנו יכולים להבטיח תהליכי ייצור נסיגים ותוצרת באיכות גבוהה שמתאימים להלכות של ה-US FDA, תכנית IND לעומת BLA, אוסטרליה TGA, וסין NMPA. Yaohai BioPharma עבר בהצלחה ביקורת באתר שנערכה על ידי האדם המוסמך (QP) של האיחוד האירופי למערכת איכות GMP ואתר הייצור שלנו.我们也прошли את בדיקות התעודה הראשונות של מערכת ניהול האיכות ISO9001 ומערכת ניהול הסביבה ISO14001.
האפליקציהIND vs BLA Application היא מובילה בתחום CDMO של ביולוגיים מיקרוביליים. התמקדותנו הייתה על חיסונים ותרפיות מיוצרים מיקרוביולוגית שמתאימים לניהול בריאות אנושי, וטרינרי וכן בריאות בעלי חיים. יש לנו את פלטפורמות ה-R&D והטכנולוגיה הייצור המתקדמות ביותר שמכסות את כל התהליך, החל מהפיתוח של אצגוני מיקרובים ובנקות תאים, דרך הפיתוח של תהליכים וethodologies, ועד לייצור קליני ומסחרי, מה שמבטיח את מסירת פתרונות חדשניים בהצלחה. עם הזמן, צברנו ידע רב בעיבוד ביולוגי מיקרוביולוגי. יותר מ-200 פרוייקטים הושלמו בהצלחה, ואנחנו עוזרים ללקוחות שלנו להתאים את דרישות רגולטוריות כמו אלו של US FDA ו-EU EMA. אנו גם עוזרים להם לנווט את דרישות TGA האוסטרלית ו-NMPA הסינית. המומחיות המקצועית והניסיון הרחב שלנו מאפשרות לנו להגיב במהירות לצרכים השווקיים ולהציע שירותים מותאמים של CDMO.
ל-Yaohai Bio-Pharma יש נסיון בייצור תרופות ביולוגיות שמוצאות מ徵rganizmy. אנו מציעים פתרונות RD מותאמים וייצור תוך מזעור הסיכונים. עבדנו עם שיטות מגוונות, כמו בקשות IND לעומת BLA של חיסונים (כולל פפטידים), גורמי צמיחה, הורמונים וסיטוקינים. אנו מומחים במספר מארחי מיקרואורגניזמים, כולל שמרים מחוץ לתא ובתוך התא (תוצר עד 15 גרם/ליטר), סקרטציה פריפלסמית של חיידקים, פתירה בתוך התא והרכבים כלולים (תוצר עד 10 גרם/ליטר). יש לנו גם פלטפורמה של BSL-2 לבניית חיסוני חיידקים. אנו מומחים לשיפור תהליכים, להגדלת תוצרי המוצרים ולמזעור עלויות הייצור. יש לנו צוות טכנולוגי יעיל שמבטיח אספקה בזמן ובאיכות איכות. זה מאפשר לנו להגיש את המוצרים האקסלוסיביים שלכם לשווקים מהר יותר.
Yaohai Bio-Pharma, אחת מ-10 הגדלות בבקשות IND לעומת BLA של תכשירים ביולוגיים, היא מומחית בתחום התסיסה המיקרוביאלית. הקמנו מתקן מודרני עם יכולות חזקות של מחקר ופיתוח ובינפראסטרקטורה מתקדמת. ישנן חמש קווי ייצור לתרופות המתאימות לסטנדרטים של GMP לטיהור והתסיסה של תאים מיקרוביאליים, וכן שני קווי מלאי עבור פלאקים, קרטרים ומחטים מוכנים מראש. סקאלת התסיסה הזמינה נע בין 100L ל-2000L. תקן המילוי לפלאקים הוא בין 1ml ל-25ml, בעוד שדרישות מילוי למחטים או קרטרים מוכנים מראש הן בין 1-3ml. אולם הייצור מאושר לפי cGMP ומציע זמינות של דגימות קליניות ומסחריות. המולקולות הגדולות שיוצרות במתקן שלנו זמינות להובלה ברחבי העולם.