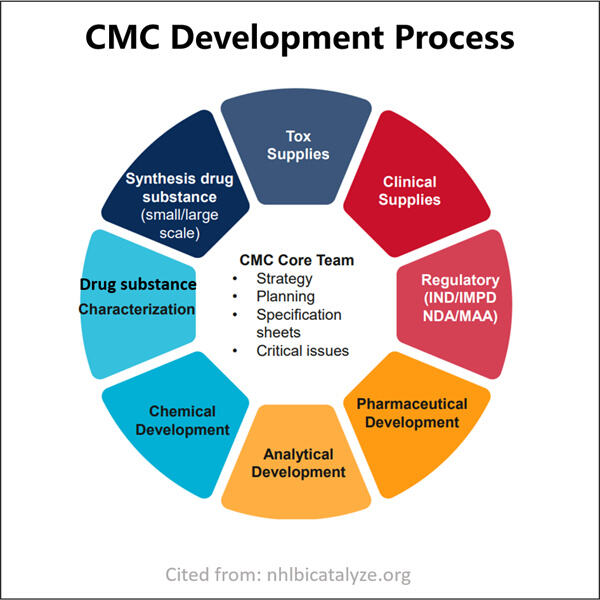
Navigācija caur tehniskajiem prasībām zāļu pieteikumiem
Tas notiek tāpēc, ka viens no galvenajiem pamatnostādnēm drošības apstiprināšanai ir parādīt, ka produkts ir gars un nodrošina uzticamu efektivitāti. Tādējādi, medicīnas līdzekļu izstrādes process jākontrolē intensīvi, tāpēc vairākas zālēm veltītas uzņēmumus, kas darbojas ar simillāru s593 variantu, kopā strādāja vairākus desmitgadus, lai nodrošinātu medicīnas līdzekļu ražošanu. Tas ietver uzņēmumu pienākumu pildīt soli pa solim paredzēto procesu, lai nodrošinātu, ka gala produkts atbilst augstiem kvalitātes standartiem. Tas ir būtiski, jo cilvēku dzīvības ir bīstamas no zālēm, ko tie patērē.
Uzņēmumi, kas reģistrē drošības prasījumus, ir pienākums nodrošināt datus par to, kas ietilpst zālē un kā tā tiek izgatavota. Tas ietver ķīmisko sastāvu, ražošanas procesu un drošības parametrus, kas tajā iekļauti. Šie dati arī atbalstīti zinātniskiem pierādījumiem — parādot, ka zāle ir gan droša, gan efektīva. Jo labāk FDA to saprot, mRNA kopā ar transkripciju notiek apvirsnes procedūra zāle, jo lielāka iespēja novērtēt to informāciju salīdzinājumā ar to, kas jau izmantots citos pētījumos (meta-analīze) konstatēts-citsviet.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN