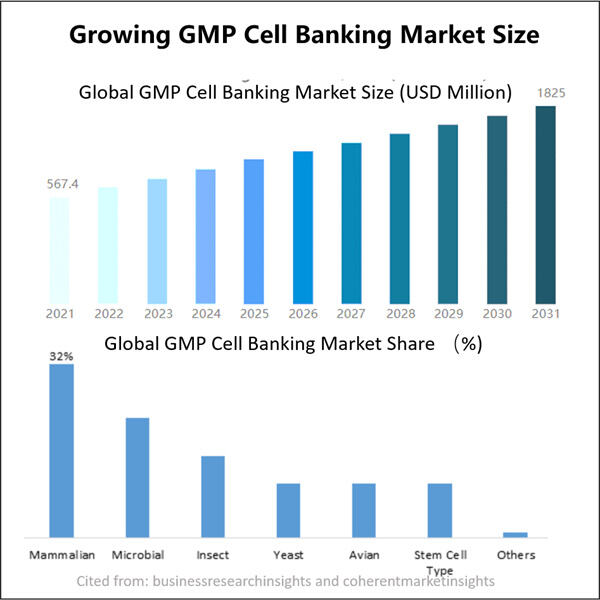
Výhody GMP mikrobiálního buněčného bankovnictví pro vývoj biologických léků
Co získám pomocí GMP mikrobiálního buněného bankovnictví a jeho používání při výrobě mého léku? To účinně ušetří čas výroby, což je jednou z klíčových výhod, protože lze ověřit, zda jsou buňky konzistentní přes více výrobních sérií. To odpovídá konzistentní kvalitě buněk, dávek za dávkou v rámci stejné baterie. Kvalitní kontrola - je důležitá, aby léčba skutečně bezpečně doprovázela domů. S připravenou buněnou bankou mohou výrobci léků vyrobit další dávku téměř hned, jakmile se dostanou do krátkosti své poslední. Toto je potřeba zajistit dobrý a pravidelný zásobník léků.
Společnost musí zajistit patentovaný postup a udržovat své buňky v Výroba GMP CMV antigenu . Tyto buňky, které jsou potřebné k výrobě léků, musí být chráněny před gingivitidou a dalšími znečišťujícími látkami. To znamená, že buňky jsou pěstovány v čistém a sterilním prostředí. To také znamená, že jejich prostředí je čisté a volné od jakýchkoli potenciálních kontaminantů, že ano? Buňky jsou kryoprezervovány pro dopravu a uchování při velmi nízké teplotě. Banka buněk musí také zajistit, aby během uchovávání se do buněk nedostalo nic škodlivého (jako bakterie nebo viry, které mohou být nebezpečné). Taková péče znamená, že buňky jsou jak čisté, tak i připravené k použití.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN