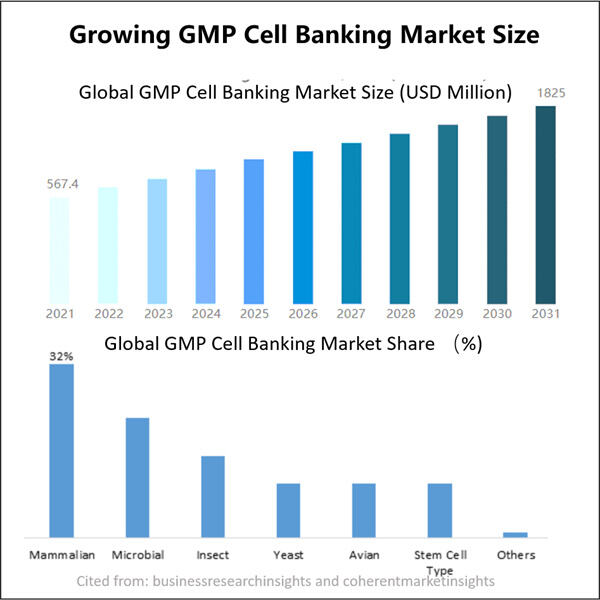
GMP-mikrobisoluvarastoinnin edut biofarmaseuttisen kehityksen kannalta
Mitä saan hyötyä käyttämällä GMP-mikrobisoluontoja lääketyönnössäni? Tämä säästää tehokkaasti tuotantoaikaa, mikä on yksi keskeisimmistä etuista, koska se voi vahvistaa, ovatko solut yhteneviä useissa tuotannossa. Tämä tarkoittaa vakiona olevaa soluplaatua joka toinen sarja samassa joukossa. Laadunvalvonta - on tärkeää, jotta hoito todella vie sinut turvallisesti kotiin. Kun solupankki on valmiina, lääkkeitä valmistavat voivat tuottaa uuden erän melkein heti, kun viimeisestä alkaa loppua. Tämä varmistaa, että on hyvä ja säännöllinen varastollamme lääkkeitä.
Yrityksen on taattava patentoidtu menetelmä ja pidettävä solujaan GMP CMV-antigeenin valmistus . Nämä solut, jotka tarvitaan lääkitykseen, on suojattava parodontiittia ja muita saastumisia vastaan. Tämä tarkoittaa, että solut kasvatetaan puhtaassa ja steriilisessä tilassa. Se tarkoittaa myös, että niiden ympäristö on puhtaana ja vapaana kaikista mahdollisista saasteista, oikein? Solut cyropreserveerataan kuljetusta varten ja säilyttämistä hyvin matalalla lämpötilalla. Solupankki on myös varmistettava, ettei mitään pahaa (kuten bakteereja tai viruksia, jotka voivat olla haitallisia) pääse niihin säilytyksen aikana. Tällainen huolenpito tarkoittaa, että solut ovat sekä puhtaita että valmiita käyttöön.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN