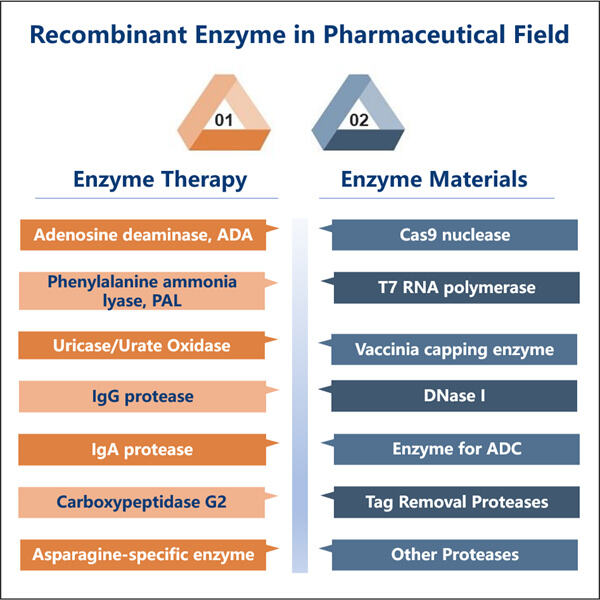
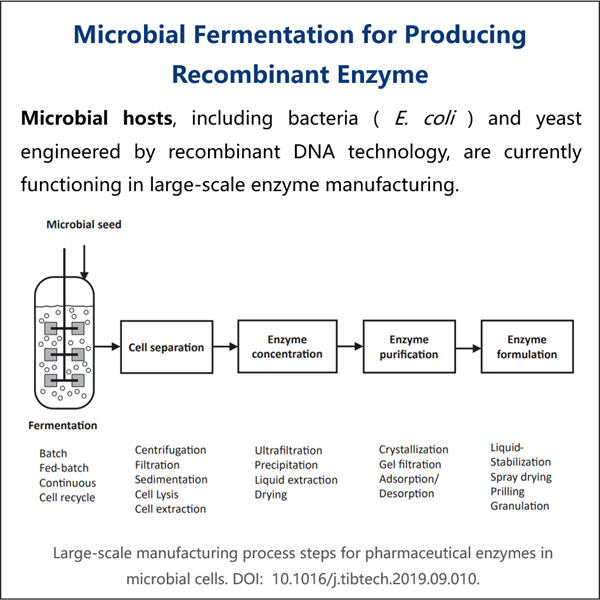
Lợi ích của việc Sử dụng Enzyme Tái tổ hợp GMP trong Công nghiệp
Enzym, mặt khác, là protein làm tăng tốc độ của các phản ứng hóa học. Chúng giống như những gốc tự do nhỏ giúp bạn đạt được kết quả nhanh hơn. Enzym tiêu hóa thức ăn của chúng ta hoặc hỗ trợ trong việc sản xuất năng lượng; Chúng tôi muốn nói rằng bạn tạo ra rất nhiều enzym chất lượng cao theo cách đặc biệt từ DNA và tuân thủ các quy tắc tốt để mọi thứ an toàn và hoạt động hiệu quả — giống như khi chúng ta nói về GMP Semaglutide API sản xuất.
J Pharm Biomed Anal 53: 267—284; với sự cho phép từ Elsevier51 Có hai lợi thế chính của các enzyme tái tổ hợp GMP, cái đầu tiên là chúng có thể được sản xuất với số lượng lớn. Chúng ta có thể sản xuất hàng loạt. Chúng cũng bền hơn, tồn tại lâu hơn các enzyme tự nhiên. Do tính ổn định này, chúng thường có chi phí thấp và rất tốt cho việc xử lý và bảo quản từ một nơi đến nơi khác. Điều này rất quan trọng đối với các công ty cần phải bảo quản và sau đó vận chuyển các enzyme.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN