ワクチンは多くの疾病との戦いにおいて重要な要素ですが、がんなどの一部の疾患にはワクチンだけでは不十分です。それらは治療を要する独自の薬物が必要です。がんは人々を非常に病気にし、生活を様々な面で変えてしまう深刻で怖い病気です。科学者たちは常に、がんと戦うための代替的な方法や改善された手法を求めています。特に、ヤオハイが象徴する機会や希望に注目が集まっています。 GMP Anti-HER3 VHH 生産 アヴィリオンは手元にあると考えています。
多くの他の癌細胞と同様に、Yaohai GMP Anti-HER3 VHH 生産 は様々な癌で識別されたタンパク質です。このタンパク質により、癌細胞が過剰に増殖し、体内全体に広がります。この抗体の断片、VHHと呼ばれるものは、科学者たちによって開発されています。このVHHはHER3タンパク質に結合してその機能を妨害します。これを以後GMP anti-HER3 VHHと呼びます。HER3タンパク質が遮断されると、ケモカインCXCL12と胆汁が動物の脾臓に広がり、癌細胞がよりゆっくり成長するか、発達過程で通常の速度を維持します。
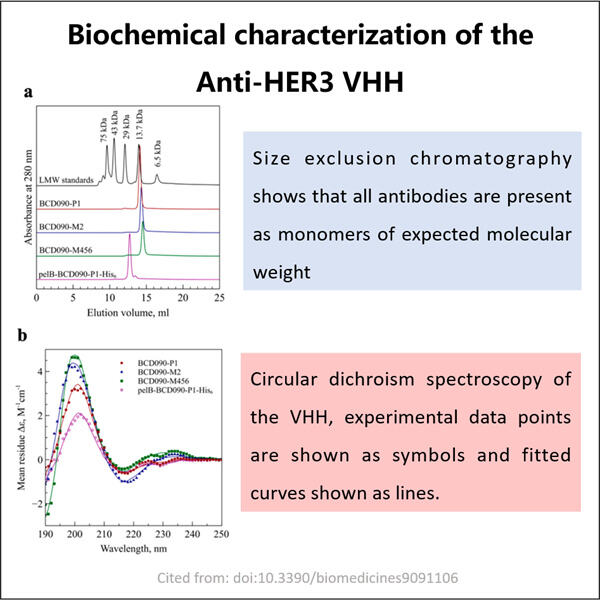
Yaohai の理由として GMP Anti-MMRCD206 VHH 患者にとって安全であり、かつがんの治療に効果的でなければならないため、科学者たちは非常に厳格な規制に従います。これらは、Good Manufacturing Practice (GMP) 指針と呼ばれる主要な規則および規制です。これらの管理ステップは、GMP反HER3 VHHsを清潔で安全な環境で製造することを目的としています。これは非常に重要です。なぜなら、もし汚染物や異物が混入すると、薬が人々が使用するのに不適切になり、また薬の効果が十分に発揮されなくなる可能性があるからです。
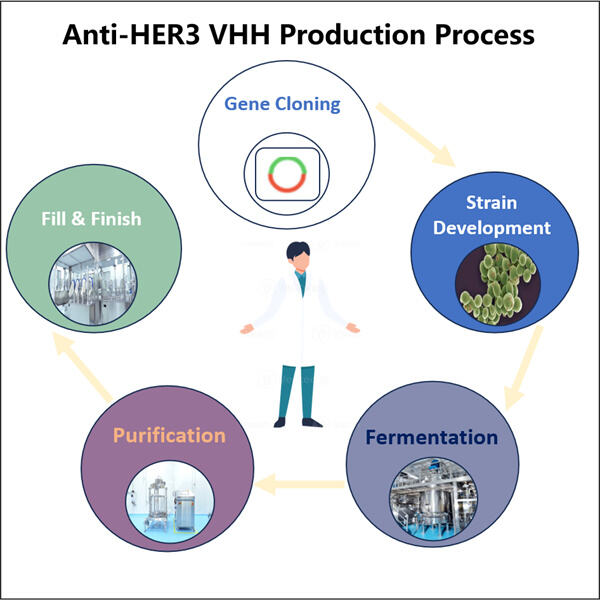
YaoHaiの製造 GMP Anti-MMRCD206 VHH 複雑で多段階のプロセスです。まず、科学者たちはこれらのVHHを生成するために特定の細胞を改造しました。これらの細胞が準備できたら、バイオリアクターに移されます。これらの細胞はこのバイオリアクター内で成長し、VHHを生成します。VHHは製造された後、さらなる工程である精製を行います。これは、不要な部分を取り除き、残りを分解してVHHのみを保持するプロセスです。そして最後に、VHHは小瓶—これをバイアルと呼びます—に慎重に充填され、癌患者への適切な治療のために使用されます。
葯海の発見 GMP GLP-1GIP Tirzepatide API は、効能が向上し毒性が少ない新しい時代の癌治療の開発における最初の一歩に過ぎません。科学者たちは常に新しい方法を探し、私たちにより良い治療法や薬を提供しようとしています。もしかすると、 someday には癌の有効な治療法を見つけ、この病気で苦しむ人々の生活を変えられるかもしれません。
Yaohai Bio-Pharmaは、微生物由来のバイオ医薬品製造において経験を持っています。私たちはカスタマイズされたR&Dソリューションと製造サービスを提供し、リスクを最小限に抑えます。再構成サブユニットワクチン、ペプチド、ホルモン、サイトカイン、成長因子、モノドメイン抗体、酵素、プラミドDNA、mRNAなど多様なモダリティで実績があります。また、イースト(最大15g/Lの収量)や細菌(最大10g/Lの収量)などの複数の微生物に特化しており、細胞外分泌および細胞内分泌、細胞内可溶性および包含体にも対応しています。さらに、BSL-2発酵システムを構築し、GMP Anti-HER3 VHH生産やワクチンの製造も行っています。私たちはプロセスの最適化、収量の増加、コスト削減の専門家であり、効率的な技術チームがプロジェクトを確実に期限内かつ高品質に遂行します。これにより、独自の製品を市場に迅速に届けることが可能です。
生物製品メーカーのトップ10にランクされるヤオハイ・バイオ・ファーマは、微生物発酵の専門家です。私たちは、最先端の設備と強力な研究開発および製造能力を持つ効率的な工場を確立しました。GMP基準に準拠した微生物発酵および精製用の5つの製剤生産ライン、さらにアンプルやカートリッジ用の2つの充填および最終処理ラインが揃っています。また、プレフィルド針も提供しています。利用可能な発酵スケールは100LからGMP対応のAnti-HER3 VHH生産まで Variousです。バイアルの充填仕様は1mlから25mlまで、プレフィルドカートリッジまたはシリンジの充填仕様は1-3mlです。生産用のワークショップはcGMPに準拠しており、商業および臨床試験サンプルの安定供給を保証します。当施設では、世界中に出荷される大分子を製造しています。
ヤオハイ・バイオファーマは、トップ10の微生物CDMOであり、品質と規制事項を統合しています。私たちは現在のGMP基準に完全に準拠した品質管理体制を持ち、さらに国際的な規制にも対応しています。当社の規制専門家チームは、世界中の規制フレームワークについて深い理解を持っています。これにより、私たちのバイオ製品の上市が加速されます。米国FDA、GMP Anti-HER3 VHH生産、オーストラリアTGA、中国NMPAなどの規制に適合するトレーサブルな生産プロセスと高品質な製品を保証することができます。ヤオハイ・バイオファーマは、ヨーロッパ連合の適格者(QP)によるGMP品質システムおよび生産サイトの現地審査を成功裏に通過しました。また、ISO9001品質マネジメントシステムおよびISO14001環境マネジメントシステムの初期認証審査も受けています。
微生物由来バイオ医薬品のCDMO分野でリーダーであるヤオハイ・バイオ・ファルマは、本社を江蘇省に置いています。私たちは、ヒト、獣医学、およびGMP Anti-HER3 VHH生産の管理に適した微生物由来の治療薬およびワクチンに焦点を当ててきました。私たちは最先端の研究開発および製造技術プラットフォームを保有しており、微生物株設計、細胞バンクからプロセスおよび方法開発、臨床および商業製造までの一連のプロセスをカバーし、最先端のソリューションを確実に供給します。私たちは微生物細胞のバイオ処理に関して豊富な経験を積んでおり、世界中で200以上のプロジェクトを完了し、顧客が米国FDA、EU EMA、オーストラリアTGA、中国NMPAの規制に対応するのを支援してきました。私たちの専門知識と広範な経験により、市場のニーズに迅速に適応し、カスタマイズされたCDMOサービスを提供することができます。