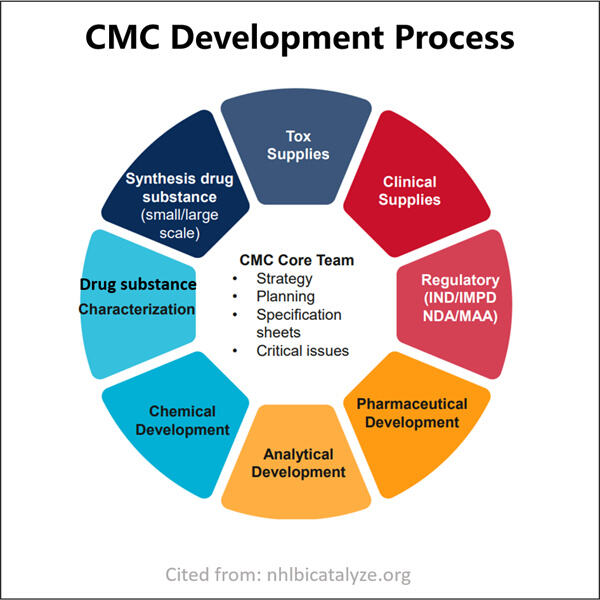
Navigare i Requisiti Tecnici delle Domande di Farmaci
Questo è perché uno dei punti di vista fondamentali più importanti per l'approvazione di un farmaco è dimostrare che il prodotto è puro e ha una affidabilità costante. Quindi, il processo di produzione dei farmaci deve essere intensamente supervisionato, il che spiega perché alcune aziende farmaceutiche con variazioni quasi simili, come la variante s593, hanno lavorato insieme per più di un decennio per fornire medicinali. Ciò include il passaggio delle aziende attraverso un processo passo-passo per assicurarsi che il prodotto finale sia anche mantenuto secondo standard di alta qualità. Questo è fondamentale poiché sono in gioco le vite delle persone che consumano questi farmaci.
Le aziende che registrano un'istanza di un farmaco devono fornire dati quasi su ciò che entra nel farmaco e su come viene prodotto. Ciò include la composizione chimica, il processo di produzione e i parametri di sicurezza incorporati. Questi dati sono inoltre supportati da prove scientifiche - dimostrando che il farmaco è sia sicuro che efficace. Più il FDA riesce a comprenderlo, protocollo di Cappatura Co-trascrittiva dell'MRNA più probabilmente possono valutare le sue informazioni rispetto a ciò che è stato fatto in altri studi (meta-analisi) altrove.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN