Tādēļ Yaohai mēs saprotam GMP RSV G Protein ražošanas nozīmi mums. Tas ļauj mums pārbaudīt, vai mūsu produkti ir gan droši, gan augstas kvalitātes. Ko nozīmē GMP RSV G Protein ražošanā? Mēs apspriedīsim, kā definējam GMP vai labo ražošanas praksi, un dažādus stratēģijas, ko izmantojam, lai sasniegtu savu produktu augstāko kvalitāti nākamajos posmos.
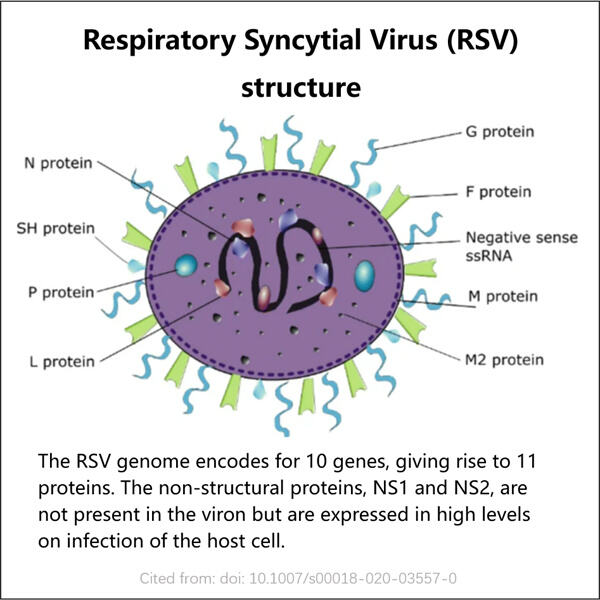
Dažādās valstis ir atšķirīgas standartizācijas piemēram: *GMP: Labā prakse ražošanā. Tie ir norādījumi, kuros mēs ražojam drošu un efektīvu RSV G Protein. Viens no ļoti svarīgajiem produktiem ir RSV G Protein, kas palīdz cilvēkiem, kuri slimnīku dēļ vīrusa, kas sauc par respiratoriju sinhronisma virusu vai RSV. AAV Plazmīda ražošana bīstība var būt īpaši smaga jaunām bērniem, maziem bērniem un vecākiem cilvēkiem. Tāpēc ir neiedomājami svarīgi, lai RSV G proteīns, ko mēs piegādājam, būtu gan drošs, gan piemērots uzdevumam.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN