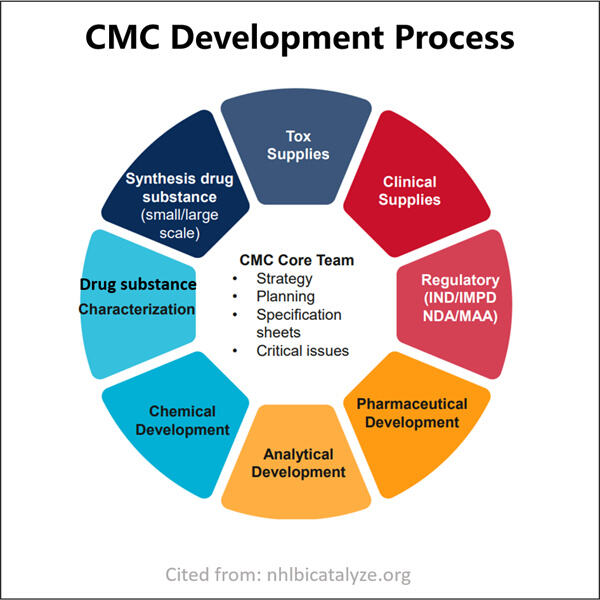
Navegando por los Requisitos Técnicos de las Solicitudes de Medicamentos
Eso es porque uno de los puntos de vista básicos más importantes de la aprobación de medicamentos es demostrar que el producto es puro y tiene una eficacia confiable. Por lo tanto, el método de fabricación de los medicamentos debe estar altamente regulado, lo cual es por qué algunas empresas farmacéuticas con variaciones s593 comparativamente similares han trabajado colectivamente durante más de una década para proporcionar medicamentos. Esto incluye que las empresas pasen por un proceso paso a paso para asegurarse de que el producto final también se mantenga dentro de las normas de alta calidad. Esto es fundamental ya que las vidas de las personas están en juego con los medicamentos que consumen.
Las empresas que registran una solicitud de medicamento deben proporcionar datos sobre casi todo lo que entra en el fármaco y cómo se fabrica. Esto incluye la composición química, el proceso de fabricación y los parámetros de seguridad incorporados en él. Estos datos también están respaldados por pruebas científicas, demostrando que el medicamento es tanto seguro como efectivo. Cuanto más entienda la FDA, protocolo de Co-transcripción y Capping de ARNm el medicamento, más probabilidades tendrán de evaluar su información en comparación con lo que se ha utilizado en otros estudios (metanálisis) en otras partes.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN