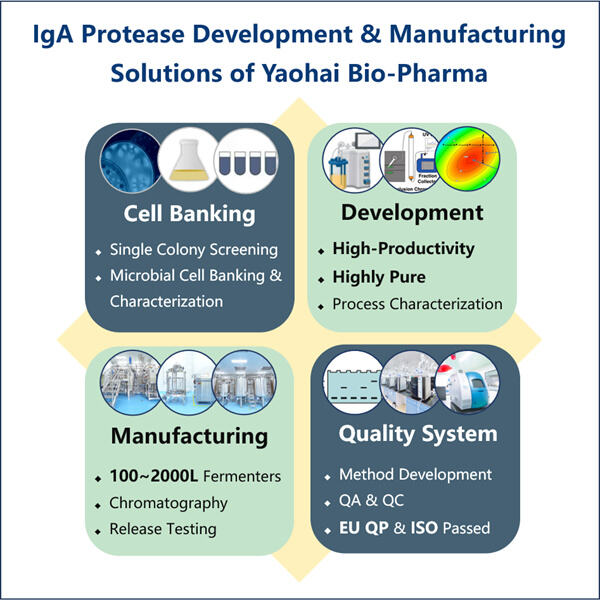
Bước đầu tiên cho phương pháp sản xuất này là nhân bản gen. Khi thực hiện, các nhà nghiên cứu chuyển DNA — bản thiết kế để sản xuất protease IgA1 — vào một tế bào chủ. Trong trường hợp này, tế bào chủ là một tế bào sống sẽ hỗ trợ sản xuất enzyme. Khi các nhà khoa học bắt được tế bào chủ phù hợp, họ sẽ tạo ra tế bào đó trong một chất lỏng đặc biệt gọi là môi trường nuôi cấy để cho phép tế bào phát triển khỏe mạnh và mạnh mẽ.
Lên men là quá trình thứ hai. Tại thời điểm này, các tế bào chủ được thêm vào một bình lớn, còn được gọi là lò phản ứng sinh học. Tất nhiên, các tế bào chủ được phép phát triển và sinh sôi trong lò phản ứng sinh học này. Sau đó, protease IgA1 tái tổ hợp được các tế bào tiết vào dịch lên men khi chúng phát triển. Đây là bước thiết yếu nhất cho đến nay vì đây là lúc enzyme thực sự được tổng hợp.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 KHÔNG
KHÔNG
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN