Tùy chỉnh, hiệu quả và tiết kiệm chi phí
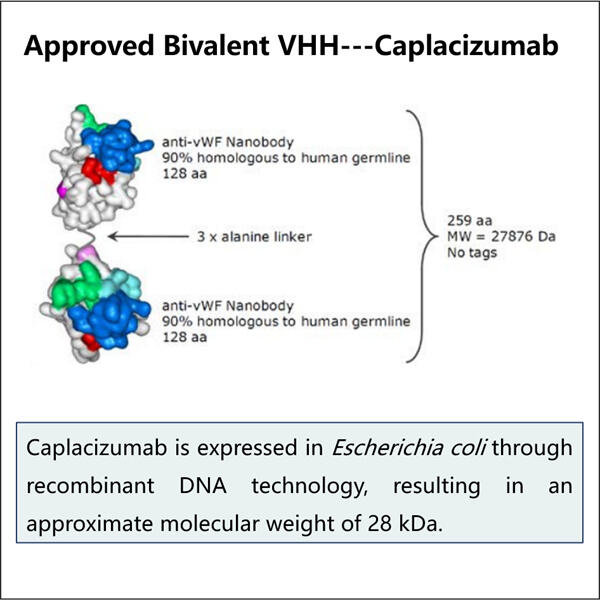
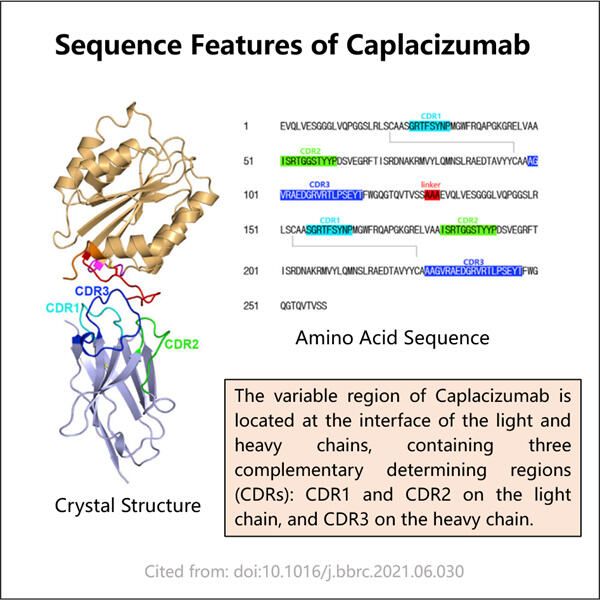
Yaohai Bio-Pharma has experience in manufacturing biologics that are created from microorganisms. We offer bespoke RD solutions as well as manufacturing services while minimising potential risks. We have worked with diverse techniques, such as recombinant cellular subunits, vaccines (including peptides), growth factors, hormones, and the Caplacizumab Manufacturing. We are a specialist in many microorganisms like yeast extracellular and intracellular secretion (yields up to 15g/L) and bacteria intracellular soluble, and inclusion body (yields up to 10g/L). We have also developed a BSL-2 fermentation platform to create bacterial vaccines. We have a track record of improving production processes, thereby increasing yields and reducing costs. We have a highly-efficient technology team to ensure timely and high-quality delivery of projects. This helps us bring your products that are unique faster to the market.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 KHÔNG
KHÔNG
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN