これは、INDまたはBLA /sを提出する際に確認するチェックリストです。これにより、必要なすべてのファイルを生成し、FDAに適切に提出することができます。当社のマップを使用すると、レガシーからデータを引き出すための重要なステップを見逃すことはありません。このようにして、申請は正確で徹底したものになります。
INDまたはBLA申請は長くて実行が難しい場合があります。Yaohaiの指示に従って整理されたチェックリストを使用すると、間違いが減り、効率が向上します。このチェックリストは、申請のすべてのステップで明確かつ明確に作成されています。 HPVワクチンVLP プロセス
嬉しいことに、すべての手順を正しく実行できるように、チェックリストが用意されています。さらに重要なのは、各手順に明確な指示が用意されているため、次に何をすべきかが簡単にわかることです。
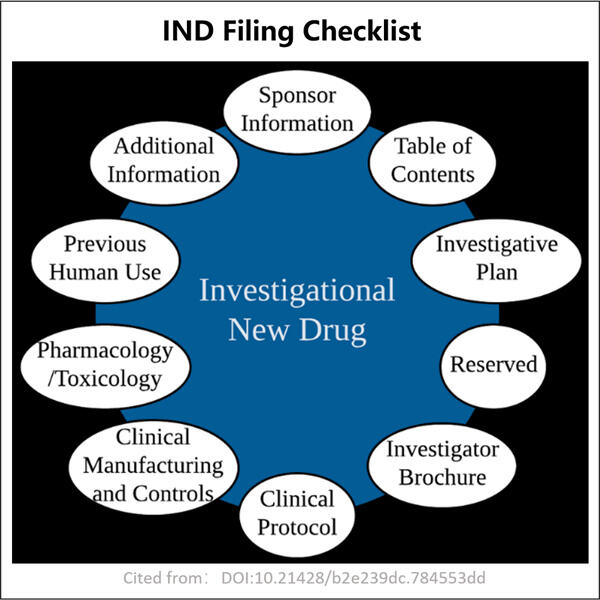
チェックリスト GMP 抗 PD-1PD-L1 VHH 最初の準備から申請書の提出、そしてその後に至るまでのステップごとのロードマップを提供します。全体を通して、申請をできるだけスムーズに行うためのヒントやアドバイスを散りばめています。

INDおよびBLAプロセスの重要なステップを1つも見逃してはいけません。これは非常に重要です。INDまたはBLAの申請は非常に詳細かつ正確なプロセスです。そのため、常にチェックリストを参照することをお勧めします。 GMP 抗MMRCD206 VHH すべてのボックスにチェックを入れてください。

当社のチェックリストには、IND / BLA 申請に従ったすべての要件が含まれています。これにより、申請が包括的で、事実に基づいており、すべての FDA 規制要件に準拠していることを確認できます。
Yaohai BioPharma は、IND および BLA 充填チェックリストのトップ 10 にランクされており、規制関連業務と品質管理を組み合わせています。当社は、世界中の現在の GMP 基準と規制に準拠した品質システムを備えています。当社の規制チームは、世界中の規制フレームワークを深く理解しています。これにより、生物学的製剤の発売を加速できます。当社は、高品質の製品による追跡可能な製造手順と、米国 FDA および EU EMA の規制への準拠を確保しています。オーストラリア TGA および中国 NMPA も満たしています。Yaohai BioPharma は、欧州連合の認定資格者 (QP) が実施した、GMP システムと製造施設の検査を実施した対面監査に合格しました。また、ISO9001 品質管理システムと ISO14001 環境管理システムの初期認証監査にも合格しています。
Yaohai Bio-Pharma は、微生物由来の生物製剤の開発に豊富な経験を持っています。当社は、リスクがないことを確認しながら、カスタマイズされた RD および製造ソリューションを提供します。当社は、サブユニットベースの組み換えワクチン、IND および BLA 記入チェックリスト、サイトカイン、成長因子、単一ドメイン抗体、酵素、プラスミド DNA、mRNA など、さまざまな手法に取り組んできました。当社は、酵母の細胞外および細胞内分泌物 (最大 15g/L の収量) や細菌の細胞内可溶性および封入体 (最大 10g/L の収量) など、さまざまな微生物の専門家です。また、細菌ベースのワクチンを作成するための BSL-2 発酵プラットフォームも開発しました。当社は、生産プロセスを改善し、それによって収量を増やし、コストを削減した実績があります。非常に効率的な技術チームにより、タイムリーで質の高いプロジェクト配信を保証し、製品をより早く市場に投入します。
Yaohai Bio-Pharma は、微生物バイオロジクスの CDMO のリーダーです。当社は、ヒト、獣医、ペットの健康管理のための微生物生産治療薬とワクチンに注力しています。当社は、IND および BLA 充填チェックリスト RD プラットフォームに加え、微生物株細胞、方法、プロセスの開発から商業および臨床製造までの全プロセスを網羅する製造技術を備えており、最先端のソリューションを確実に実装できます。当社は、微生物細胞のバイオ処理で豊富な経験を積んでいます。当社は 200 を超えるグローバル プロジェクトを実施しており、米国 FDA、EU EMA、オーストラリア TGA、中国 NMPA の法律を順守するお手伝いをしています。当社の専門知識と豊富な経験により、市場の需要に迅速に対応し、カスタマイズされた CDMO サービスを提供することができます。
Yaohai Bio-Pharma は、IND および BLA 充填チェックリストを専門とするトップ 10 のバイオ企業です。当社は、強力な RD 機能と最新の製造設備を備えた最新の製造施設を建設しました。微生物発酵および精製の GMP 基準に準拠した 100 つの薬物物質製造ライン、およびバイアルとカートリッジ、および充填済みニードル用の 2000 つの充填および最終ラインがすぐに利用できます。使用可能な発酵スケールは 1L から 25L までです。充填量は 3ml から 3.5ml までです。充填済みのシリンジまたはカートリッジには、XNUMXml から XNUMXml が充填されます。cGMP に準拠した当社の製造ワークショップでは、臨床サンプルと市販製品を安定的に供給できます。当社の施設では、世界中に輸出される高分子を製造しています。