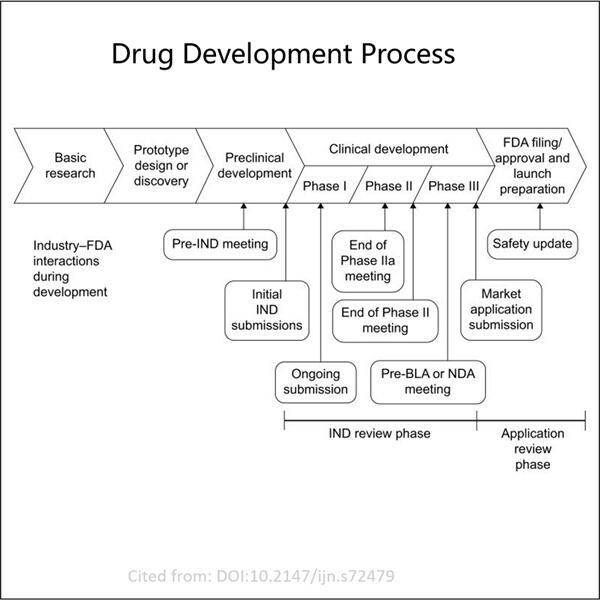
Радзі і хітрыніцы
Аднак, патрабаванне BLA трохі складней. Перш за ўсё, кампанія павінна была вытеставаць лекарства на людзях, каб паказаць, што яно яўляецца і безпечным, і эфектыўным. Гэта трымае кампанію збору агромных дадзеных і інфармацыі з выкананых тэsts. Заяўленне BLA ўваходзіць у намношую колькасць дэталей, чым заявка IND, і яе падготовка займае прыкладна 1 год у традыцыйных выпадках. Гэта бярэ намнош часу, бо кампанія павінна даказаць, што яна Высоцкая ферментацыя плазміда лекарства працуе дужа добра і безпечно для чалавека
Тут Яаўхай дзеліцца некаторымі асноўнымі radкарамі для тых, хто шукае падаць ўспеховыя заявку IND/BLA. Пачаткам, яны радуюць збір няшта групы прафесіяналаў, якія магуць кіраўваць іншым праз процэс заяўлення. Гэтая каманда павінна ўключаць людзей, якія разумеюць, як розвіваюцца лекарства і правілы, якім неабходна дасталецца, і ведаюць, як працуе клінічнае даследванне. Бяспрысудна маць правільную каманду можа змяніць фарт заяўлення.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN