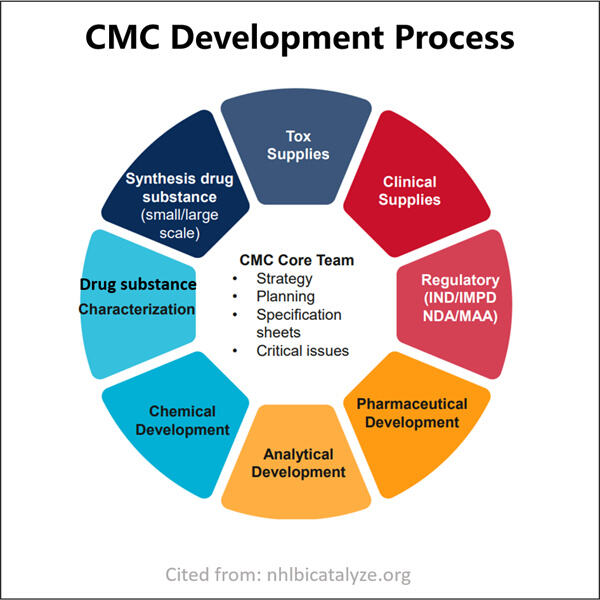
Навігація у технічних вимогах до заяв на лікарські засоби
Це тому, що одна з головних базових позицій регулювання лікарських засобів полягає у доведенні, що продукт є чистим та має стабільну ефективність. Отже, процес виготовлення ліків повинен бути жорстко регульованим, тому кілька фармацевтичних компаній з майже схожими варіаціями s593 працюють разом більше десяти років для доставки ліків. Це включає проходження компаніями крок за кроком певної процедури, щоб переконатися, що кінцевий продукт також підтримується в якісних нормах. Це важливо, оскільки життя людей залежить від ліків, які вони споживають.
Компанії, що фіксують заявку на лікарське засоби, повинні надавати дані майже про те, що входить у склад лікарського засобу та як він виготовляється. Це включає хімічний склад, процес виготовлення та параметри безпеки, які вбудовані у нього. Ці дані також підтверджуються науковими доказами — що ілюструє, що лікарський засіб є як безпечним, так і ефективним. Чим краще FDA може це зрозуміти, протокол ко-транскрипційного закриття MRNA лікарський засіб, тим більша ймовірність, що вони зможуть оцінити його дані у порівнянні з тим, що було використано в інших дослідженнях (мета-аналіз) const-в інших місцях.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN