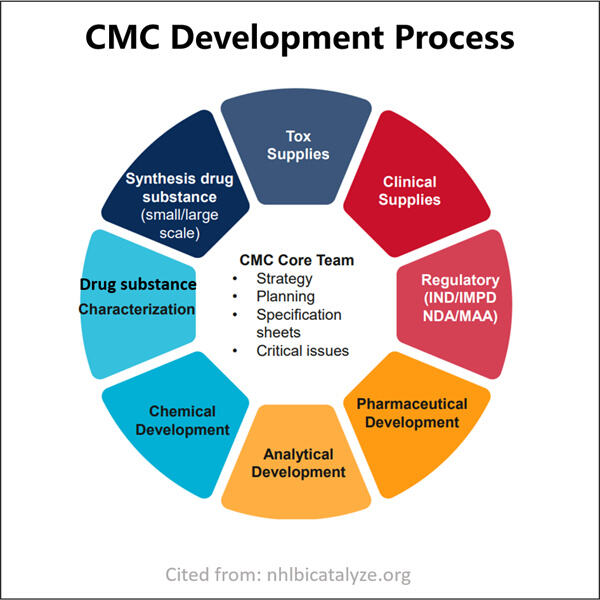
Navigace technickými požadavky při podávání léků
To je proto, že jednou z nejdůležitějších základních zásad schválení léků je dokázat, že produkt je čistý a má spolehlivou účinnost. Proto musí být proces výroby léků přísně kontrolován, což je důvod, proč některé lékařské firmy s téměř stejnou variací s593 spolupracují již více než deset let na dodávce léků. To zahrnuje procházení krok za krokem procesem, který zajistí, že konečný produkt splňuje také kvalitní normy. Je to klíčové, protože jsou v sázce lidské životy těch, kteří tyto léky konzumují.
Společnosti zaznamenávající lékařskou aplikaci by měly poskytovat data téměř o všem, co je součástí farmaceutického produktu a jak je vyroben. To zahrnuje chemickou složení, výrobní proces a bezpečnostní parametry spojené s ním. Tyto údaje jsou dále podpořeny vědeckými důkazy – dokazujícími, že lék je jak bezpečný, tak účinný. Čím lépe FDA porozumí tomuto obsahu, protokol ko-transkripčního uzavření mRNA tím spíše mohou porovnat jeho informace s tím, co bylo použito v jiných studiích (meta-analyza) v jiných oblastech.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN