GMP(Good Manufacturing Practice)는 프로세스, 절차 및 문서로 구성된 품질 보증의 한 측면입니다. GMP는 의약품이 인간이나 동물의 의도된 용도에 적합한 품질 표준에 따라 일관되게 생산되고 관리되도록 보장합니다.
GMP 등급 생물학적 제제의 안정적이고 신뢰할 수 있는 공급은 전임상, 1상, 2상, 3상 및 상업 단계를 포함하여 제품 수명주기의 모든 단계에서 매우 중요합니다.
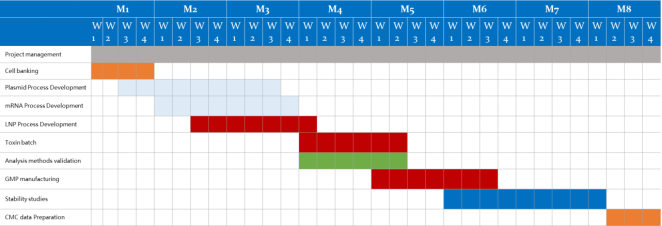
GMP 제조 역량
|
학년 |
산출물 |
수량 |
어플리케이션 |
|
비GMP |
mRNA DS |
0.1~10mg(mRNA) |
전임상 연구, 형질감염, 분석법 개발, 제형 개발 |
|
mRNA-LNP DP |
|||
|
GMP, 무균 |
mRNA DS |
10mg~70g(mRNA) |
IND/CTAor BLA/MAA 제출, 임상시험 및 상업용 공급. |
|
mRNA-LNP DP |
5000개 바이알 또는 사전 충전된 주사기/카트리지 |
|
P로세스 |
서비스 세부정보 |
단위 운영 |
|
기술 이전 |
문서 전송 |
공정, 제제, 분석 방법 및 품질 표준 |
|
기술 및 규정 준수 평가
|
인간-기계-재료-방법-환경-측정 평가; 공정, 제형, 분석 방법 및 품질 표준을 평가합니다. |
|
|
기술이전 실시 |
제조 공정 및 분석 전달 |
|
|
프로세스 검증 |
1~3공학배치프로세스가 견고하다는 것을 평가하고 확인합니다. |
|
|
플라스미드 제조 |
E. 대장균발효 |
발효 시스템의 준비 |
|
씨c배양, 유가식 발효 |
||
|
플라스미드 정제 |
E. 대장균세포 수확 및 알칼리 용해 |
|
|
플라스미드 정제, 불순물 제거 |
||
|
플라스미드 선형화 |
S단일 효소 소화 |
|
|
선형화된 템플릿 플라스미드의 정제 |
||
|
mRNA DS 제조 |
mRNA 합성 |
체외전사 (IVT) 반응 |
|
mRNA 정제 |
DNA 템플릿 제거 |
|
|
mRNA 정제, 불순물 제거 |
||
|
mRNA 버퍼 교환 |
접선 흐름 여과 |
|
|
LNP DS 제조 |
LNP 캡슐화 |
지질을 함유한 에탄올 상의 제조 |
|
미세유체공학 기술 |
||
|
농도 및 버퍼 교환 |
접선 흐름 여과 |