La conjugación del antígeno objetivo con proteínas portadoras también es una estrategia de desarrollo de vacunas, como las vacunas conjugadas. La unión con proteínas portadoras puede mejorar la inmunogenicidad de las vacunas. Actualmente, las proteínas portadoras aprobadas en el mercado incluyen el toxoide diftérico (DT), el mutante no tóxico de la toxina diftérica CRM197, el toxoide tetánico (TT), etc.
Con una potente plataforma de desarrollo de procesos, talleres de nivel de bioseguridad BSL-1 y BSL-2, y un sistema de calidad GMP, Yaohai Bio-Pharma puede proporcionar a los clientes una solución integral desde el desarrollo de cepas microbianas hasta la producción GMP de proteínas portadoras.
Ofrecemos proteínas portadoras a escala de gramo a kilogramo que cumplen con los estándares de calidad, así como registros de producción GMP e informes de pruebas a nuestros clientes.
Las vacunas conjugadas aprobadas incluyen las siguientes proteínas portadoras (no recombinantes):
|
Tipos de Proteínas
|
Proteínas Portadoras
|
Tipos de Cepas
|
Plataforma
|
|
Proteína portadora, extraída
|
Mutantes no tóxicos de la toxina de la difteria CRM197
|
Corynebacterium diphtheriae
|
Sistemas de fermentación microbiana
Equipo de centrifugación y homogeneización
Sistemas de cromatografía de alta/baja presión
Tanque de reacción conjugada
Nivel de bioseguridad: BSL-2
Sistema de calidad GMP
|
|
Toxina Diftérica (DT)
|
Corynebacterium diphtheriae
|
|
Toxoides tetánicos (TT)
|
Clostridium tetani
|
|
Complejo de proteína de membrana externa meningocócica (OMPC)
|
Neisseria meningitidis
|
|
Otras proteínas portadoras de origen microbiano (BSL-1, BSL-2)
|
|
Servicios relacionados: Soluciones CDMO de Proteína Portadora Recombinante .
|
Proceso del Producto Farmacéutico con Proteína Portadora
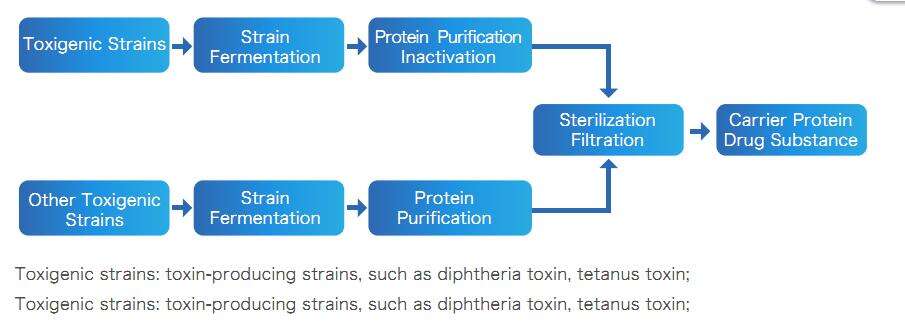
Entregable
| Grado |
Entregables |
Especificación |
Aplicaciones |
| GMP, BSL-1/BSL-2 |
Sustancia intermedia |
Proteína portadora derivada de bacterias |
Materiales para la producción de vacunas conjugadas |
| Producto final de la vacuna |
Polvo liofilizado |
Solicitud de nuevo fármaco de investigación (IND),
Autorización de ensayo clínico (CTA),
Suministro para ensayos clínicos,
Solicitud de licencia biológica (BLA),
Suministro comercial
|

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN


