Trình độ chuyên môn & kinh nghiệm phong phú
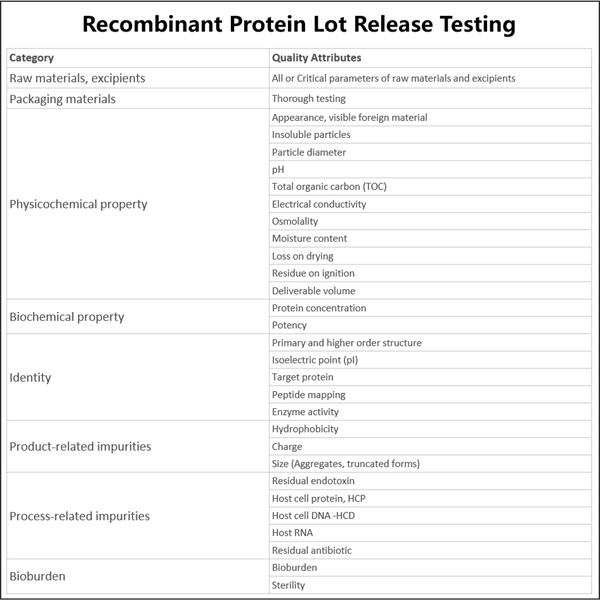
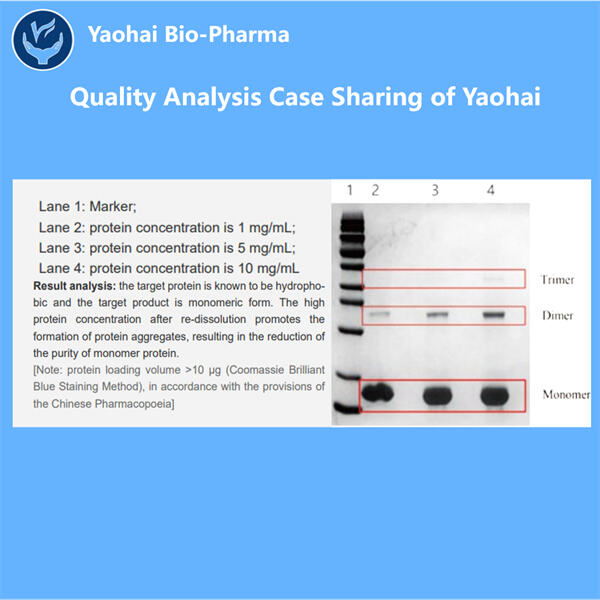
Yaohai Bio-Pharma là một CDMO sinh học vi sinh hàng đầu. Chúng tôi tập trung vào các liệu pháp và vắc-xin do vi sinh sản xuất cho con người, thú y và quản lý sức khỏe vật nuôi. Chúng tôi được trang bị các nền tảng RD thử nghiệm giải phóng lô protein tái tổ hợp cũng như công nghệ sản xuất bao gồm toàn bộ quy trình bắt đầu từ việc phát triển các tế bào, phương pháp và quy trình chủng vi khuẩn, đến sản xuất thương mại và lâm sàng, đảm bảo triển khai thành công các giải pháp tiên tiến. Chúng tôi đã có được nhiều kinh nghiệm trong quá trình xử lý sinh học các tế bào vi khuẩn. Chúng tôi đã thực hiện hơn 200 dự án toàn cầu và giúp khách hàng của mình điều hướng các luật từ FDA Hoa Kỳ, EMA EU, TGA Úc và NMPA Trung Quốc. Chuyên môn chuyên nghiệp và kinh nghiệm sâu rộng của chúng tôi cho phép chúng tôi phản ứng nhanh chóng với nhu cầu của thị trường và cung cấp các dịch vụ CDMO phù hợp.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 KHÔNG
KHÔNG
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN