Tipy a triky
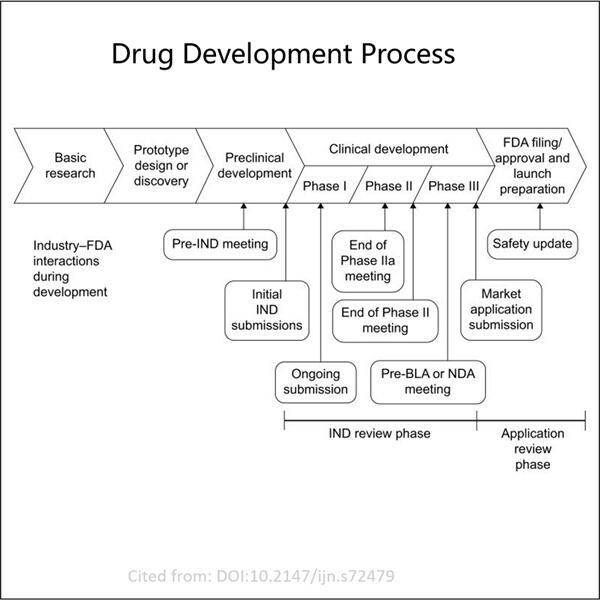
Avšak, podanie žiadosti BLA je niečo komplikovanejšie. Pred tým, než spoločnosť môže žiadať o licenciu, musela už testovať liek na ľuďoch, aby dokázala, že je bezpečný a účinný. To vyžaduje, aby spoločnosť zosbírala obrovské množstvo údajov a informácií z vykonaných testov. Žiadosť BLA sa dostane do mnohem väčších detailov ako žiadosť IND a ich príprava trvá tradične asi 1 rok. Trvá to oveľa dlhšie, pretože spoločnosť musí dokázať, že ich Vysokoproduktívna plazmidová fermentácia liek veľmi dobre funguje a je bezpečný pre ľudí
Tu sa Yaohai delí s niektorými základnými radami pre tých, ktorí hľadajú podanie úspešnej žiadosti IND/BLA. Na začiatku odporúčajú zoskupiť skupinu odborníkov, ktorí môžu mentovať druhého cez proces podávania žiadosti. Tento tím by mal obsahovať ľudí, ktorí rozumejú tomu, ako sa vyvíjajú lieky a pravidlá, ktorým musia dodržiavať, a tiež vedieť, ako funguje klinický výskum. Bez pochýb má mať správny tímový dosah na štěstie žiadosti.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN