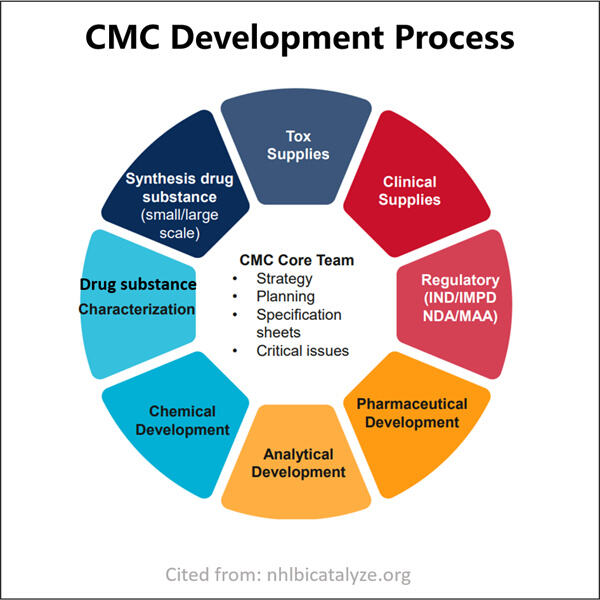
Navigácia technických požiadaviek na podanie liečiv
A to preto, lebo jedným z najzákladnejších pohľadov na schválenie liekov je dokázanie, že produkt je čistý a má spoľahlivú účinnosť. Preto by mala byť metóda výroby liekov intenzívne riadená, čo je dôvod, prečo niektoré lekárskych spoločnosti s témami skoro rovnakého typu s593 spolupracovali po viac ako desaťročie na dodávaní liečiv. To zahŕňa prechádzanie spoločností krokovo procesom, aby sa uistiili, že konečný produkt je tiež vyrobený podľa kvalitných štandardov. Je to kľúčové, pretože sú v súvislosti životy ľudí, ktorí ich konzumujú.
Spoločnosti, ktoré zaznamenávajú podanie lieku, by mali poskytnúť údaje takmer o tom, čo sa dostane do lieku a ako je vyrobený. To zahŕňa chemickú sústavu, výrobný proces a bezpečnostné parametre, ktoré sú do neho zapracované. Tieto údaje sú tiež podporené vedeckými dôkazmi - ukazujúcimi, že liek je bezpečný a účinný. Čím lepšie FDA pochopí, protokol súčasného zakončenia mRNA lieku, tým väčšia je pravdepodobnosť, že môžu zhodnotiť jeho údaje v porovnaní s tým, čo bolo použité v iných štúdiách (meta-analýza) konštantne inde.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN