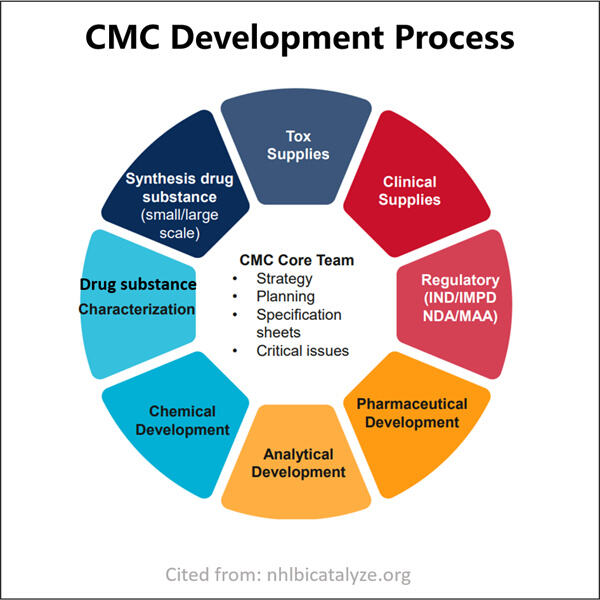
CMC står for Kjemi, Fabrikkering & Kontroll. Denne komponenten kan være en betydelig del av den roligere behandlingsprosessen for et nytt legemiddel. Det forteller deg hvordan legemiddelet er laget og hvordan det har blitt testet for å være sikker på at det er et trygt, høykvalitetsmedisinsk alternativ for de som skal ta dette legemiddelet. Forståelse av hva Yaohai CMC forklarer. test av effektivitet av MRNA-kapping for Plasmid DNA kan gi ny innsikt i hvordan bedrifter sikrer kvaliteten på sine produkter.
Det finnes nøyaktige regler for å tilby et medisin, selskapene må vise at legemiddelet er godt laget og er bra for deg. FDA, som er forkortelsen for Mat og Medisinvirksomhet, inneholder en veileder om hvordan man forbereder og produserer søknader for legemiddelgodkjenning. Reglene beskytter helsen til både offentligheten og sikrer at bare trygge legemer er tilgjengelige.

 EN
EN
 AR
AR
 HR
HR
 CS
CS
 DA
DA
 NL
NL
 FI
FI
 FR
FR
 DE
DE
 EL
EL
 IT
IT
 JA
JA
 KO
KO
 NO
NO
 PL
PL
 PT
PT
 RO
RO
 RU
RU
 ES
ES
 SV
SV
 IW
IW
 ID
ID
 LV
LV
 LT
LT
 SR
SR
 SK
SK
 SL
SL
 UK
UK
 VI
VI
 ET
ET
 HU
HU
 TH
TH
 TR
TR
 FA
FA
 AF
AF
 MS
MS
 BE
BE
 MK
MK
 UR
UR
 BN
BN